
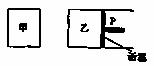
18. (6分)现有可逆反应:A(g)+2B(g) C(g)+D(g);△H<0。在相同温度下,将1mol
A和2mol B加入到容积固定不变的甲容器中,将2mol C和2mol
D加入到容积可变的乙容器中,t1=5min时两容器内均达到平衡状态,甲中c(C)=1.5mol/L。请回答下列问题:
(6分)现有可逆反应:A(g)+2B(g) C(g)+D(g);△H<0。在相同温度下,将1mol
A和2mol B加入到容积固定不变的甲容器中,将2mol C和2mol
D加入到容积可变的乙容器中,t1=5min时两容器内均达到平衡状态,甲中c(C)=1.5mol/L。请回答下列问题:
(1)5min内,用B物质表示甲容器中的平均反应率度v(B)= 。
(2)若使甲容器化学平衡向正反应方向移动,则可以改变的条件是(填写字母) ;
改变条件的瞬间,体系的正反应速率将 。(填“增大”、“减小”、“不变”)
A.减小A的物质的量 B.降低体系的温度
C.增大D的浓度 D.加入催化剂
(3)保持温度不变,移动活塞P,使乙的容积和甲相等,达到新的平衡后,乙容器中C的物质的量浓度c(C) (填“>”“<”“=”)3mol/L。
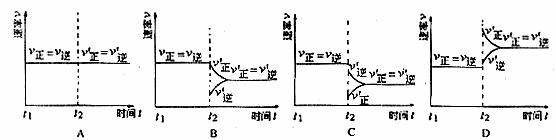
(4)保持温度不变,t2时分别向甲、乙中加入等质量的氦气后,下图中能表示甲中反应速率变化情况的是 ,能表示乙中反应速率变化情况的是 。
17.(9分)A、B、C、D为四种短周期主族元素,其中A、C同族,B、C同周期,D与A、B不在同周期;A原子最外层电子数是核外电子层数的3倍;B的最高正价与最低负价代数和为6。
(1)B的原子结构示意图是 ;实验室制备B单质的离子反应方程式是 。
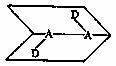
(2)D2A2结构如图所示(两个平面的夹角是93°51′,D-A-A夹角96°52′),D2A2分子属于 (填“极性”或“非极性”)分子。
(3)D2A2溶液与D2C反应生成一种淡黄色的沉淀,该反应的化学方程式是 。
(4)经测定,D2A2为二元弱酸,其酸性比碳酸的还要弱,请写出其第一步电离的电离方程式 。过去常用硫酸处理BaO2来制备D2A2,写出该反应的化学方程式 ;现在实验室可以将过氧化钠加入到水中来制取D2A2,写出该反应的化学方程式 ;简述这两种制备原理的不同之处 。
16.25℃时,在25mL 0.1mol/L的NaOH溶液中,逐滴加入0.2mol/L的CH3COOH溶液,溶液的pH变化如图所示,下列分析结论中正确的是 ( )
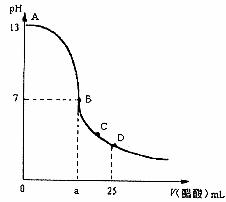
A.B点的横坐标a=12.5
B.C点时溶液中有:
c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
C.D点时溶液中有:
c(CH3COO-)+c(CH3COOH)=2c(Na+)
D.曲线上A、B间的任意一点,溶液中都有:
c(Na+)> c(CH3COO-)> c(OH-)>c(H+)
|
15.25℃时,20.00mL硫酸和硝酸的混合溶液,加入足量氯化钡溶液,充分反应后过滤、洗涤、烘干,可得0.466g 沉淀。滤液跟2.00mol/L氢氧化钠溶液反应,共用去10.00mL碱液时恰好中和。下列说法中正确的是 ( )
A.原混合液中c(SO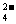 )=0.20mol/L
)=0.20mol/L
B.原混合液中c(NO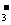 )=0.90mol/L
)=0.90mol/L
C.原混合液中pH=0
D.原混合液中由水电离出的c(H+)=0.10mol/L
14.分子组成为C9H12苯的同系物,已知苯环上只有一个取代基,下列说法中正确的是( )
A.该有机物不能发生加成反应,但能发生取代反应
B.该有机物不能使酸性的高锰酸钾溶液褪色,但能使溴水褪色
C.该有机物分子中的所有原子可能在同一平面上
D.该有机物有一溴代物最多有6种同分异构体
13.阿伏加德罗常数约为6.02×1023mol-1,下列说法中正确的是 ( )
A.2.4g镁作还原剂时失去电子数是0.1×6.02×1023
B.标准状况下,22.4L甲烷中含有的共价键数是6.02×1023
C.标准状况下,5.6L的甲醛所含的电子数4×6.02×1023
D.100 mL 1mol/L氨水溶液中,铵根离子的个数是0.1×6.02×1023
11.糖类、油脂和蛋白质都是人类必需的基本营养物质,下列关于它们的说法中不正确的是
( )
A.淀粉、油脂和蛋白质都能发生水解反应
B.糖类、油脂和蛋白质都属于高分子化合物
C.人们可以利用电泳来分离某些氨基酸和蛋白质
D.可以利用丁达尔效应来鉴别葡萄糖和淀粉溶液

|
下列叙述不正确的是 ( )
A.放电时锌做负极
B.充电时氢氧化铁被氧化
C.充电时溶液的碱性减弱
D.放电时每转移3mol电子,有2mol FeO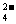 被还原
被还原
9.将2molX和2mol Y充入2L密闭容器中发生如下反应:
 X(g)+3Y(g) 2Z(g)+aQ(g)
X(g)+3Y(g) 2Z(g)+aQ(g)
达到平衡时生成0.8mol Z,测得Q的浓度为0.4mol/L,下列叙述错误的是 ( )
A.a的值为2 B.平衡时X的浓度为0.2mol/L
C.平衡时Y的转化率为60% D.平衡时Z的体积百分含量20%
|
①过氧化钠、硫 ②乙醛、苯、四氯化碳 ③无水硫酸铜、碳酸钡、氯化钠
A.蒸馏水 B.AgNO3溶液 C.汽油 D.乙醇
8.已知X、Y、Z、W四种短周期主族元素在周期表中的相对位置如图所示,下列说法正确的是 ( )
|
B.Z元素的最高化合价可能比Y元素的高
C.W的气态氢化物的稳定性一定比Y的强
D.Z的最高价氧化物的水化物的酸性一定比W的强
7.下列实验操作正确的是 ( )
A.蒸馏时,将温度计的水银球插入液面下
B.称量时,将硫酸铜晶体直接放在天平右盘上称量
C.加热时,将烧杯、试管直接放在酒精灯上加热
D.闻气时,将少量的气体用手轻轻扇入算孔中
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com