
3.金属活动性的强弱与人类开发利用这些金属单质的时间顺序有着某种内在联系。由此推断,下列金属中人类开发利用最晚的是: ( )
A.Cu B.Fe C.Zn D.Al
2.1989 年世界卫生组织把铝确定为食品污染源之一,应加以控制使用。铝在下列应用时应加以控制的是①制铝合金 ②制电线 ③制炊具 ④明矾净水 ⑤明矾与苏打制食品膨松剂 ⑥用氢氧化铝凝胶制胃舒平药片 ⑦银色漆颜料 ⑧易拉罐 ⑨包装糖果和小食品( )
A.③⑤⑧⑨ B.⑥⑧⑨ C.③⑤⑨ D.③④⑤⑥⑧⑨
1.解放日报2004年10月14日报道:德国科学家日前利用卫星数据和一种先进的仪器,绘制了一幅地球上空二氧化氮的分布图。从科学家绘制的二氧化氮分布图看,欧洲和北美洲的一些大城市上空二氧化氮密度很高。近几年,珠江三角洲地区也有类似的情况,其原因是这些地区的: ( )
A.硝酸工业发达 B.雷雨天气较多
C.燃料以煤为主 D.机动车辆过多
31.(6分)在标准状况下将560L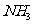 溶于1L水中,所得溶液的密度为
溶于1L水中,所得溶液的密度为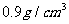 ,求该溶液中溶质的质量分数和物质的量浓度?
,求该溶液中溶质的质量分数和物质的量浓度?
30.(6分)将6.5gZn加到500mL 1 mol/L盐酸中,计算:
(1)在标准状况下,生成氢气的体积。
(2)若反应完全后,溶液的体积仍为500mL,这时溶液中的Zn2+ 和H+ 的物质的量浓度是多少?
29.(14分)(1)下列有关仪器刻度位置的叙述正确的是___________
A.容量瓶的体积标线刻在瓶颈上;
B.量筒的“0”标线在中间;
C.量筒最下端刻有“0”标线;
D.托盘天平刻度尺有“0”标线,在刻度尺的中间。
(2)下列关于托盘天平的使用叙述不正确的是__________
A.称量前先调节托盘天平的零点
B.称量时左盘放被称量物,右盘放砝码
C.易潮解或有腐蚀性的药品,必须放在玻璃皿里称量,其他固体药品可直接放在天平托盘上称量
D.用托盘天平可以准确称量至0.01g E.称量完毕,应把砝码放回砝码盒中
(3)用18mol/L浓硫酸配制100mL 1.0mol/L的稀硫酸,若实验仪器有:
A.100mL量筒 B.托盘天平 C.玻璃棒 D.50mL容量瓶
E.10mL量筒 F.胶头滴管 G.50mL烧杯 H.100mL容量瓶
实验时选用仪器的先后顺序是(填入编号)__ ____
(4)在容量瓶的使用方法中,下列操作不正确的是_____ ______(填写标号)
A.使用容量瓶前检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配溶液润洗
C.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,加入蒸馏水到接近刻度线2-3cm处,用胶头滴管滴加蒸馏水到刻度线
D.配制溶液时,如果试样是液体,用量筒量取试样后直接倒入容量瓶中,缓慢加入蒸馏水到接近刻度线2-3cm处,用滴管滴加蒸馏水到刻度线
E.盖好瓶塞,用食指顶住瓶塞,用另一只手指托住瓶底,把容量瓶倒转和摇动几次。
(5)下列操作对所配溶液的浓度有何影响?为什么?
①在未降至室温时,立即将溶液转移至容量瓶定容:
②定容后,加盖倒转摇匀后,发现溶面低于刻度线,又滴加蒸馏水至刻度: 。
③一定容时发现液面高于刻度线,用胶头滴管吸出部分水后直到于刻度线齐平: 。
28.(2分)在体积为VL的干燥烧瓶中,用排空气收集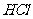 后,测得瓶中的气体对
后,测得瓶中的气体对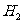 的相对密度为
的相对密度为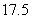 ,所以气体进行喷泉实验,当喷泉停止后,进入烧瓶中水的体积为____
,所以气体进行喷泉实验,当喷泉停止后,进入烧瓶中水的体积为____
27.(2分)某溶液只含有Na+、Al3+、Cl-、SO2- 四种离子,已知Na+、Al3+、Cl- 三种离子的物质的量浓度分别为3mol/L、2 mol/L、1 mol/L,则溶液中SO2-的物质的量浓度为________________。
26.(10分)有A、B、C、D、E 5瓶溶液.分别是HCl、CaCl2、Na2CO3、AgNO3、KI溶液.现将瓶内溶液各取少许进行两两混合实验.结果见图(图中“↓”、“↑”、“─”符号分别表示生成沉淀,气体和无明显变化),由以上实验结果判断各瓶内所装溶液是:
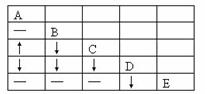
A.
B.
C.
D.
E.
25.(12分)漂白粉在生活、工业生产中用途广泛,漂白粉除了具有漂白作用外,还能杀菌消毒。2003年抗“非典”期间,各商场漂白粉及其他漂白产品曾一度脱销。
(1)1998年,我国长江流域和松花江流域都发生了百年不遇的特大洪水。灾区人民的饮用水,必须用漂白粉等药品消毒后才能饮用,以防传染病发生,但瓶装漂白粉久置空气中会失效。试用化学方程式表示漂白粉在空气中易失效的原因:① ___________ ② _________________ 。
(2)已知浓盐酸和次氯酸钙能发生如下反应:
Ca(ClO)2 +4HCl(浓)===CaCl2+2Cl2↑+2H2O
用贮存很久的漂白粉与浓盐酸制得的氯气中,可能有的杂质气体是 ( )
①CO2 ②HCl ③H2O ④O2
A.①②③ B.②③④ C.②③ D.①④
(3)用Cl2和石灰乳制作漂白粉的目的是 ( )
A.转变为较HClO稳定且易储运的物质
B.转变为更易容于水的物质
C.提高氯气的利用率
D.增强漂白能力
(4)用Cl2和石灰乳制作漂白粉的反应方程式
其成分是 有效成分是 (填名称)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com