
7.石材的放射性常用镭(Ra)作为标准,居里夫人(Marie Curie)因对Ra元素的研究两度 获得诺贝尔奖。下列叙述正确的是 ( )
A.一个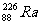 原子中含有138个中子
原子中含有138个中子
B.Ra元素们于元素周期表中第六周期IIA族
C.RaC12的熔点比CaC12高
D.Ra(OH)2是一种两性氢氧化物
6.下列各组关于强电解质、弱电解质、非电解质的归类,完全正确的是 ( )
|
|
A |
B |
C |
D |
|
强电解质 |
Fe |
NaC1 |
CaCO3 |
HNO3 |
|
弱电解质 |
CH3COOH |
NH3 |
HC1O |
Fe(OH)3 |
|
非电银质 |
C12H22O11 |
BaSO4 |
C2H5OH |
H2O |
5.物质发生化学反应是:①电子总数 ②原子总数 ③分子总数 ④物质的种类 ⑤物质的总质量 ⑥物质的总能量,反应前后不发生变化的是: ( )
A.④⑤⑥ B.②⑤⑥ C.①②③⑤ D.①②⑤
4.设NA表示阿伏加德罗常数的值,下列叙述正确的是 ( )
A.标准状况下,NA个SO3分子所占的体积约为22.4L
B.7.8g Na2O2固体中所含离子的总数为0.4NA
C.1.8g重水(D2O)中所含质子的个数为NA
D.在常温常压下,46gNO2和N2O4混合物中所含原子的数为3NA
3.常温下某溶液中由水电离产生的c(OH-)=1×10-10mol·L-1,该溶液的溶质不可能是( )
A.NaHSO4 B.A12(SO4)3 C.NaOH D.HC1
2.据报道,2007年3月10日,在丹江口市有一辆满载10t白磷的卡车因急刹车而导致磷突 然起火,并引发周围区域火灾,事故共造成79人受伤。下列说法正确的是 ( )
A.白磷是红磷的同素异形体,它们有相同的物理性质和化学性质
B.生活污水含有磷元素,排人江河易使水体富营养化,造成藻类过分繁殖,影响水质
C.少量白磷通常保存在CS2中
D.实验室未用完的白磷应弃入废液缸中
1.下列实际应用与胶体知识无关的是 ( )
A.工业生产有色玻璃 B.明矾净水
C.冶金工业用高压电除尘 D.甘油加水作护肤剂
29.(10分)化学键的键能是指气态原子间形成1mol化学键时释放的能量。
如H(g)+I(g)→H-1(g),△H=-297kJ/mol即H-I键的键能为297kJ·mol-1,也可以理解为破坏1molH-I键需要吸收297kJ的热量。一个化学反应一般都有旧化学键的破坏和新化学键的形成。下表是一些键能数据(kJ·mol-1)
|
|
键能 |
|
键能 |
|
键能 |
|
键能 |
|
H H |
436 |
C1-C1 |
243 |
H-C1 |
432 |
H-O |
464 |
|
S=S |
255 |
H-S |
339 |
C-F |
427 |
C-O |
347 |
|
C-C1 |
330 |
C-1 |
218 |
H-F |
565 |
N≡N |
941 |
回答下列问题:
(1)由表中数据能不能得出这样的结论:
①半径越小的原子形成的共阶键越牢固(即键能越大) (填“能”或“不能”)
②非金属性越强的原子形成的共价键越牢固 (填“能”或“不能”)
(2)能否从数据找出一些规律,请写出一条 。
(3)由热化学方程式H2(g)+C12(s)→2H2S(g);△H=-185kJ·mol-1并结合表上数据可推知一个化学反应的反应热(设反应物生成物均为气态)与反应物和生成物的键能之间的关系是 。
(4)由热化学方程式2H2(g)+S2(s)→2H2S(g);△H=-224.5kJ·mol-1种表中数值可计算出1molS2(s)气化时的△H为 。
(5)通过上表预测卤代烃RX在同样条件下发生碱性水解反应时,RF、RC1、RBr、RI(R相同)的反应活性由大到小的顺序是 。
28.请根据下图作答:
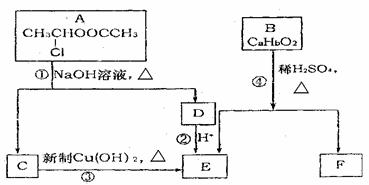
已知:一个碳原子上连有两个羟基时,易发生下列转化:
 R
O
R
O
| ||
HO-CH-OH R-C-H
(1)E中含有的官能团是 。
(2)反应③的化学方程式是 。
(3)已知B的相对分子质量为162,其完全燃烧的产物中n(CO2):n(H2O)=2:1,则B的分子式为 。
(4)F是高分子光阻剂生产的主要原料。F具有如下特点:
①能跟FeC13溶液发生显色反应;
②能发生加聚反应;
③苯环上的一氯代物只有两种。
F在一定条件下发生加聚反应的化学方程式为 。
(5)化合物G是F的同分异构体,属于芳香族化合物,能发生银镜反应。G有多种结构,写出其中一种的结构简式 。
27.(共10分)重氮甲烷在有机合成中有重要应用,可以用来合成甲醚、羟酸、酯类等重要有机产物。重氮甲烷的分子结构可以表示为CH2-N≡N,在其分子中,碳原子和氮原子之间的共用电子对是由氮原子一方提供的。
(1)重氮甲烷的电子式为 。
(2)重氮甲烷在受热或光照时容易分解放出氮气,同时生成一个极活泼的缺电子基团亚甲基或称为碳稀(:CH2)。写出重氮甲烷受热分解的化学方程式 。
(3)碳烯很容易与稀烃、炔烃发生加成反应,生成三元环状化合物。碳烯现丙烯发生加成反应后所得产物的结构简式为 。
(4)碳烯还可以插入到C-H键,C-C键之间,使碳链加长,当它插入丙烷分子中C-H键之间得到的化合物的结构简式为 。
(5)从绿色化学的角度看,碳烯(:CH2)用于合成物质的明显优点是
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com