
17.混合下列各组物质使之充分反应并加热蒸干,产物灼烧至质量不变,最终残留固体不是纯净物的是 ( )
A.在NaBr溶液中通入过量氯气
B.等物质的量浓度,等体积的(NH4)2SO4溶液与BaC12溶液混合
C.物质的量之比为2:1的NaHCO3与Na2O2固体溶于水中
D.向Na2SiO3溶液中通入足量的CO2
16. 某新型二次锂离子电池结构如下图,电池内部是固体电解质,充电、放电时允许Li+在其间通过(图中电池内部“→”表示放电时Li+的迁移方向)。充电、放电时总反应可表
某新型二次锂离子电池结构如下图,电池内部是固体电解质,充电、放电时允许Li+在其间通过(图中电池内部“→”表示放电时Li+的迁移方向)。充电、放电时总反应可表
 示为:LiCoC2+6C Li1-xCoO2+LixC6。下列说法正确的是
( )
示为:LiCoC2+6C Li1-xCoO2+LixC6。下列说法正确的是
( )
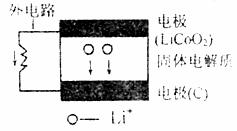
A.外电路上的“→”表示放电时的电流方和
B.充电时发生还原反应的物质是LixC6
C.放电时负极的电极反应为:LiCoO2-xe‑=Li1-xCoO2+xLi+
D.外电路有0.1mole-通过,发生迁移的Li+的质量为0.7xg
15.经测定某种溶液中只含NH4+、C1-、H+、OH-四种离子,下列说法错误的是 ( )
A.溶液中四种离子之间可能满足:c(C1-)>c(H+)>c(NH4+)>c(OH-)
B.若溶液中离子间满足:c(NH4+)>c(C1-)>c(OH-)>c(H+),则溶液中溶质一
定是NH4C1和NH3·H2O
C.若溶液中离子间满足:c(C1-)=c(NH4+)>c(OH-)=c(H+),则溶液中溶质只
有NH4C1
D.若溶液中离子间满足:c(NH4+)=c(C1-),则溶液一定呈中性
14.由一种阳离子与两种酸根离子组成的盐称为混盐。混盐CaOC12在酸性条件下可以产生C12。下列关于混盐CaOC12的有关判断不正确的是 ( )
A.该混盐与硫酸反应产生1molC12时转移2NA个电子
B.该混盐的水溶液呈碱性
C.该混盐具有较强的氧化性
D.该混盐中氯元素的化合价为+1和-1
13.R、M、T、G、J为原子序数依次递增的同一周期主族元素,下列说法一定正确的是(m、n均为正整数) ( )
A.若M(OH)n+1为强碱,则R(OH)n也为强碱
B.若HnJOm为强酸,则G是位于VA以后的活泼非金属元素
C.若T的最低化合价为-3,则J的最高正化合价为+7
D.若M的最高正化合价为+4,则五种元素都是非金属元素
12.MnO2和Zn是制造干电池的重要原料,工业上用软锰矿和闪锌矿联合生产MnO2和Zn的基本步骤为:
①软锰矿、闪锌矿与硫酸共热:MnO2+ZnS+2H2SO4=MnSO4+ZnSO4+S+2H2O
|
③电解混合液:MnSO4+ZnSO4+2H2O MnO2+Zn+2H2SO4
下列说法不正确的是 ( )
A.步骤①中MnO2和H2SO4都是氧化剂
B.步骤①中每析出12.8g S沉淀共转移0.8mol电子
C.电解时MnO2在阳极处产生
D.硫酸在生产中可循环使用
11.在一种酸性溶液中,可能存在NO3-、I-、C1-、Fe3+中的一种或几种离子,向该溶液中加入溴水,溴单质被还原,则以下的推测中不正确的是 ( )
A.一定有碘离子 B.不含铁离子
C.一定有氯离子 D.不含硝酸根离子
10.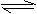 已知某可逆反应的密闭容器中进行,化学方程式为A(g)+2B(g) 3C(g)+D(s),反应放出热量。图中a曲线代表一定条件下该反应的过程。若使a曲线变为b曲线, 可采取
已知某可逆反应的密闭容器中进行,化学方程式为A(g)+2B(g) 3C(g)+D(s),反应放出热量。图中a曲线代表一定条件下该反应的过程。若使a曲线变为b曲线, 可采取
|
①增大A的浓度 ②缩小容器的容积 ③加入催化剂 ④升高温度
A.①③ B.②④ C.②③ D.③④
9.下列有关沉淀溶解平衡的说法正确的是 ( )
A.KSP(AB2)小于KSP(CD),则AB2的溶解度小于CD的溶解度
B.在氯化银的沉淀溶解平衡体系中,加入蒸馏水,氯化银的KSP增大
C.在氯化银的沉淀溶解平衡体系中,加入碘化钾固体,氯化银沉淀可转化为碘化银沉 淀
D.在碳酸钙的沉淀溶液平衡体系中,通入CO2气体,溶解平衡不移动
8.NA表示阿伏加德罗常数的值,下列说法正确的是 ( )
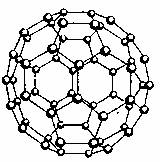
A.在含有NA个CH3COO-的醋酸溶液中,H+数目略大于NA
B.N60结构如右图,28gN60单质中含有的N-N键个数为NA
C.2.9g熟石膏(2CaSO4·H2O)含有的结晶水分子数为0.02NA
D.在标准状况下,2.24L和CC14中含有C-C1键的数目为0.4NA
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com