
25.(10分)有X、Y、Z、W四种在中学学过的固体化合物,实验现象如下:
①X、Y、Z、W的焰色反应均为黄色。
②在Z、W中加入稀盐酸,均有无色、无气味的气体放出。
③Y、Z、W分别与适量的Ba(OH)2浓溶液反应,均有白色沉淀生成;再加入过量盐酸,由Z、W生成的白色沉淀均溶解,由Y生成的白色沉淀不溶解。
④在相同条件下,将足量的Y的溶液分别加到相同物质的量浓度、相同体积的Z和W的溶液中,都有气泡出现。其中W溶液中气泡出现较快。
⑤X与CO2反应生成Z,同时生成另一种气体,此气体由地壳中含量最多的元素组成。
根据上述现象,回答下列问题:
(1)X的电子式为 ,Y的化学式为 ;
(2)X在通常状况下的颜色为 ,它的晶体类型是 ;
(3)写出下列有关反应的化学方程式或离子方程式。
①Z+石灰水(离子方程式) ;
②X+ CO2(化学方程式) ;
③W (化学方程式)
。
(化学方程式)
。
24.甲、乙两种物质的溶解度曲线如图所示,下列说法一定正确的是 ( )

A.A点表示T1℃时甲的溶液已饱和,乙的溶液未饱和
B.B点表示T2℃时甲、乙两物质的溶液均达饱和,且两溶液的物质的量浓度相等
C.将T3℃时甲、乙两物质的饱和溶液分别降温至T2℃,析出的乙比析出的甲多
D.若乙中含有少量的甲,可用结晶的方法提纯乙
|
23.在一定温度下,向容积固定不变的密闭容器中充入a mol NO2,发生如下反应:2NO2(g)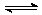 N2O4(g);ΔH < 0。达平衡后再向容器中充入a mol NO2,再次达到平衡后,与原平衡比较,下列叙述不正确的是 ( )
N2O4(g);ΔH < 0。达平衡后再向容器中充入a mol NO2,再次达到平衡后,与原平衡比较,下列叙述不正确的是 ( )
A.相对平均分子质量增大 B.NO2的转化率提高
C.NO2的质量分数增大 D.反应放出的总热量大于原来的2倍
22.在0.1 mol·L-1CH3COOH溶液中存在如下电离平衡:CH3COOH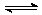 CH3COO-+ H+ 对于该平衡,下列叙述正确的是 ( )
CH3COO-+ H+ 对于该平衡,下列叙述正确的是 ( )
A.加入水时,平衡向逆反应方向移动
B.加入少量NaOH固体,平衡向正反应方向移动
C.加入少量0.1 mol·L-1HCl溶液,溶液中c(H+)减小
D.加入少量CH3COONa固体,平衡向正反应方向移动
21.中国国家主席胡锦涛在中非合作论坛北京峰会上承诺:“提供3亿元人民币无偿援款帮助非洲防治疟疾,用于提供青蒿素药品及设立30个抗疟中心”。中国研制成功的全球唯一的治疗疟疾特效药--青蒿素,是数亿外国人眼中的“中国神药”,结构如图所示。目前售价每克225美元,世界年产量15吨,是需求量的十分之一,供不应求。下列关于青蒿素的说法正确的是

A.是一种烃 B.属于高分子化合物
C.属于芳香族化合物 D.分子式是C15H22O5
20.下列反应的离子方程式书写正确的是
A.氯气与冷水反应: H2O+Cl2=== C1O-+C1-+2H+
B.过量的二氧化碳通入氢氧化钠溶液中 2OH-+CO2===CO32-+H2O
C.碳酸钙溶于醋酸: CaCO3+2H+===Ca2+ +CO2↑+H2O
D.氯化亚铁溶液中通入氯气: 2Fe2++Cl2===2Fe3++2C1-
19.下列除去杂质所用试剂或方法错误的是 ( )
A.除去Na2CO3固体中混有的少量NaHCO3:置于坩埚中加热
B.除去苯中溶有的少量苯酚:加入适量NaOH溶液,反应后分液
C.除去乙酸乙酯中混有的少量乙酸:加入乙醇并加热
D.除去CO2气体中混有的少量HCl:通入饱和NaHCO3溶液洗气
18.对氯化铵溶液的推断错误的是 ( )
A.c(NH4+)+ c(H+) = c(OH-) + c(Cl-) B.c(H+)= c(NH3·H2O)+ c(OH-)
C.c(NH3·H2O)+c(NH4+)= c(Cl-) D.c(NH4+)> c(Cl-)> c(H+)> c(OH-)
17.一定温度下,在固定体积的密闭容器中发生下列反应: 2HI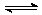 H2+I2;若C(HI)由0.1mol/L降到0.07mol/L时,需要15s,那C(HI)再由0.07mol/L降到0.05mol/L时,所需反应的时间是 ( )
H2+I2;若C(HI)由0.1mol/L降到0.07mol/L时,需要15s,那C(HI)再由0.07mol/L降到0.05mol/L时,所需反应的时间是 ( )
A.等于5s B.等于10s C.大于10s D.小于10s
16.下列各组离子在水溶液中因发生氧化还原反应而不能大量共存的是 ( )
A.H+、K+、CO32-、HCO3- B.Na+、Fe3+、Cl-、I-
C.K+、Al3+、NO3-、AlO2- D.K+、Br-、HCO3-、CO32-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com