
18.一定条件下,在体积为10 L的密闭容器中,1 mol X和1 mol Y进行反应:
2X(g)+Y(g) Z(g),经60 s达到平衡,生成0.3 mol Z,下列说法正确的是 ( )
Z(g),经60 s达到平衡,生成0.3 mol Z,下列说法正确的是 ( )
A.以X浓度变化表示的反应速率为0.001 mol/(L·s)
B.将容器体积变为20 L,Z的平衡浓度变为原来的1/2
C.若增大压强,则物质Y的转化率减小
D.若升高温度,X的体积分数增大,则该反应的DH>0
17.某工厂用CaSO4、NH3、H2O、CO2制备(NH4)2SO4,其工艺流程如下:
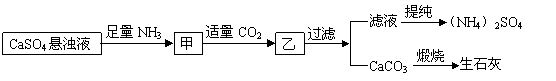

下列推断不合理的是 ( )
A.直接蒸干滤液得到纯净的(NH4)2SO4
B.生成1mol(NH4)2SO4至少消耗2molNH3
C.CO2可被循环使用
D.往甲中通CO2有利于(NH4)2SO4生成
16.以下离子方程式书写正确的是 ( )
A.Cl2溶于水:Cl2+H2O == 2H++Cl-+ClO-
B.氨气通入醋酸溶液中:CH3COOH+NH3=CH3COO-+NH4+
C.向Ca(ClO)2溶液中通入SO2气体:Ca2++2ClO-+SO2+H2O = CaSO3↓+2HClO
D.Al片投入稀硝酸中:2Al+6H+=Al3++3H2↑
15.可用如图装置制取(必要时可加热)、净化、收集的气体是 ( )
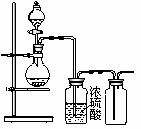
A.铜和稀硝酸制一氧化氮
B.氯化钠与浓硫酸制氯化氢
C.大理石和稀硫酸制二氧化碳
D.硫化亚铁与稀硫酸制硫化氢
14.下列比较正确的是 ( )
A.稳定性:CH4 <SiH4 <GeH4<SnH4 B.离子半径大小:Cl-<Mg2+< O2-<F-
C.熔沸点高低:SiO2> NaCl>CS2>CO2 D.酸性强弱:H2SO3<H3PO4<H2SiO3
13.下列有关工业生产的叙述正确的是 ( )
A.合成氨生产过程中将NH3液化分离,可加快正反应速率,提高N2、H2的转化率
B.硫酸工业中,在接触室安装热交换器是为了利用SO3转化为H2SO4时放出的热量
C.电解饱和食盐水制烧碱采用离子交换膜法,可防止阴极室产生的Cl2进入阳极室
D.电解精炼铜时,同一时间内阳极溶解铜的质量比阴极析出铜的质量小
12.下列叙述正确的是 ( )
A.95 ℃纯水的pH<7,说明加热可导致水呈酸性
B.pH = 3的醋酸溶液,稀释至10倍后pH = 4
C.0.2 mol·L-1的盐酸,与等体积水混合后pH = 1(忽略体积的变化)
D. Na2CO3溶液中:c(Na+) + c(H+) = c(HCO3-) +c(CO32-) + c(OH-)
11.下列说法正确的是 ( )
A.除去CO2中少量的SO2:使混合气体通过盛饱和碳酸钠溶液的洗气瓶;
B.浓硫酸不可以用铝容器存放
C.金属锂可以保存在煤油中, 白磷可以保存在水中。
D.硝酸银应存贮在棕色试剂瓶中
9.下列说法正确的是 ( )
① 非金属氧化物一定不是碱性氧化物
② 电解质溶液的导电过程属于化学变化
③ 盐酸既有氧化性又有还原性
④Fe(OH)3 、FeCl2、SiH4 都不能直接用化合反应制备
⑤SO2能使酸性高锰酸钾溶液褪色,所以它具有漂白性
A.②⑤ B.①②③④ C. ①②③ D.①②③⑤
|
( )
A.①②③ B.①②④ C.①③④ D.②③④
8.将用于2008年北京奥运会的国家游泳中心(水立方)的建筑采用了膜材料ETFE,该材料为四氟乙烯与乙烯的共聚物,四氟乙烯也可与六氟丙烯共聚成聚全氟乙丙烯。下列说法错误的是 ( )
A.ETFE分子中可能存在“-CH2-CH2-CF2-CF2-”的连接方式
B.合成ETFE及合成聚全氟乙丙烯的反应均为加聚反应
C.聚全氟乙丙烯分子的结构简式可能为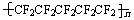
D.四氟乙烯分子中既含有极性键又含有非极性键
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com