
21.(8分)测定一定体积的NaOH和Na2CO3混合溶液中NaOH的含量:取20mL溶液,加入足量BaCl2溶液后,滴入几滴酚酞,再用0.10mol·L-1盐酸进行滴定。
(1)用盐酸进行滴定之前不需要过滤以除去BaCO3的的理由是
;
(2)达到终点时,溶液的颜色变化是 ;
(3)达到终点时消耗25.0mL 的HCl,则原混合液中NaOH的含量为 g/mL;
(4)若向含有大量BaCO3固体的浊液中,分别加入下列试剂,则发生的变化是:
①加入少量BaCl2固体,则c(Ba2+) c(CO32+) (填“增大”、“减少”)。
②加入少量稀盐酸,则Ksp(BaCO3) (填“增大”、“减少”或“不变”)。
(三)问题讨论
(7)酒精灯和酒精喷灯点燃的顺序是 。
(8)为了防止甲中气体收集装置发生的安全问题,可以在不增减仪器种类、数量,不改变其连接方式的前提下进行简单的改造,请在甲中画出你改造之处的示意图。
(二)实验过程
(4)甲同学可以证明两者发生反应的现象是 ;
(5)从反应物元素的种类分析,生成的气体可能是氢气,进一步验证的方法是
;
(6)当玻璃管中的铁粉充分反应后,停止实验,称量反应后固体产物质量为b,则固体产物的化学式为 (用字母表示)。
(一)装置的评价
(1)在水蒸气的生成装置中乙同学在烧瓶底部放置了几片碎瓷片,其作用是 ;
(2)在反应装置中甲同学在硬质玻璃管中放入的是还原铁粉和石棉绒,石棉绒的作用是
;
(3)在收集装置中甲同学用的是排水集气法,这种方法存在的安全隐患是 ;
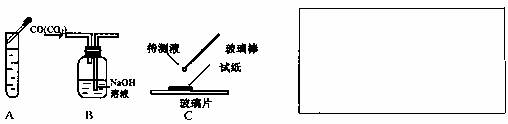
19.(4分)下图为某学生在实验报告中所绘制的实验操作及装置图,如有不正确的请在下面方框中绘制出正确的。
(其中A:向碳酸氢钠溶液中滴加盐酸;B:除去CO气体中的CO2气体;C:检验某溶液的酸碱性。)
20.(11分)常温下,在没有氧气存在时,铁与水几乎不反应。某化学兴趣小组设计实验探究在高温下还原铁粉与水蒸气能够发生反应,并检验其生成物。
甲、乙两同学分别设计了如图所示的两套实验装置(所取的铁粉均为a g):
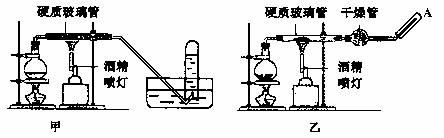
请回答下列问题:
2.答卷前将密超过计划线内的项目和座号填写清楚。
1.用钢笔或圆珠笔直接答在试卷上。
18.取x g铜镁合金完全溶于浓硝酸中,反应过程中硝酸被还原只产生8960mL的NO2气体和672mL N2O4的气体(都已折算到标准状态),在反应后的溶液中加足量的氢氧化钠溶液,生成沉淀质量为17.02g。则x等于 ( )
A.8.64g B.9.20g C.9.00g D.9.44g
第II卷(非选择题 共54分)
|
17.已知:CH3CH2CH2CH3(g)+6.5O2(g)→4CO2(g)+5H2O(l) △H=-2878kJ mol-1
(CH3)2CHCH3(g)+6.5O2(g) →4CO2(g)+5H2O(l) △H=-2869kJ mol-1
下列说法不正确的是 ( )
A.异丁烷分子中的碳氢键比正丁烷的多
B.异丁烷的稳定性大于正丁烷
C.正丁烷转化为异丁烷的过程是一个放热过程
D.正丁烷分子储存的能量大于异丁烷分子
16. 在一定温度下,向体积恒定为2L的密闭容器里充入2mol M和一定量的N,发生如下反应:M(g)+N(g)
E(g);当反应进行到4min时达到平衡,测知M的浓度为0.2mol·L-1。下列说法不正确的是 ( )
在一定温度下,向体积恒定为2L的密闭容器里充入2mol M和一定量的N,发生如下反应:M(g)+N(g)
E(g);当反应进行到4min时达到平衡,测知M的浓度为0.2mol·L-1。下列说法不正确的是 ( )
A.2min时,M的物质的量浓度为0.6mol·L-1
B.4min时,用M表示的反应速率为0.2mol·L-1·min-1
C.4min后,向容器中充入不参与反应的稀有气体,M的物质的量不变
D.4min时,M的转化率为80%
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com