
23.(4分)回答下列问题:
(1)保持恒温,向pH=6的蒸馏水中加入2.3g金属钠,充分反应后,再加蒸馏水稀释到1L,所得溶液的pH= 。
(2)向pH=6的蒸馏水和c(H+)=10-6mol·L-1的稀盐酸中分别投入大小、质量相同的金属钠,反应刚开始时,产生H2的速率前者与后者相比是 (填选项序号)。
A.一样快 B.前者快 C.后者快 D.无法比较
22.下图是一水溶液在pH从 0至14的范围内,H2CO3、HCO3-、CO32-三种成分平衡时的组成百分率[H2CO3]、[HCO3-]、[CO32-],下列叙述正确的是 ( )
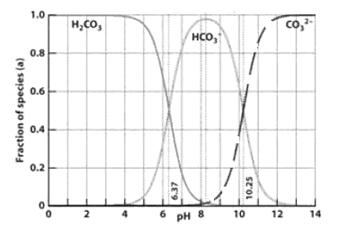
A.此图可完全根据1.0 mol/LHCl溶液滴定1.0mol/L碳酸钠溶液的实验数据绘出
B.1.0 mol/LHCl溶液滴定1.0mol/L碳酸钠溶液恰好反应时呈中性
C.二氧化碳溶解在血液中多以HCO3-的形式存在
D.在pH为6.37及10.25时,溶液中[H2CO3]=[HCO3-]=[CO32-]
第Ⅱ卷(共44分)
|
21.常温下,下列有关叙述正确的是: ( )
A.Na2CO3溶液中,2c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3)
B.NaB溶液的pH=8,c(Na+)-c(B-)=0.99×10-6mol/L
C.pH相等的①NH4Cl、②(NH4)2SO4、③NH4HSO4三种溶液中,c(NH4+)大小顺序①=②>③
D.10mL pH=12的氢氧化钠溶液中加入pH=2的HA至pH刚好等于7,所得溶液体积V(总)≥20mL
20.在一定条件下化学反应:2SO2(g)+O2(g) 2SO3(g);△H=-197kJ/mol。现有容积相同的甲、乙、丙三个容器,在上述条件下分别充入的气体和达到平衡时反应放出的热量(Q)如下表所列:
2SO3(g);△H=-197kJ/mol。现有容积相同的甲、乙、丙三个容器,在上述条件下分别充入的气体和达到平衡时反应放出的热量(Q)如下表所列:
|
容 器 |
SO2(mol) |
O2(mol) |
N2(mol) |
Q(kJ) |
|
甲 |
2 |
1 |
0 |
Q1 |
|
乙 |
1 |
0.5 |
0 |
Q2 |
|
丙 |
1 |
0.5 |
1 |
Q3 |
根据以上数据,下列叙述不正确的是 ( )
A.Q1=2Q2=2Q3=197
B.在上述条件下每消耗2摩SO2气体时放出的热量为197 kJ
C.在上述条件下反应生成1 molSO3气体放热98.5 kJ
D.2Q2=2Q3<Q1<197 kJ
19.有BaCl2和NaCl的混合溶液aL,将它均分成两份。一份滴加稀硫酸,使Ba2+离子完全沉淀;另一份滴加AgNO3溶液,使Cl-离子完全沉淀。反应中消耗xmol H2SO4、ymol AgNO3。据此得知原混合溶液中的c (Na+) (单位: mol·L-1)为: ( )
A.(y-2x)/a B.(y-x)/a C.(2y-2x)/a D.(2y-4x)/a
18.短周期元素A、B、C的原子序数依次递增,它们的原子最外层电子数之和为10,A与C同主族,B原子的最外层电子数等于A原子的次外层电子数,则下列叙述正确的是( )
A.原子半径:A<B<C
B.A的氢化物稳定性大于C的氢化物稳定性
C.三种元素的最高价氧化物对应水化物均可由化合反应得到
D.高温下,A单质能置换出C单质
17.某无色溶液可能有Na2CO3、MgCl2、NaHCO3、BaCl2中的一种或几种。在该溶液中加入NaOH溶液时出现白色沉淀;若加入稀H2SO4,既有白色沉淀又有气体放出。则下列判断中正确的是: ( )
A.肯定有BaCl2 B.一定有MgCl2
C.肯定无NaHCO3 D.Na2 CO3、NaHCO3至少存在一种
16.已知可逆反应A+2B  2M+N;正反应为放热反应,起始投料时A、B中A的质量分数为40%。在一定条件下达到平衡时,A在反应混合物中的质量分数为a%(a<10)
2M+N;正反应为放热反应,起始投料时A、B中A的质量分数为40%。在一定条件下达到平衡时,A在反应混合物中的质量分数为a%(a<10)
若要通过改变条件使A的质量分数变为2a%,则下列各项可改变的条件中一定能达到目的的是 ( )
A.增大容器体积 B.增大反应容器内压强
C.升高反应温度 D.使用适当催化剂
15.某化学兴趣小组用回收的镁铝合金制取氢气。现有l0.8 g镁铝合金,下列说法正确的是( )
A.常温下与足量18mol/LH2SO4溶液反应,最多可放出0.6 mol H2
B.常温下与足量2mol/LHNO3溶液反应,最少可放出0.45 mol H2
C.常温下与足量2 mol/L H2SO4溶液反应,放出H2的物质的量在0.45 mol-0.6 mol之间
D.常温下与足量2mol/LNaOH溶液反应,放出H2的物质的量在0.45 mol-0.6 mol之间
14.某同学按下图所示的装置进行电解实验。下列说法正确的是: ( )
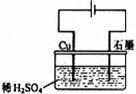
A.电解过程中,铜电极上有H2产生
B.电解初期,主反应方程式为:Cu+H2SO4 CuSO4+H2↑
CuSO4+H2↑
C.电解一定时间后,石墨电极上有铜析出
D.整个电解过程中,H+的浓度不断增大
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com