
11.原子序数依次相差1,且由小到大排列的A、B、C、D、E五种短周期元素。下列有关这五种元素的叙述中,正确的是 ( )
A.若A的单质既能与强酸又与强碱反应且放出氢气,则B元素的氧化物也既能与盐酸反应又能与烧碱溶液反应
B.若B元素的原子最外层电子为4个,则D元素的最高正价一定为+6
C.若A的阳离子比E的阴离子少8个电子,则E元素一定是非金属元素
D.若A的最高价氧化物对应的水化物与A的氢化物可以发生化合反应,则E元素在空气中燃烧生成的化合物中只含离子键
9.十七大把“节能减排”工作放在更加突出的战略位置。下列有关的叙述中,错误的是( )
A.实验室中“通风厨”能排出有害的气体,能防止有害气体污染大气环境
B.减少碳水化合物、氮氧化物的排放可以有效的防止光化学烟雾的产生
C.处理废弃塑料制品较为合理的方法是用化学方法将废弃塑料加工成防水涂料或汽油
D.对废弃电池进行集中回收后处理的主要目的是防止重金离子的污染
|
A.石油的分馏和煤的干馏均属于化学变化
B.乙烷、苯、乙醇、乙酸等均能发生取代反应
C.石油的馏分、聚乙烯、瓦斯气、甘油、蛋白质均是混合物
D.制备乙酸乙酯时,正确加入试剂的顺序是依次将乙醇和乙酸加入到浓硫酸中
8.根据下图,分析下列说法正确的是 ( )
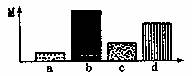
A.若a、b、c、d表示四种溶液,M为萝卜块浸入溶液后增加的重量,则a溶液浓度最低
B.若M表示遗传多样性,a、b、c、d表示四种不同的植物,则在剧烈变化的环境中生存能力最强的是b
C.若M表示某生态系统中某条捕食链a、b、c、d四个营养级的能量比例,则c为初级消费者
D.若M表示细胞中的有机物含量,a、b、c、d表示四类有机物,则表示蛋白质的是d
22.(12分)某有机物的球棍模型如下图所示:
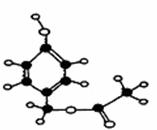
(1)请写出物质的分子式 ,结构简式 。
(2)该物质在一定条件下,可以发生水解反应,生成A、B两种物质(它们的相对分子质量关系是A>B)
①请写出该物质发生水解反应的化学方程式 。
②A有多种同分异构体,请写出具有两种不同官能团的A的同分异构体的结构简式(写出2种即可): 。
(3)1molA分别与Na、NaOH反应,用Na、NaOH物质的量最大值之比是 。
(4)B可以用以下方法制得: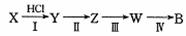 。其中W能发生银镜反应。
。其中W能发生银镜反应。
则I属于 反应,IV属于 反应(填反应类型);写出W发生银镜反应的化学方程式 。
21.(12分)A、B、C、D、E、F六种中学化学中常
见的物质,有下图转化关系。
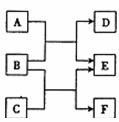
(1)若A、C、E皆为氧化物,且E为有毒气体,B、D、F皆为非金属单质,且D为气体,A与B,B与C均在高温下发生的应,则:A的结构式为 ,单质F的晶体类型为 。1molC中含有 个共价键。
(2)若A、C、E皆为氢化物,具有10个电子或18个电子,三者皆为极性分子,其中C的相对分子质量最小;D、E、F皆为氧化物,其中D、F为有毒气体。则:
①A、C、E沸点从高到低的顺序为 (填化学式)。
②B跟C反应生成E和F的化学方程式为 。
③A跟D常温下反应可生成一种单质,化学方程式为 。
20.(8分)恒温恒溶下,将2molA气体和2molB气体通入容积为2L的密闭容器中发生如下反应:2A(g)+B(g) xC(g)+2D(s)。2min时反应达到平衡状态,此时剩余1.2molB并测得C的浓度为1.2mol/L。
xC(g)+2D(s)。2min时反应达到平衡状态,此时剩余1.2molB并测得C的浓度为1.2mol/L。
(1)x= 。
(2)A的转化率为与B的转化率之比为 。
(3)下列各项能作为该反应的平衡状态标志的是 。
A.压强不再变化
B.气体密度不再变化
C.气体平均式量不再变化
(4)欲使反应达到平衡时C的物质的量分数与上述平衡时相等,起始加入的A、B物质的量n(A)、n(B)满足的关系式为 。
19.(14分)亚氯酸钠(NaCO2)是一种重要的含氯消毒剂,主要用于消毒以及砂糖、油脂的漂白与杀菌。以下是过氧化氢法生产亚氯酸钠的工艺流程图。
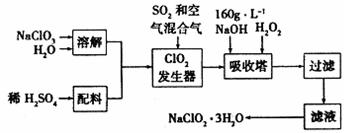
已知:①NaC1O2的溶解度随温度升高而增大,适当条件下可结晶析出NaC1O2·3H2O。
②纯C1O2易分解爆炸,一般用稀有气体或空气稀释到10%以下才安全。
③160g·L-1NaOH溶液是指160gNaOH固体溶于水所得溶液的体积为1L。
(1)160g·L-1NaOH溶液的物质的量浓度为 。若要计算该溶液的质量分数,还需要的一个条件是 (用文字说明)。
(2)发生器中鼓入空气的作用可能是 (选填序号)
A.将SO2氧化成SO3,增强酸性;
B.稀释C1O2以防发生爆炸;
C.将NaC1O3氧化成C1O2
(3)吸收塔内的反应的化学方程式为 。吸收塔的温度不能超过20℃,其目的是防止H2O2分解,写出H2O2分解的化学方程式 。
(4)在碱性溶液中NaC1O2比较稳定,所以吸收塔中应维持NaOH稍过量,判断NaOH是否过量的简单实验方法是 。
(5)吸收塔中为了防止NaCO2被还原成NaC1,所用还原剂的还原性应适中。除H2O2外,还可以选择的还原剂是 (选填序号)。
A.Na2O2 B.Na2S C.FeC12 D.Pbo(悬浊夜)
(6)从滤液中得到NaC1O2·3H2O粗晶体的实验操作依次是 (选填序号)。
A.蒸馏 B.蒸发 C.灼烧 D.过滤
E.冷却结晶
要得到更纯的NaC1O2·3H2O晶体必须进行的操作是 。
18.今有一混合物的水溶液,只可能含有以下离子的若干种:K+、NH4+、C1-、Mg2+、Ba2+、CO32-、SO42-,现取三份100ml溶液做如下实验:
①第一分加入AgNO3溶液有沉淀生成
②第二份加足量NaOH溶液加热后,收集到气体0.04mol
③第三份加入足量BaC12溶液后,得干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g。
根据上述实验,以下推测正确的是 ( )
A.100m1溶液中含0.01molCO32- B.Ba2+一定不存在,Mg2+可能存在
C.K+可能存在 D.C1-可能存在
第Ⅱ卷(非选择题 共46分)
|
注意:第Ⅱ卷用钢笔或圆珠笔直接答在答题卷上。
17.咖啡鞣酸具有广泛的抗菌作用,其结构简式如下所示。关于咖啡鞣酸的下列叙述不正确的是 ( )
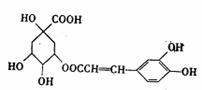
A.分子式为C16H18O9
B.与苯环直接相连的原子都在同一平面上
C.1mol咖啡鞣酸水解时可消耗8molNaOH
D.与浓溴水既能发生取代反应又能发生加成反应
16.仔细分析下列表格中烃的排列规律,判断排列在第15位烃的分子式是 ( )
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
…… |
|
C2H2 |
C2H4 |
C2H6 |
C3H4 |
C3H6 |
C3H8 |
C4H6 |
C4H8 |
C4H10 |
|
A.C6H12 B.C6H14 C.C7H12 D.C7H14
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com