
22.(9分)X、W、Y、Z、V代表原子序数依次减小的五种短周期主族元素,它们满足以下条件:X原子L层电子数是其最外层电子数的2倍;W原子K、L层电子数之和比L、M层电子数之和多1个电子;Z是自然含量最多的元素;V元素形成的化合物种类是所有元素中最多的。请填空:
(1)X元素的原子结构示意图为 。X的最高价氧化物形成的晶体属于 晶体(填“分子”、“原子”、“离子”或“金属”)。
(2)Y、Z两元素形成的氢化物中沸点比较高的是 (填化学式)。
(3)X、W、Y、Z、V五种元素的原子半径由大到小的顺序是 (填元素符号)
(4)W、Z和V可组成一种化合物,其原子个数比为2:3:1,该物质的水溶液中各离子浓度由大到小的顺序是 ;由W、Z和V也可组成另一种化合物,其原子个数比为1:2:1,该化合物的结构简式为 。
21.(4分)用A、B、C、D分别表示含有18个电子的四种分子,请回答:
(1)A是所有含18个电子的微粒中氧化能力最强的分子,其分子式是 。
(2)B是由两种元素组成的三原子分子,其分子是 。
(3)C分子中含有4个原子,其分子式是 。
(4)D分子中含有8个原子,其分子式是 。
20.Bg某金属与足量的稀硫酸反应,生成该金属的三价正盐和ag氢气。则该金属的相对原子质量为 ( )
A.2b/a B.3b/2a C.3b/a D.a/3b
第Ⅱ卷 非选择题(共50分)
|
19. 已知热化学方程式:2SO2(g)+O2(g) 2SO3(g),△H=-QkJ/mol(Q>0)则下列说法正确的是 ( )
已知热化学方程式:2SO2(g)+O2(g) 2SO3(g),△H=-QkJ/mol(Q>0)则下列说法正确的是 ( )
A.相同条件下2molSO2(g)和1molO2(g)所具有能量大于2molSO3(g)所具有的能量
B.将2molSO2(g)和1molO2(g)置于一密闭容器中充分反应后放出QkJ的热量
C.升高温度,平衡向逆反应移动,上述热化学方程式中的Q值将减小
D.如将一定量SO2(g)和O2(g)置于某密闭容器中充分反应后放热QkJ,则此过程中有2mol SO2(g)被还原
18. 已知反应N2(g)+3H2(g) 2NH3(g)
,△H<0,向某体积恒定的密闭容器中按体积比1:3充入N2和H2,在一定条件下发生反应。右图是某物理量(Y)随时间(t)变化的示意图,Y可以是
( )
已知反应N2(g)+3H2(g) 2NH3(g)
,△H<0,向某体积恒定的密闭容器中按体积比1:3充入N2和H2,在一定条件下发生反应。右图是某物理量(Y)随时间(t)变化的示意图,Y可以是
( )
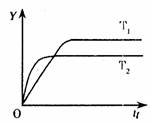
A.N2的转化率 B.混合气体的密度
C.密闭容器的压强 D.H2的体积分数
17.X、Y、Z、W均为短周期元素,它们在周期表中相对位置如图所示。若Y原子的最外层电子数内层电子数的3倍,下列说法中正确的是 ( )

A.原子半径:W>Z>Y>X
B.最高价氧化物对应水化物的酸性W比Z弱
C.Y的气态氢化物的稳定性较Z的弱
D.四种元素的单质中,Z的熔、沸点最高
16.用铂电极分别电解下列物质的溶液,阴极和阳极上同时都有气体产生,且溶液的pH下降的是 ( )
A.H2SO4 B.CuSO4 C.HCl D.KCl
15.浓度均为0.1mol·L-1的三种溶液等体积混合,充分反应后没有沉淀的是 ( )
A.BaCl2 NaOH NaHCO3
B.Na2CO3 MgCl2 H2SO4
C.AlCl3 NH3·H2O NaOH
D.Ba(OH)2 CaCl2 Na2SO4
14.下列离子方程式中正确的是 ( )
A.铝片和氢氧化钠溶液反应:Al+2OH- === AlO-2+H2↑
B.硫酸镁溶液跟氢氧化钡溶液反应:SO-4+Ba2+ === BaSO4↓
C.硫化钠溶于水中:S2-+2H2O = H2S↑+2OH-
D.苯酚钠溶液中通入少量CO2:
13.下图是某只含有C、H、O、N的有机物简易球棍模型。下列关于该有机物的说法正确的是 ( )
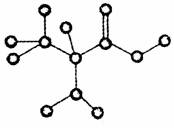
A.分子式为C3H8NO2
B.在一定条件下,可以通过聚合反应,生成高分子化合物
C.不能和盐酸反应
D.一定条件下能和CH3COOH反应,生成酯类化合物
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com