
29.(15分)A~I9种有机物有如下转化关系。有机物A的结构简式为:
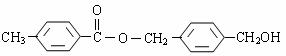 ;H的分子式为C12H14O4;I与H互为同分异构体;E的一种相邻同系物是室内装修空气污染的一种主要成分。已知
;H的分子式为C12H14O4;I与H互为同分异构体;E的一种相邻同系物是室内装修空气污染的一种主要成分。已知
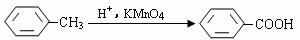
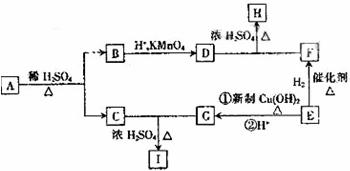
试回答下列问题:
(1)G中所含官能团的名称为_____________,E→F的反应类型为_____________。
(2)写出下列物质的结构简式:
B______________________,C______________________,E_________________。
(3)与B互为同分异构体,且苯环上只有一个取代基的有机物结构简式有4种,除
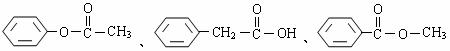 外,
外,
还有_______________________。
(4)D+F→H的化学方程式为_____________________________。
28.(16分)某研究性学习小组同学查阅资料得知,漂白粉与硫酸溶液反应可制取氯气,化学方程式Ca(ClO)2 + CaCl2 + 2H2SO4
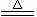 2CaSO4 + 2Cl2↑ + 2H2O,他们设计了如下图制取氯气并验证其性质的实验装置:
2CaSO4 + 2Cl2↑ + 2H2O,他们设计了如下图制取氯气并验证其性质的实验装置:
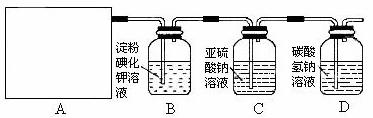
请回答下列问题:
(1)该实验中A部分的装置是___________(填写装置的序号)。
(2)A中发生反应一段时间后,B中的现象是_______________;整套实验装置存在的明显缺陷是_________________。
(3)写出D装置中发生反应的离子方程式______________________________。
(4)请你帮该小组同学设计一个实验,证明洗气瓶C中的Na2SO4已被氧化(简述实验步骤):______________________________
(5)该小组同学又进行了如下实验:称取漂白粉2.0g,研磨后溶解,配制后溶解,配制成250mL溶液,然后取出25mL溶液加入到锥形瓶中,再加入过量的KI溶液和过量的H2SO4溶液,静置。待完全反应后,用0.1mol·L-1的Na2SO4溶液做标准液滴定反应生成的碘,已知反应的化学方程式为2Na2S2O3 + I2 ==== Na2S4O6 + 2NaI, 共用去Na2S2O3溶液20.00mL,则放漂白粉中Ca(ClO)2的质量分数为______________。
27.(14分)有A、B、C、D四种可溶于水的电解质,它们在溶液中电离出的阴、阳离子分别是以下两组离子中的各一种(每种离子只出现一次)。
|
阳离子 |
Ag+ NH4+ Mg2+ |
|
阴离子 |
Cl- SO42- NO3- OH- |
现进行下列实验:将B的溶液分别加到A、D两溶液中均产生稳定的白色沉淀;C、D两溶液适量混合产生蓝色沉淀,C中阳离子与阴离子的质量比为2:3.据此回答下列问题:
(1)推断出四种电解质的化学式:
A_________,B_________,C__________,D______________。
(2)将D溶液逐滴加在A溶液中的现象为_______________________________________。
(3)C、D两溶液反应产生蓝色沉淀的离子方程式为____________________________。
26.下表中的实线表示元素周期表的部分连界,①~⑧分别表示元素周期表中对应位置的元素。
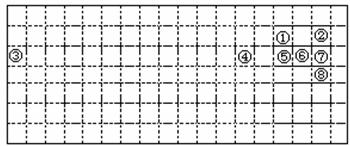
(1)请在表中用实线补全元素周期表上方边界。
(2)元素②③④⑥的原子半径由大到小的顺序是_____________(用元素符号表示)。元素⑤和⑥诉最高价氧化物对应的水化物中,酸性较弱的物质的化学式为_________。
(3)元素②⑦⑧的氢化物的沸点由高到低的顺序为___________(用化学式表示)。
(4)元素①的气态氢化物的化学式为________,该分子属于________(填“极性”或“非极性”)分子。
(5)元素③与⑦形成的化合物是一种重要的工业原料,写出工业上电解其水溶液时反应的离子方程式:______________。
13.在某体积固定的密闭容器中发生如下可逆反应:A(g)+B(g) 2C(g),在反应过程中体系的温度不断升高,实验测得混合气体中C的含量与温度关系如图所示,下列说法中正确的是 ( )
2C(g),在反应过程中体系的温度不断升高,实验测得混合气体中C的含量与温度关系如图所示,下列说法中正确的是 ( )
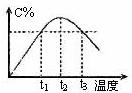
A.此反应的正反应吸热反应
B.反应在t3温度时气体对容器的压强比t1温度时大
C.t3温度时正反应速率大于逆反应速率
D.t3温度时正反应速率大于t1温度时正反应速率
|
12.对室温下体积相同,浓度均为0.1mol·L-1的盐酸和醋酸两种溶液分别采取下列措施。有关叙述中一定正确的是 ( )
A.加入稀释100倍后,两溶液的pH相同
B.加入NaOH固体恰好中和后,丙溶液的pH相同
C.加入足量的小苏打固体充分反应后,两溶液中产生的CO2一样多
D.分别加入足量的锌粉充分反应,反应开始时两酸产生H2的反应速率相等
11.下列离子方程式中正确的是 ( )
A.镁条溶于稀硝酸:Mg+2H+===Mg2++H2↑
B.氯化铁溶液中滴入硫氰化钾溶液:Fe3++2SCN-==Fe(SCN)2
C.把铝片加入到氢氧化钠溶液中:2Al+2OH-+2H2O==2AlO3+3H2↑
D.硫酸铁溶液中加入铁粉:Fe3++Fe==2Fe2+
9. 用NA表示阿伏加德罗常数的数值,下列说法中正确的是 ( )
A.0.2mol过氧化氢完全分解电子数为0.4NA
B.300mL 2mol·L-1庶糖溶液中所含分子九为0.6NA
C.在常温常压下,17g硫化氢所含质子数为8NA
D.在标准状况下,二氧化硫一氧气的混合气体2.24L中所含氧原子数为0.2NA
|
A.Na B.Na2O2 C.Na2CO3 D.NaHCO3
8. 下列是几种不同燃料的热值:
|
物质 |
天然气 |
氢气 |
乙炔 |
甲醇 |
|
热值/kJ·g-1 |
56 |
143 |
50 |
23 |
在等物质的量的情况下,充分燃烧放热最多的是 ( )
A.天然气 B.氢气 C.乙炔 D.甲醇
7. 在下列生成二氧化硫的反应中,硫元素被氧化的是 ( )
A.硫在空气中燃烧 B.铜片与浓硫酸共热
C.红热的木炭与浓硫酸反应 D.亚硫酸钠与稀硫酸反应
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com