
7.氢元素与其他元素形成的二元化合物称为氢化物,下面关于氢化物的叙述正确的是( )
A.一个D2O分子所含的中子数为8
B.HCl的电子式为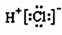
C.NH3的结构式为: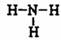
D.热稳定性:H2S>HF
6.下列有关铁元素的叙述中正确的是 ( )
A.氢氧化铁可以由相关物质通过化合反应而制得
B.铁是较活泼的金属,它与卤素(X2)反应的生成物均为FeX3
C.氢氧化铁与氢碘酸反应:Fe(OH)3+3HI=FeI3+3H2O
D.铁元素位于周期表的第四周第VIIIB族
5.下列有关实验中,用所选用试剂(括号内物质)不能达到目的是 ( )
A.证明FeCl2溶液被氧化(KSCN溶液)
B.除去C2H2中的H2S气体(CuSO4溶液)
C.鉴别SO2和CO2两种气体(溴水)
D.检验Na2SO4溶液中是否混有NaCl(AgNO3)溶液
4.下列离子方程式正确的是 ( )
A.澄清的石灰水与稀盐酸反应Ca(OH)2+2H+ = Ca2++2H2O
B.钠与水的反应Na+2H2O = Na+ + 2OH-+ H2↑
C.大理石溶于醋酸的反应CaCO3+2CH3COOH = Ca2++2CH2COO-+CO2↑+H2O
D.氯气通入冷的氢氧化钠溶液中2Cl2+2OH- = 3Cl-+ClO-+H2O
3.NA表示阿伏加德罗常数,下列说法正确的是 ( )
A.由最外层有1个电子的微粒构成的单质与1molO2反应时转移电子数4NA
B.6 g SiO2晶体中,含有Si-O键数为0.2NA
C.17g氨气溶于水,得到NH3·H2O的分子数为NA
D.0.5mol羟基中含有的电子数为4.5NA
2.下列说法正确的是 ( )
A.氢化物的熔点:NH3<PH3<AsH3
B.分子式为CnH2n+2的一切物质(n为不相等的自然数)互为同系物
C.在水溶液中导电能力强的化合物是强电解质,导电能力弱的化合物是弱电解质
D.N+5离子中含有36个电子
1.下列说法中,正确的是 ( )
A.用在航空航天器中的抗氧化陶瓷复合材料属于新型无机非金属材料
B.提倡使用乙醇汽油主要是为了提高汽油的燃烧效率
C.赤潮、潮汐、酸雨、臭氧空洞都是与环境污染有关的现象
D.在松花江污染事件中,使用活性炭减少污染是因为活性炭与硝基发生了化学反应
22.(8分)(有机化学基础)工业上以石油裂解得到的乙烯和1,3-丁二烯为原料,通过下列反应合成高分子化合物H,该物质可用于制造以玻璃纤维为填料的增强塑料(俗称玻璃纲)。
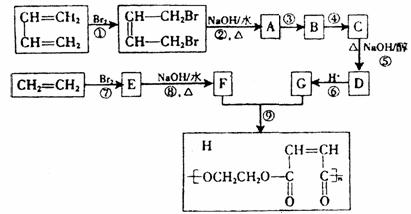
请按要求填空:
(1)写出下列反应的反应类型:① 反应,⑧ 反应。
(2)反应③④中某一步反应是与HCl的加成反应,该反应是 (填反应序号);设计该步反应的目的是
(3)物质D的结构简式是
(4)反应⑨的化学方程式是
21.(9分)水的电离平衡曲线如图所示:
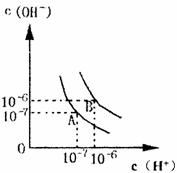
(1)若以A点表示25℃水在电离平衡时的离子浓度,当温度上升到100℃时,水的电离平衡状态到B点,则此时水的离子积从 增加到 ,造成水的离子积增大的原因是 ___________________ 。
(2)已知:25℃时,0.1mol/L的H2R溶液的0.7<pH<1(已知1g2=0.3),则H2R在水溶液中的电离方程式为
(3)100℃时,将pH=9的NaOH溶液与pH=4的硫酸溶液混合,若所得溶液pH=7,则NaOH溶液与硫酸溶液的体积比为 。
(4)100℃时,若10体积的某强酸溶液与1体积的某强碱溶液混合后溶液呈中性,则混合之前强酸溶液的pH与强碱溶液的pH之间应满足的关系是 _________________________________ 。
20.请按要求回答问题:(15分)
Ⅰ.(8分)短周期主族元素A、B、C、D的原子序数依次增大,其中A、C同主族,B、C、D同周期,A原子的最外层电子数是次外层电子数的3倍,B是短周期元素中原子半径最大的主族元素。试回答下列问题:
(1)A的元素符号 ;D的原子结构示意图 。
(2)A、B、C三种元素形成的简单离子的半径由大到小的顺序是 。
(3)CA2与D元素的单质在水溶液中反应的化学方程式是 。
Ⅱ.(4分)在25℃时,用石墨电极电解100mL 1mol·L-1 AgNO3溶液,如有0.2mol电子发生转移,试回答下列问题:
(1)阴极上发生的电极反应为 ;
(2)电解产生的气体的总体积(标准状况)为 。
Ⅲ.(3分)已知298K时下列反应:
Ca(s)+C(s)+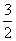 O2(g)=CaCO3(s);△H=-1206.8kJ·mol-1 ①
O2(g)=CaCO3(s);△H=-1206.8kJ·mol-1 ①
Ca(s)+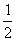 O2(g)=CaO(s);△H=-635.1kJ·mol-1 ②
O2(g)=CaO(s);△H=-635.1kJ·mol-1 ②
Ca(s)=CaO(s)+CO2(g);△H=+178.2kJ·mol-1 ③
则该温度下12g C完全燃烧的热化学方程式为_____ 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com