
1.各地环保部门在“科学发展观”的指导下,合理利用城市生活垃圾,实施了生活垃圾分类投放。其中塑料袋、废纸、旧橡胶制品等属于 ( )
A.无机物 B.有机物
C.盐类 D.非金属单质
27.(6分)现有一种碱金属的碳酸正盐和另一种碱金属的酸式碳酸盐组成的混合物试样0.506g,加热至质量不再变化为止,将生成的气体用足量的澄清石灰水吸收,得到白色沉淀0.200g。将加热后残留的固体与足量稀硫酸充分反应,生成的气体充分干燥后通过足量的过氧化钠粉末,过氧化钠粉末的质量增加0.084g。试回答:
(1)混合物中酸式碳酸盐物质的量为 mol。
(2)加热后残留固体中两碳酸盐物质的量之和为 mol。
(3)通过计算和推理确定混合物中两种盐的化学式分别为 。
26.(4分)在一定温度下有甲、乙两容积相等的容器。
(1)向甲容器中通入3molN2和4molH2,反应达到平衡时,生成NH3a mol。此时,NH3的物质的量分数是 。若在达到平衡状态的甲容器中通入少量的N2,则达到新平衡时,体系中N2的体积分数将 (选填“增大”“减小”或“不变”)。
(2)向乙中通入2molNH3,欲使反应达到平衡时,各物质的浓度与(1)中第一次平衡相同,则起始时还需通入 molN2和 molH2。
25.(12分)下图为某实验者设计的验证银元完全溶解于一定量的浓硝酸后生成NO2气体中含有NO的实验装置图。常温时,NO2与N2O4同时存在;在低于0℃时,几乎只有无色的N2O4晶体存在。

(1)反应前先打开A中的活塞K1,持续通一段时间N2,其理由是 。
(2)若装置中缺B,其后果是 。
(3)反应结束后,打开D中的活塞K2,并通入氧气,D瓶气内气体由无色变为红棕色,反应的化学方程式为 ;若通入的是热氧气,则瓶内气体的颜色比以前更深,其原因是 。(用方程式和必要的文说明)
(4)C装置的作用是 ;
E中a仪器所起的作用是 。
(5)为测定该银元中银的质量分数,还需进行的主要实验操作是:将A中溶液倒入烧杯中,然后加入过量的NaCl溶液,随后进行的操作为 (用ABCD字母排序),最后测定溶液中Ag+的质量。
A.洗涤 B.过滤 C.称量 D.烘干
24.(12分)已知A为酸式盐,B为某二价主族金属元素的化合物,C、D、F、G、I在常温常压下均呈气态,且D燃烧时产生的氧炔焰常用来焊接或切割金属。等物质的量A、B与少量的水充分混合能恰好完全反应。图中反应条件(除高温外)均已略去。

(1)写出B的电子式 ,D的结构简式 。
(2)写出A与B反应的化学方程式 。
(3)将I气体通入溶有饱和C气体的NaCl溶液,是侯氏制碱法的一步关键反应,该反应的化学方程式为 。
(4)写出下列反应的离子方程式:
①在A溶液中加入M 。
②向A溶液中加入过量NaOH溶液,并加热 。
③已知Fe3O4能溶于M溶液并产生F气体,该离子反应式为: 。
23.(6分)有机物A为食品包装纸的常用防腐剂。A难溶于水,但在酸性条件下会水解,且1molA水解得到1molB(C4H4O4)和2mol甲醇。通常状况下,B为无色晶体,可使溴水褪色,且能与氢氧化钠溶液反应。
(1)B分子所含的官能团的名称是 、 。
(2)已知B是无支链的直链分子,下列关于B分子空间结构的说法正确的是 。
①所有原子可能在同一平面 ②所有的碳原子在同一直线上
③所有碳原子在同一平面上 ④所有的原子在同一直线上
(3)A在酸性条件下水解的化学方程式 。
22.(7分)已知pH=2的H3IO5(高碘酸)溶液与pH=12的NaOH溶液等体积混合,所得混合溶液呈酸性,0.01mol/L的HIO3(碘酸)或HMnO4(高锰酸)溶液与pH=12的NaOH溶液等体积混合,所得混合溶液均呈中性,请回答下列问题:
(1)高碘酸是 (填写“强酸”或“弱酸”),原因是 。
(2)已知高碘酸和硫酸锰在溶液中反应生成高锰酸、碘酸及硫酸,此反应的氧化剂是 ,反应的离子方程式为 。
21.(3分)下列实验操作或实验所得出的结论一定正确的是 (填代号)。
A.用98%的浓硫酸配制100g10%的稀硫酸溶液时,除使用量筒外还需用到容量瓶
B.用渗析法分离淀粉中混有的NaNO3杂质
C.无法用分液漏斗将乙二醇和水的混合液体分离
D.某无色溶液中加入盐酸产生无色无味气体,则溶液中一定含CO2-3离子
E.SO2、乙烯、乙炔通入溴水都能被氧化而使溴水褪色
F.用碱式滴定管量取20.00mL 0.1000mol/L的KMnO4溶液
H.在中学“硫酸铜晶体里结晶水含量测定”的实验中,称量操作至少需要四次
20.某有机物A是农药生产中的一种中间体,其结构简式如下。下列叙述正确的是( )
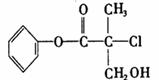
A.有机物A属于芳香烃
B.有机物A可以和Br2的CCl4溶液发生加成反应
C.有机物A和浓硫酸混合加热,可以发生消去反应
D.1molA和足量的NaOH溶液反应,最多可以消耗3mol NaOH
第Ⅱ卷(非选择题50分)
|
19.某K2CO3样品中含有Na2CO3、KNO3和Ba(NO3)2三种杂质中的一种或两种,现将13.8g样品加入足量水中,样品全部溶解,再加入过量的CaCl2溶液,得到9g沉淀。下列对样品所含杂质的正确判断是 ( )
A.肯定没有KNO3
B.肯定有KNO3,可能还有Na2CO3
C.肯定没有Ba(NO3)2,可能有KNO3
D.肯定没有Na2CO3和Ba(NO3)2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com