
18.A、B、C、D、E五种短周期元素中,A、B、C位于同一周期相邻位置,A和C原子的最外层电子数比为2:3,A、B、C能分别与D形成含有18个电子的分子,E的原子结构中从内到外各电子层的电子数之比为1:4:1。下列叙述中,正确的是 ( )
A.A、B、C分别与D形成的化合物的热稳定性依次减弱
B.由A、B、C原子和D原子构成的分子都是极性分子
C.C的最高价氧化物对应的水化物是强酸
D.E的单质在冷的浓硫酸中会发生纯化现象
17.下图中每条折线表示周期表IVA~VIIA中的某一族元素氢化物的沸点变化,每个小黑点代表一种氢化物,其中a点代表的是 ( )
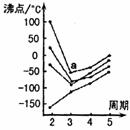
A.NH3 B.H2S C.SiH4 D.HF
16.(NH4)2SO4在一定条件下能够发生如下反应:
4(NH4)2SO 4N2↑+6NH3↑+3SO2↑+SO3↑+7H2O。将反应后的混合气体通入BaCl2溶液,产生的沉淀为 ( )
4N2↑+6NH3↑+3SO2↑+SO3↑+7H2O。将反应后的混合气体通入BaCl2溶液,产生的沉淀为 ( )
A.只有BaSO4 B.只有BaSO3 C.BaS D.BaSO4和BaSO3
15.将NaHCO3溶液分别加入到下列溶液中,不会产生沉淀的是 ( )
A.Ca(OH)2 B.Al2(SO4)3 C.NaAlO2 D.CaCl2
14.下列反应的离子方程式正确的是 ( )
A.氯化铝溶液中加入过量氨水:Al3++4NH3·H2O=AlO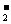 +4NH
+4NH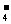 +2 H2O
+2 H2O
B.二氧化硅与氢氧化钠溶液反应:SiO2+2OH-=SiO + H2O
+ H2O
C.氯气与水反应:Cl2+ H2O=2H++Cl-+ClO-
D.向溴化亚铁溶液中通入少量氯气:Cl2+2Br-=2Cl-+Br2
13.下列有关实验的叙述,正确的是 ( )
A.浓硝酸可保存在带橡皮塞的棕色细口瓶中
B.用pH试纸测定溶液的pH时,pH试纸应事先润湿
C.配制一定物质的量浓度的溶液时,选用的容量瓶规格由需配制溶液的体积决定
D.用分液漏斗将乙醇和水的混合液体分离
12.短周期元素M和N的离子M2+和N2-具有相同的电子层结构,则下列说法正确的是( )
A.M2+的离子半径比N2-小 B.M的原子序数比N小
C.M和N原子的电子层数相等 D.M和N原子最外层电子数相等
11.下列关于元素周期表和元素周期律的说法不正确的是 ( )
A.从氟到碘,生成的氢化物熔、沸点逐渐升高,稳定性逐渐减弱
B.因为钠原子比铝原子容易失去电子,所以钠比铝的还原性强
C.从钠到氯,最高价氧化物的水化物碱性逐渐减弱,酸性逐渐增强
D.氧与硫为同主族元素,氧比硫的原子半径小,氧比硫的非金属性强
9.下列说法中正确的是 ( )
A.原子晶体中只存在非极性共价键
B. Fe与
Fe与 Fe互为同位素
Fe互为同位素
C.干冰升华时,分子内共价键会发生断裂
D.金属元素和非金属元素形成的化合物一定是离子化合物
|
A.6 B.8 C.11 D.16
8.25℃、101kPa下,碳、氢气、甲烷和葡萄糖的燃烧热依次是393.5kJ/mol、285.5kJ/mol、890.3kJ/mol、2800kJ/mol。下列热化学方程式中,正确的是 ( )
A.C(s)+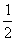 O2=CO(g);△H=-393.5kJ/mol
O2=CO(g);△H=-393.5kJ/mol
B.2H2(g)+O2(g)=2H2O(l);△H=+571.6kJ/mol
C.CH4(g)+2O2(g)=CO2(g)+2H2O(g);△H=-890.3kJ/mol
D.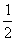 C6H12O6(s)+3O2(g)=3CO2(g)+3H2O(l);△H=-1400kJ/mol
C6H12O6(s)+3O2(g)=3CO2(g)+3H2O(l);△H=-1400kJ/mol
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com