
13.在一定温度下体积恒定的密闭容器中,充入2mol/LA和1mol/LB发生如下反应:
2A(g)+B(g)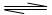 xC(g),达到平衡后C的体积分数为a%;若在相同条件下,x分别为2或3时,均按起始物质的量为0.6molA、0.3molB、1.4molC充入容器中,分别达到平衡状态,两平衡状态中C的体积分数为 ` ( )
xC(g),达到平衡后C的体积分数为a%;若在相同条件下,x分别为2或3时,均按起始物质的量为0.6molA、0.3molB、1.4molC充入容器中,分别达到平衡状态,两平衡状态中C的体积分数为 ` ( )
A.两者都小于a% B.两者都大于a%
C.两者都等于a% D.无法确定
第Ⅱ卷(本卷共10题,共174分)
12.在由水电离产生的c(H+)=1×10-12mol/L的溶液中,一定能大量共存的离子组是( )
A.Mg2+、NO3-、Cl-、Na+ B.K+、Cl-、NO3-、SO42-
C.Na+、Cl-、SO42-、HCO3- D.Fe2+、NO3-、I-、SO42-
11.下列说法正确的是 ( )
A.0.1mol/L的氨水和0.1mol/L的盐酸等体积混合,充分反应后所得溶液中:
c(Cl-)>c(NH4+)>c(OH-)>c(H+)
B.0.1mol/L的醋酸溶液中:c(H+)=c(CH3COO-)
C.0.1mol/L的硫化钠溶液中:c(Na+)=2c(S2-)+c(HS-)+c(H2S)
D.将氨气通入一定量硫酸溶液中,充分反应后溶液pH=7则:c(NH4+)>c(SO42-)
9.下列各组物质在适宜的条件下反应,其中氧化剂与还原剂的物质的量之比为2:1的是
( )
A.H2SO4(浓)+C B.Fe2O3+Al
C.Cl2+Mg D.NO2+H2O
|
①C17H35COOH ②C17H33COOH ③C15H31COOH ④C17H31COOH
⑤C17H29COOH
A.②④⑤ B.③②④ C.②③④ D.①⑤③
8.下列有关电化学知识的描述中正确的是 ( )
A.原电池的正极和电解池的阳极均发生氧化反应
B.铜的电解精炼时,粗铜板作阳极
C.铜、锌和稀硫酸构成的原电池中铜为负极
D.石墨作电极电解氯化镁溶液的离子方程式为2Cl-+2H2O 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑
7.设NA为阿伏加德罗常数,则下列说法不正确的是 ( )
A.32g氧气和臭氧的混合气体中含氧原子数为2NA
B.pH=2、体积为1L的醋酸溶液中含醋酸分子的数目为0.01NA
C.2.3g钠在足量氧气中完全燃烧转移电子数为0.1NA
D.标准状况下,11.2L“电石气”含有的分子数为0.5NA
6.下列说法正确的是 ( )
A.目前已被使用的高性能通信材料光导纤维的主要原料是硅
B.在医疗上,碳酸钠是治疗胃酸过多症的一种药剂
C.从电影业、照相业、科研单位和医院X光室回收的定影液中可以提取银
D.空气中的二氧化碳是造成光化学烟雾的主要因素
33.(8分)[化学-有机化学]
有机物A→F均为链状结构,它们之间的转化关系如下图所示:
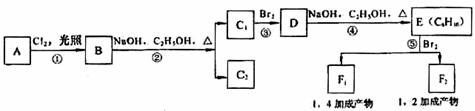
其中B为饱和化合物A的一氯取代产物,反应②只得到C1、C2两种互为同分异构体的有机物,核磁共振谱图表明E分子中只有两种类型的氢。
(1)有机物B的结构简式为 ,根据系统命名法C2的名称为 ;
(2)反应②和③的反应类型为 和 反应,写出由D生成E的化学方程式 ;
(3)化合物E是重要的工业原料,写出E发生加聚反应的化学方程式
。
32.(8分)[化学-物质结构与性质]
请完成下列各题:
(1)已知结构为正四面体型的离子A和直线型离子B反应,生成三角锥形分子C和V形分子D(组成A、B、C、D微粒的元素原子序数均小于10)。回答下列问题:
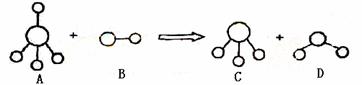
①在A、B、C、D所含的原子中未成对电子数最多的原子的电子排布式为 。
②C分子是 (“极性”或“非极性)分子,D分子的晶体的熔沸点明显高于同主族的组成相似的分子晶体的熔沸点的原因是 。
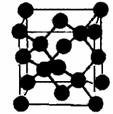
(2)晶体硅、碳化硅、金刚石三晶体的熔点由高到低的顺序是 。下图为金刚石晶胞结构示意图,若将此晶胞中的所有C原子换成Si原子,同时在每两个距离最近的相邻Si原子中心联线的中点处增添一个O原子,则构成SiO2晶胞,故SiO2晶胞中_____个Si原子, 个O原子,离O原子最近的Si原子有 个,离Si原子最近的O原子有 个。
31.(8分)[化学-化学与技术]
海水中含有丰富的化学元素,下面是某化工厂从海水中提取NaCl、Mg(以MgCl2形式存在)和Br2(以NaBr的形式存在)及综合利用的生产流程简图:
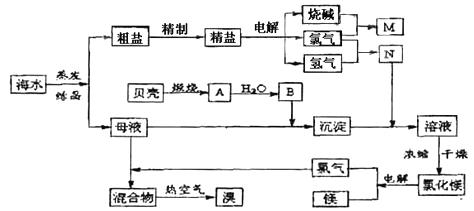
请回答:
(1)Mg(OH)2中加入盐酸中,要获得MgCl2·6H2O晶体,需要进行的实验操作依次为
;
(2)目前工业上主要采用离子交换膜法电解饱和食盐水,下列关于离子交换膜电解槽的叙述错误的是 ;
A.精制饱和食盐水进入阳极室 B.纯水(加少量NaOH)进入阴极室
C.阴极产物为氢氧化钠和氢气 D.电解槽的阳极用金属铁网制成
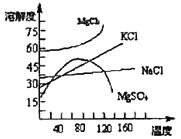
(3)母液中常含有MgCl2、NaCl、MgSO4、KCl等,可进一步加工制得一些重要的产品。若将母液加热升温到60℃以上,随着水分的蒸发,会逐渐析出晶体,此晶体的主要成分是 ;过滤上述晶体后,将滤液降温到30℃以下,又逐渐析出晶体,用一定量的冷水洗涤该晶体,最后可得到比较纯净的 晶体。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com