
28.(18分)某芳香烃A有如下六步转化:
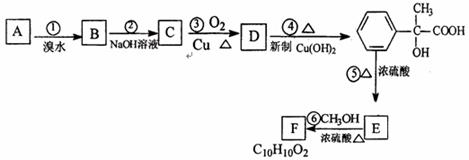
(1)写出反应类型:② ⑤
(2)写出结构简式A ,D
(3)写出E所含的官能团
(4)写出反应②和⑥的化学方程式
②
⑥
(5)有机物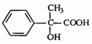 的同分异构体有多种,写出同时满足:
的同分异构体有多种,写出同时满足:
①遇FeCl3溶液显紫色,②苯环上的一氯取代物中只有两种,③属于酯类三个要求的同分异构体的结构简式三种
27.(15分)A、B、C是中学化学常见的三种短周期元素,已知①A元素原子最外层电子数是次外层电子数的2倍;②B元素最高正价与负价的代数和为2;③C元素有多种化合价,且常温下C元素的单质与某种一元碱溶液反应,可得两种含C元素的化合物;④B、C两种元素质子数之和是A元素质子数的4倍。
(1)写出A、B、C三种元素的名称A B C
(2)写出B的最高价氧化物的水化物与A的单质反应的化学方程式:
(3)由B、C两种元素组成的化合物X,常温下为易挥发的淡黄色液体,X分子为三角锥形分子,且分子里B、C两种原子最外层均达到8个电子的稳定结构。X遇水蒸气可生成一种常见的漂白性物质;则X的分子式为 ,分子中B、C原子间的化学键类型为 (填“极性键”或“非极性键”); X与水反应的化学方程式为
(4)A、B两元素可形成一种硬度比金刚石还大的化合物Y,化合物Y中,A、B两原子以单键相结合,且每个原子最外层均达到8个电子的稳定结构,则Y的化学式为 ,Y的硬度比金刚石硬度大的原因是:
26.(10分)以海水中常见物质A为原料可以发展很多种工业,下图中包含了中学课本中介绍的几种基本工业生产,请根据各物质之间的转化关系回答下列问题:

(1)C和D、C和G反应都可以制取消毒剂。C和G反应制取的消毒剂中有效成分的化学式为______________________。
(2)电解A溶液反应的离子方程式为_______________________________
(3)将F和J通入A的饱和溶液中,反应的化学方程式为:
_____________________________________________________________________
(4)图中所示工业制法获得的纯碱中常含有NaCl杂质,用下述方法可以测定样品中NaCl的质量分数。
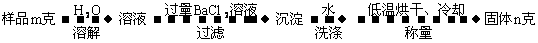
①检验沉淀是否洗涤干净的方法是_________________________________
②样品中NaCl的质量分数的数学表达式为__________________________
13.某有机物A是农药生产中的一种中间体,其结构简式如下,下列叙述正确的是 ( )
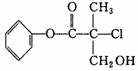
A.有机物A属于芳香烃
B.有机物A可以和Br2的CCl4溶液发生加成反应
C.有机物A和浓硫酸混合加热,可以发生消去反应
D.1molA和足量的NaOH溶液反应,最多可以消耗3molNaOH
|
12.
|
A.往NaOH溶液中滴加少量AlCl3溶液 Al3+ + 3OH- == Al(OH)3↓
B.石灰石和盐酸溶液反应 CO3 2- + 2H+ === CO2↑+ H2O
C.向氯化亚铁溶液中通入氯气 Fe2+ + Cl2 == Fe3+ + 2Cl-
D.向Ba(OH)2 溶液中逐滴加入NaHCO3溶液至Ba2+刚好沉淀完全:
Ba2++OH-+HCO3-=BaCO3↓+H2O
11.设NA为阿伏加德罗常数值,下列说法正确的是 ( )
A.7.8gNa2O2与足量的CO2反应,转移的电子数为0.2NA
B.常温常压时,36g重氧(18O2)气体所含分子数为NA
C.17g羟基中含有的电子数为10NA
D.标准状况下,22.4L苯所含的分子数约为NA
9.下列各组比较中,前者比后者大的是( )
A.25℃,pH均为2的盐酸和CH3COOH溶液中溶质的物质的量浓度
B.将pH=4的盐酸和醋酸分别稀释成pH=5的溶液,所加水的量
C.同温、同浓度的NaCl溶液和氨水的导电能力
D.25℃时,pH均为3的HCl和FeCl3溶液中水的电离程度
|
A.铂做阳极、铜做阴极,电解硫酸铜溶液
B.石墨做阳极和阴极,电解硫酸
C.铜做阳极、铁做阴极,电解氯化铜溶液
D.铜做阳极、铜做阴极,电解硫酸铜溶液
8.在容积不变的密闭容器中,一定条件下进行如下反应:
NO(g) + CO(g)  N2(g) + CO2(g);△H=-373.2kJ/mol。下图曲线a表示该反应过程中,NO的转化率与反应时间的关系。若改变起始条件,使反应过程按照曲线b进行,可采取的措施是 ( )
N2(g) + CO2(g);△H=-373.2kJ/mol。下图曲线a表示该反应过程中,NO的转化率与反应时间的关系。若改变起始条件,使反应过程按照曲线b进行,可采取的措施是 ( )

A.加催化剂 B.向密闭容器中通入氩气
C.降低温度 D.增大反应物中NO的浓度
7.下列说法不正确的是 ( ) A.NaOH、SO2、CH2=CH2 都能使溴水褪色,但原理各不相同
B.活性炭、氯气和二氧化硫都能使品红溶液褪色,且原理相同
C.Al、NaHCO3、CH3COONH4既能跟盐酸反应,又能跟烧碱溶液反应
D.C6H5OH、FeSO4溶液、Na2SO3溶液在空气中都易因氧化而变质
6.据报道,月球上有大量3He存在。以下关于3He的说法正确的是 ( )
A.是4He的同分异构体 B.比4He多一个中子
C.是4He的同位素 D.比4He少一个质子
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com