
3.下列各组物质中,互为同系物的是 ( )
A.
B.
C.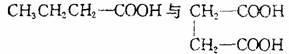
D.
2.在下列实验中,不能达到目的的是 ( )
A.用金属钠分别与水和乙醇反应,确定水和乙醇分子中羟基氢的活泼性强弱
B.用石墨作电极,电解Mg(NO3)2、Cu(NO3)2的混合溶液,确定铜和镁的金属活动性强弱
C.对H2O、H2S进行热分解实验,确定硫和氧的非金属性强弱
D.为确定溴乙烷中含有溴元素,向该溴乙烷中加入NaOH水溶液后,再加入AgNO3
溶液
1.下列说法错误的是 ( )
A.两种互为同分异构体的化合物一定不是同系物
B.两种含碳元素质量分数相同的烃不一定互为同分异构体
C.两种分子的组成相差若干个CH3原子团的有机物不一定是同系物
D.氟利昂-12(分子式为CCl2F2)有两种同分异构体
25.(12分)下列物质均为中学化学常见的物质,其转化关系如图所示,反应条件及部分产物未全部标出。已知A为正盐,试剂①和试剂②为中学化学实验室常用的试剂,其中B、C、D、E、G常温下为气体,H常温下为液体。
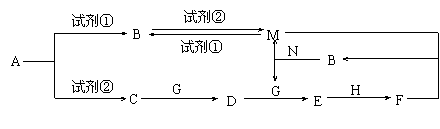

(1)A的化学式为 。
(2)N的电子式为 ,所含化学键为 。
(3)A→C的离子方程式为 。
(4)C→D的化学方程式为 。
(5)已知标准状况下有33.6L的C与G完全反应生成D,则转移的电子数为 NA。
24.(10分)有机黏合剂是生产和生活中一类重要的材料。黏合过程一般是液态的小分子黏合剂经化学反应转化成为大分子或高分子而固化。
(1)“502胶”是一种快干胶,其主要成分是α-氰基丙烯酸乙酯,其结构简式为:
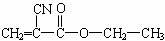 它在空气中微量水催化下发生加聚反应,迅速固化而将被黏物粘牢。请写出“502胶”发生黏合过程的化学方程式:
它在空气中微量水催化下发生加聚反应,迅速固化而将被黏物粘牢。请写出“502胶”发生黏合过程的化学方程式:
。
(2)厌氧胶也是一种黏合剂,其结简式为:


它在空气中稳定,但在隔绝空气(缺氧)时分子中双键断开发生聚合而固化。工业上用丙烯酸(CH2=CH-COOH)和某种物质在一定条件下反应可制得这种黏合剂。请写出这一制取过程的化学方程式:
(3)乳白胶是一种常见黏合剂,其主要成分为醋酸乙烯酯(CH3COOCH=CH2),其中同时含有“-CHO”和“-CH=CH-”结构的同分异构体有多种,如:
 “CH3-CH=CH-O-CHO”和“CH2=CH-CH2-O-CHO”,请再写出三种能稳定存在的同分异构体的结构简式(已知含有-C=C-OH的结构不能稳定存在)
,
,
。
“CH3-CH=CH-O-CHO”和“CH2=CH-CH2-O-CHO”,请再写出三种能稳定存在的同分异构体的结构简式(已知含有-C=C-OH的结构不能稳定存在)
,
,
。
23.(12分)现有aA、bB、cC、dD、eE五种短周期元素,它们都是生命中不可缺少的重要元素。已知它们的原子序数有如下关系:a+b=c,a+c=d,c+d=e,B、D、E都有多种同素异形体,B的化合物的种类与A的化合物的种类何者最多尚有争议。据此,回答下列有关问题:
(1)写出下列元素的元素符号:B ,D ;写出E的常见两种同素异形体的名称 ;C、E的氢化物的沸点高低关系是 (用分子式和“>”表示)。
(2)X是C的最高价氧化物的水化物,它是重要的化学试剂,其浓溶液需避光保存,这是因为(用化学方程式表示) 。
(3)Y是C的最高价氧化物的水化物和其氢化物反应生成的化合物,常温时,PH= a的X、Y两种溶液中由水电离出来的H+浓度之比为 。
(4)X与A、B组成的某化合物在一定条件下反应制得一种常见的烈性炸药,其反应的化学方程式为 。
(5)由上述元素组成的某化合物其化学式为B8C8D16 ,其分子中B元素原子之间以非极性键结合,非极性键之间的夹角都为90°;同种元素的原子在结构中毫无区别。则此化合物的结构简式为 。
22.(10分)莫尔是一位著名分析化学家,以他命名的莫尔盐[ (NH4)2Fe(SO4)2·6H2O]是化学分析中重要的试剂,常作为一种稳定的还原剂使用。某同学模拟制备莫尔盐并利用莫尔盐测定高锰酸钾溶液的浓度。他的实验过程如下:
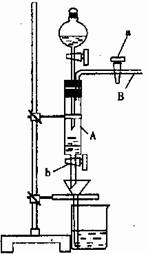
A中放有2g废铁屑(含铁锈,其他杂质不与稀硫酸反应),烧杯中盛有饱和硫酸铵溶液,实验时打开a,关闭b,从分液漏斗内向A中加一定量的稀硫酸,此时溶液呈浅绿色,再打开b进行过滤,过滤结束后取烧杯内溶液倒入蒸发皿中加热,蒸发掉部分水,再降温结晶获得莫尔盐晶体。然后用莫尔盐测定未知高锰酸钾溶液的浓度。
试回答下列问题:
(1)请写出在蒸发皿中制得莫尔盐的化学方程式是
。
(2)滴加稀H2SO4时,发现其反应速率比同浓度硫酸与纯铁粉反应快,其原因是 。
(3)取3.92g莫尔盐晶体配成100mL溶液,用酸式滴定管取20.00mL注入锥形瓶中,然后用未知浓度的酸性高锰酸钾溶液进行滴定,消耗该溶液的体积为8.00mL。
①配平下列反应式:
Fe2++ MnO4-+ H+ - Mn2++ Fe3++ H2O
②用 (酸式或碱式)滴定管盛装高锰酸钾溶液
③高锰酸钾溶液的物质的量浓度是 。
21.(6分)A、B、C、D、E均为可溶于水的固体,组成它们的离子可能有:Na+、Mg2+、Ba2+、ClO-、HSO4-、CO32-、Cl-。分别取它们的溶液进行实验,主要操作及现象如下:
①向A的溶液中通入二氧化碳,再加入品红溶液,红色褪去。
②A、B、E的溶液的焰色反应都呈黄色
③将B和C的溶液混合,生成白色沉淀,该沉淀可溶于E溶液
④将B和D的溶液混合,生成白色沉淀,继续加入过量的E溶液,有气泡产生的同时还有白色沉淀存在。
(1)写出下列物质的化学式:A ,C 。
(2)向B的溶液中,缓慢滴入少量的E溶液,其主要的离子方程式为:
。
20.尼泊金甲酯 ( ) 是苯的含氧衍生物,在化妆品中可作防腐剂。其同分异构体A满足如下条件:①含有苯环,②含有碳碳双键,③苯环上一氯代物只有一种;其同分异构体B,能发生银镜反应,也能与NaOH溶液反应生成C8H7O3Na。下列推论合理的是 ( )
) 是苯的含氧衍生物,在化妆品中可作防腐剂。其同分异构体A满足如下条件:①含有苯环,②含有碳碳双键,③苯环上一氯代物只有一种;其同分异构体B,能发生银镜反应,也能与NaOH溶液反应生成C8H7O3Na。下列推论合理的是 ( )
A.1mol尼泊金甲酯最多与含有1mol NaOH的溶液反应生成对应的钠盐
B.符合题述条件的有机物A的同分异构体有2种
C.有机物B一定不能发生酯化反应
D.符合条件的有机物A只能与溴水发生加成反应
|
19.美丽的 “水立方”是北京奥运会游泳馆,设计灵感来自于有机细胞的天然图案以及肥皂泡的形成。在这个中心的蓝色泡墙之内,钢结构的基本单位是一个由12个正五边形和2个正六边形组成的几何细胞,覆盖这个框架的是半透明的“气泡”,称为ETFE,该材料为四氟乙烯(CF2=CF2)与乙烯的共聚物,它能为场馆内带来更多的自然光。根据以上信息,下列说法不正确的是 ( )
A.若设想将一个结构单元用钢棍焊成足球形状“碳笼”,它与C24形状相似
B.若设想将一个结构单元用钢棍焊成足球形状“碳笼”,需钢棍(相当于键)36根
C.ETFE在空气中易被氧气氧化
D.四氟乙烯中既含有极性键又含有非极性键
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com