
7.某温度下,容积一定的密闭容器中进行如下可逆反应:X(g)+Y(g)=Z(g)+W(s);△H>0下列叙述正确的是 ( )
A.加入少量W,逆反应速率增大 B.当容器中气体压强不变时,反应达到平衡
C.升高温度,平衡逆向移动 D.平衡后加入X,上述反应的△H增大
6.许多国家十分重视海水资源的综合利用。不需要化学变化就能够从海水中获得的物质是
( )
A.氯,溴,碘 B.钠,镁,铝 C.烧碱,氢气 D.食盐,淡水
22.(8分)乙烷和乙烯混合气体共amol,与bmol的氧气共存于一密闭容器中,点燃充分反应后,乙烷、乙烯全部消耗完,得到CO、CO2混合气体和45g水,试求:
(1)当a=1时,乙烷与乙烯的物质的量之比n(C2H4):n(C2H4)= ;
(2)当a=1时,且反应后CO和CO2混合气体的物质的量为反应前O2的物质的量的2/3时,则b = ,生成的CO和CO2的物质的量之比为 ;
(3)a的取值范围 。
21.(16分)奶油中有一种只含C、H、O的化合物A。A可用作香料,其相对分子质量为88,分子中C、H、O原子个数比为2:4:1。
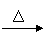 已知:①ROH +HBr(氢溴酸) RBr+H2O
已知:①ROH +HBr(氢溴酸) RBr+H2O
②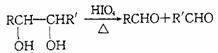
A中含有碳氧双键,与A相关的反应如下:
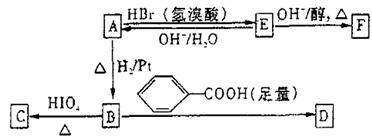
(1)A的分子式为 。
(2)写出与A分子式相同的所有酯的结构简式: 、 、
、 。
(3)写出A→E、E→F的反应类型:A→E 、E→F 。
(4)写出A、C的结构简式:A 、C 。
(5)写出E→F反应的化学方程式: 。
(6)在空气中长时间搅拌奶油,A可转化为相对分子质量为86的化合物G,G的一氯代物只有一种,写出G的结构简式 ,A→G的反应类型为 。
20.(10分)100mL某无色透明溶液中可能含有Fe3+、Ag+、Al3+、Ba2+、Mg2+、K+、Na+等阳离子。进行下述实验(所加试剂均过量)
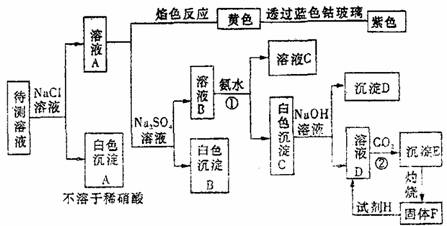
(1)根据上图推断:溶液中一定存在的阳离子有 ;
溶液中一定还存在阴离子,则其可能存在的一种阴离子是 ;
(2)反应①的离子方程式为 、 ;
(3)若实验中进行焰色反应、过滤等操作时对原溶液的损耗忽略不计,实验中只测得沉淀C和固体F的质量分别为mg和ng,据此能确定原溶液中 等离子的物质的量浓度。
19.(10分)实验室用电石与水反应制取的乙炔气体含有少量的H2S气体,为了净化和检验乙炔气体,并通过测定乙炔的体积计算电石的纯度,请按下列要求填空(已知X溶液为含有3.2%的溴的CCl4溶液的150g):
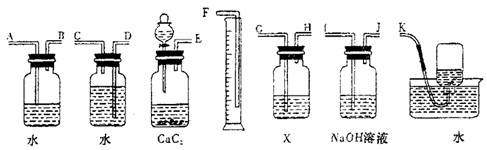
(1)试从上述装置中选择几种必要的装置,把它们连成一套完整的装置,这些被选用的装置的接口编号连接顺序是 ;
(2)为了获得比较平稳的乙炔气流,常用 代替水;
(3)净化乙炔反应的离子方程式为 ;
(4)假设溴的CCl4溶液与乙炔完全反应,生成C2H2Br4,用Wg电石与足量水反应后,测得量筒内排水的体积为VmL(标准状况下),则电石纯度计算式为 。
18.(10分)苯环上原有的取代基对再进入苯环的第二个取代基的位置有一定影响。如:苯环上已有-OH、-CH3(或烃基)、-Br时,新导入的取代基主要进入苯环上的邻位和对位;而当苯环上已有-NO2、-SO3H等取代基时,新导入的取代基主要进入苯环上的间位。现有下图的转化:
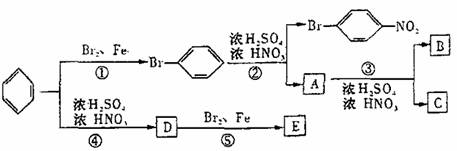
请按要求写出反应的化学方程式:
(1)反应①的化学方程式 ;
(2)由A变成B、C的化学方程式 ;
(3)反应④的化学方程式 ;
(4)反应⑤的化学方程式 。
17.(6分)有机物的结构可用“键线式”表示,
如:CH3-CH = CH-CH = CH2可表示 。有机物X的键线式为:
。有机物X的键线式为: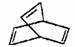
(1)有机物Y是X的同分异构体,且属于芳香烃,则Y的结构简式为
;
(2)Y与乙烯在一定条件下可发生聚合反应,写出其反应的化学方程式
;
(3)X与足量的H2在一定条件下反应可生成环状饱和烃Z,Z的一氯代物有 种。
16.若要使1mol的CH4完全与氯气发生取代反应,并生成相同物质的量的四种取代物,则需要氯气的物质的量为 ( )
A.1mol B.1.25mol C.2mol D.2.5mol
15.1mol某烃在氧气中充分燃烧,需要消耗氧气179.2L(标准状况下),它在光照的条件下与氯气反应能生成三种不同的一氯取代物。该烃的结构简式可能是 ( )
A.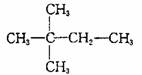 B.CH3CH2CH2CH2CH3
B.CH3CH2CH2CH2CH3
C.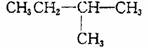 D.
D.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com