
27.(4分)KClO3和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯(ClO2),其反应的化学方程式为:2KClO3十4HCl(浓)=2KCl+2ClO2↑+Cl2↑+2H2O
(1)浓盐酸在反应中显示出来的性质是 (填序号);
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
(2)产生0.1mol Cl2,则转移电子的物质的量为 mol,被氧化的HCl的物质的量为 mol。
26.(10分)某同学要配制1.0mol·L-1的NaOH溶液,提供的仪器有①容量瓶(250mL) ②玻璃棒 ③托盘天平(配砝码和镊子) ④药匙 ⑤胶头滴管 ⑥量筒 ⑦烧杯 ⑧漏斗
请回答下列问题:
(1)上述仪器中配制溶液时所需的玻璃仪器有 (填序号);
(2)由题意可知,你应该称取固体NaOH g,如果由于称量的时间过长,你所配制NaOH溶液的浓度与要求相比 (填“偏大”、“偏小”或“相等”);
(3)在配制的整个过程中,如果使用玻璃棒,试说明其用途
;
(4)用上述浓度的NaOH溶液500mL,与1.0mol·L-1的硫酸恰好完全反应,则需硫酸的体积是 。
25.(5分)某研究性学习小组欲开展一次以化学为主体的活动,确定的课题是“研究浓硫酸与木炭粉在加热条件下反应的产物”。根据小组成员的推测,浓硫酸与木炭粉在加热条件下反应的产物可能有CO2、SO2,为了验证推测,小组讨论用以下装置进行实验:
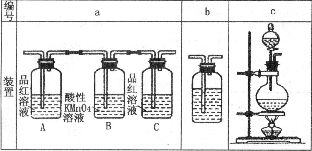
(1)实验时可观察到装置a中A瓶溶液退色,C瓶溶液不退色。则A瓶溶液的作用
,C瓶溶液的作用 ;
(2)装置b中所加的液体是 ,装置b可验证的产物是 ;
(3)甲、乙两位同学分别设计了两套不同的装置:
甲的装置顺序:c b a 乙的装置顺序:c a b
你认为合理的是(填“甲”或“乙”) 。
24.(7分)教材中对“铝热反应”的现象有这样的描述:“反应放出大量的热和耀眼的白光”,实验时还观察到纸漏斗的下部被烧穿,有熔融物落入沙中。又已知Al、Fe2O3 Al2O3、Fe的熔点、沸点数据如下:
|
物质 |
Al |
Fe2O3 |
Al2O3 |
Fe |
|
熔点/℃ |
660 |
1462 |
2054 |
1535 |
|
沸点/℃ |
2467 |
- |
2980 |
2750 |
(1)某同学推测,铝热反应所得到的熔融物应是铁铝合金。你通过上表数据分析此结论是否合理?答: (填“合理”或“不合理”);
(2)实验室欲溶解此熔融物,下列试剂中最好的是 (填字母标号);
A.浓硫酸 B.稀硫酸 C.稀硝酸 D.NaOH溶液
(3)设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝。填写下列表格.
|
所用试剂 |
|
|
实验操作及现象 |
|
|
有关反应的化学方程式 |
|
23.(8分)已知A是一种不溶于水的固体,在一定条件下有下列转化关系:

(1)写出物质的化学式:A ,E ;
(2)写出由B和C反应生成A,由F的浓溶液生成C的化学方程式:
B+C→A ,
F(浓)→C ;
(3)写出D和F的稀溶液反应的离子方程式 。
22.(6分)5.5gCO2在标准状况下的体积是 ,温度不变,压强变为202kPa,则体积变为 ;同温同压下,同体积的NH3和H2S气体的质量比是 ;同温同压下,同质量的NH3和H2S气体的体积比是 ;同质量的NH3和H2S气体中所含氢原子个数比是 ;若NH3和H2S所含氢原子个数相等,则它们的物质的量之比是 。
21.(4分)物质氰(CN)2、硫氰(SCN)2的性质与卤素单质相似,故称它们为类卤化合物。它们可以生成酸和盐(见下表,表中X代表F、Cl、Br或I)。
|
|
卤
素 |
氰 |
硫氰 |
① |
|
单质 |
X2 |
(CN)2 |
(SCN)2 |
(OCN)2 |
|
酸 |
HX |
HCN |
② |
HOCN |
|
盐 |
KX |
KCN |
KSCN |
③ |
请填写下列空白:
(1)在上表中①、②、③空格处应分别填写 、 、 ;
(2)(CN)2与水反应的化学方程式: 。
20.在通常条件下,NO2和SO2可以很容易发生反应生成NO和SO3。现将炭跟浓硫酸共热产生的气体X和炭跟浓硝酸共热产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图装置),下列有关说法正确的是
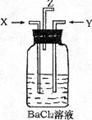
A.洗气瓶中产生的沉淀是碳酸钡
B.在Z导管出来的气体中无二氧化碳
C.洗气瓶中产生的沉淀是硫酸钡
D.反应一段时间后洗气瓶中溶液的酸性减弱
第Ⅱ卷(非选择题 共50分)
19.下列有关胶体的叙述中不正确的是
A.实验室可用丁达尔现象鉴别胶体与溶液
B.豆浆制豆腐是利用了胶体聚沉的原理
C.氢氧化铁胶体微粒带正电,通电时胶体微粒向直流电源正极移动
D.分散质微粒粒度介于1nm ~100nm之间的分散系称为胶体
18.氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性能,被广泛应用于电子工业、陶瓷工业等领域。在一定条件下,氮化铝可通过如下反应合成:
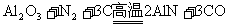
下列叙述中正确的是
A.在氮化铝的合成反应中,C是还原剂,N2是氧化剂
B.氮化铝中氮元素的化合价为-3
C.因为具有抗冲击、导热性好等优良性能.所以氮化铝属于金属材料
D.合成氮化铝的反应符合“绿色化学”的思想
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com