
31.(16分)X、Y、Z三种短周期元素,它们的原子序数之和为16。X、Y、Z三种元素常见单质在常温下都是无色气体,在适当条件下三种单质直接化合,可发生如下图所示变化:
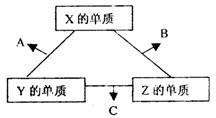
已知一个B分子中含有Z元素的原子个数比 C分子中的Z元素的原子个数少一个。
请回答下列问题:
(1)X的单质与Z的单质可制成新型的化学电源(KOH溶液作电解质溶液),两个电极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电。
则:正极通入的物质名称是 ;
负极电极反应式为 。
(2)X、Y、Z三种元素可组成一种强酸W,C在适当条件下被W溶液吸收生成一种盐。该盐的水溶液pH 7(填“大于”、“小于”或“等于”)其原因是(用离子方程式表示):
。
(3)已知Y的单质与Z的单质生成C的反应是可逆反应,△H<0。将等物质的量的Y、Z的单质充入一密闭容器中,在适当催化剂和恒温,恒压条件下反应。下列说法中,正确的是 。(填写下列各项的序号)
a. 达到化学平衡后,再升高温度,C的体积分数增大
b. 达到化学平衡时,Y、Z的两种单质在混合气体中的物质的量之比为1:1
c. 反应过程,Y的单质体积分数始终为50%
d. 达到化学平衡的过程中,混合气体平均相对分子质量减小
e. 达到化学平衡时,正反应速率与逆反应速率相等
(4)若在另外一个2L的容器中只发生物质A与单质X生成化合物M的反应,其中A、X、M的起始浓度次是0.2mo·L-1、0.1 mo·L-1、0.2 mo·L-1,当反应达到平衡时,各物质的浓度可能是 (选填字母代号)。
A.c(A)=0.35 mo·L-1或c(A)=0.09 mo·L-1
B.c(M)=0.4 mo·L-1
C.c(M)=0.35 mo·L-1
D.c(X)=0.2 mo·L-1或c(A)=0.4 mo·L-1
|
共8题,考生必须从中选择1个物理题、1个化学题和一个生物题在答题纸规定的区域作答。
30.(12分)已知下图所示各物质的转化关系中,某些反应部分产物已被省去。其中反应②用于常见金属I的冶炼,B为淡黄色固体,D、G、H均为气体且D、H无色。
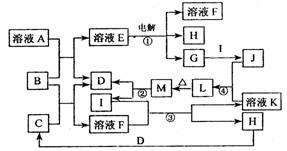
试回答下列问题:
(1)写出物质B的电子式 。
(2)写出反应①的离子方程式 ;
反应③的离子方程式 。
(3)由溶液J加热灼烧最终获得的物质是 (填化学式);由溶液K加热灼烧最终可获得的物质是 (填化学式)。
29.(14分)已知SiO2、SO2和CO2都是酸性氧化物,化学性质是具有一定的相似性;Mg和Na的化学性质也具有一定的相似性。
I.用如图所示装置进行Mg与SO2的反应的实验。
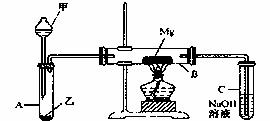
(1)选择制取SO2的合适试剂 (填写序号)。
①10%H2SO4溶液 ②80%H2SO4溶液 ③Na2SO3固体 ④CaSO3固体
(2)写出装置B中发生的主要反应的化学方程式 。
装置C中NaOH溶液的作用是 。
(3)指出C装置不足之处? 。
Ⅱ.某研究小组进行了“实验制Si”的研究,它们以课本为基础,查阅资料得到以下可供参考的信息:
①工业上在高温时用C还原SiO2可制得Si
②Mg在点燃的条件下即可与SiO2反应
③金属硅化物与稀H2SO4反应生成硫酸盐的SiH4
④Si和SiO2均不与稀H2SO4反应
⑤SiH4在空气中自然
他们在研究报告中记载着“……选用合适的物质在适宜的条件下充分反应;再用足量稀硫酸溶解固体产物;然后过滤、洗涤、干燥;最后称量……在用稀硫酸溶解固体产物时,发现有爆鸣声和火花,其产率也只有预期值的63%左右”。
(1)该小组“实验室制Si”的化学方程式是 。
(2)你估计“用稀硫酸溶解固体产物时,发现有爆鸣声和火花”的原因是:
。
3.第II卷所有题目的答案考生须用黑色或蓝色钢笔、圆珠笔答在答题纸规定位置上,在试题卷上答题无效。
15.下列关于电解质溶液的叙述正确的是 ( )
A.常温下,pH=7的NH4Cl与氨水的混合溶液中离子浓度大小顺序为:
c(Cl-)>c(NH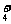 )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
B.将pH=4的醋酸溶液稀释后,溶液中所有离子的浓度均降低
C.中和pH与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量相同
D.常温下,同浓度的Na2S与NaHS溶液相比,Na2S溶液的pH大
|
14.将含有O2和CH4的混合气体置于盛有23.4g Na2O2的密闭容器中,电火花点燃,反应结束后,容器内的压强为零(150℃),将残留物溶于水中,无气体生成。下列叙述中正确的组合是 ( )
①混合气体中O2和CH4的体积比为2:1
②残留物只有Na2CO3
③混合气体中O2和CH4的物质的量之比为1:2
④残留物只有Na2CO3和NaOH
A.①② B.②③ C.③④ D.①④
13. CCTV“科技博览”报道,2004年3月中科院首创用CO2合成可降解塑料,聚二氧化碳
CCTV“科技博览”报道,2004年3月中科院首创用CO2合成可降解塑料,聚二氧化碳

 [ C-O ]n ,下列说法合理的是 ( )
[ C-O ]n ,下列说法合理的是 ( )
A.聚二氧化碳是通过加聚反应制得的 B.聚二氧化碳与干冰互为同素异形体
C.聚二氧化碳与干冰都是纯净物 D.聚二氧化碳的使用会产生白色污染
12.关于下列各装置图的叙述中,不正确的是 ( )
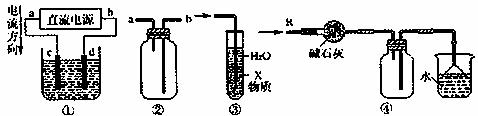
A.装置①中,d为阳极、c为阴极
B.装置②可用于收集H2、NH3、CO2、Cl2、HCl、NO2等气体
C.装置③中X若为四氯化碳,可用于吸收氨气或氯化氢,并防止倒吸
D.装置④可用于干燥、收集氨气,并吸收多余的氨气
11.下列热化学方程式中,能够表示物质燃烧热的是 ( )
A.C(s)+ O2(g)=CO(g);△H=-110.5kJ/mol
O2(g)=CO(g);△H=-110.5kJ/mol
B.H2(G)+Cl2(g)=2HCl(g);△H=-184.6kJ/mol
C.H2(g)+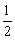 O2(g)= H2O(g);
O2(g)= H2O(g); H=-241.8kJ/mol
H=-241.8kJ/mol
D.C8H18(s)+ 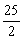 O2(g)= 8CO2(g)+ 9H2O(l);
O2(g)= 8CO2(g)+ 9H2O(l); H=-5518kJ/mol
H=-5518kJ/mol
10.判断下列有关化学基本概念的依据正确的是 ( )
A.强弱电解质:溶液的导电能力大小 B.共价化合物:是否含有共价键
C.氧化还原反应:是否有电子转移 D.胶体:分散质粒子能否透过半透膜
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com