
17.已知热化学反应方程式:
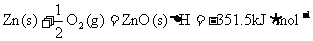
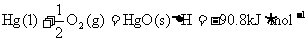
则锌汞电池中热化学反应方程式:Zn(s)+HgO(s)==ZnO(s)+Hg(1)的△H为
A.△H=+260.7kJ·mol B.△H= -260.7kJ·mol
B.△H= -260.7kJ·mol
C.△H= 一442.3kJ·mol D.△H=+442.3kJ·mol
D.△H=+442.3kJ·mol
16.常温时,将HA和HB两种一元酸溶液分别加水稀释,其pH变化如下图所示。下列叙述中正确的是
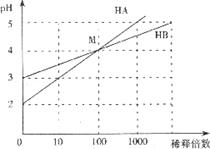
A.HA、HB都是弱酸 B.在M点,c(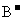 )=c(
)=c( )
)
C.稀释前,c(HA)=10c(HB) D.在M点,HA、HB酸的电离常数相同
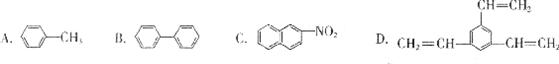
15.工业上将苯的蒸气通过赤热的铁能合成一种可作传热载体的化合物。该化合物分子中苯环上的一氯代物有3种。1mol该化合物催化加氢时最多消耗6molH2。这种化合物可能是
14.下列有关沉淀溶解平衡的说法正确的是
A.KSP(AB2)小于KSP(CD),则AB2的溶解度小于CD的溶解度
B.在氯化银的沉淀溶解平衡体系中,加入蒸馏水,氯化银的KSP增大
C.在氯化银的沉淀溶解平衡体系中,加入碘化钾固体,氯化银沉淀可转化为碘化银沉淀
D.在碳酸钙的沉淀溶解平衡体系中,加入稀盐酸,溶解平衡不移动
13.近年来,科学家研制了一种新型的乙醇电池,它用酸性电解质(H+)作溶剂。电池总反应为:C2H5OH+3O2==2CO2+3H2O,下列说法不正确的是
A.乙醇在电池的负极上参加反应
B.1mol CH3CH2OH被氧化转移6mol电子
C.在外电路中电子由负极沿导线流向正极
D.电池正极的电极反应为4H++O2+4e ==2H2O
==2H2O
12.设NA为阿伏加德罗常数的值,下列有关叙述正确的是
A.7gCnH2n中含氢原子数为NA
B.1.0 L 0.1 mol·L 氨水中,NH3·H2O的分子数为0.1NA
氨水中,NH3·H2O的分子数为0.1NA
C.在标准状况下,l L乙烯完全燃烧后,生成的气态产物的分子数为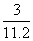 NA
NA
D.1mol甲基所含的电子数目为7NA
11.现有常温时pH=1的某强酸溶液10mL,下列能使溶液的pH变成2的操作是
A.加入10mL 0.01 mol·L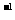 的NaOH溶液
的NaOH溶液
B.加入10mL的水进行稀释
C.加水稀释成100mL
D.加入100mL0.01mol·L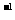 的HCl溶液
的HCl溶液
10.下列各项中的两个量,其比值一定为2:1的是
A.液面在“0”刻度时,50 mL滴定管和25 mL滴定管所盛溶液的体积
B.在反应2H2S+SO2=3S↓+2H2O中氧化产物与还原产物的质量
C.相同温度下,0.6 mol·L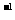 醋酸溶液与0.3 mol·L
醋酸溶液与0.3 mol·L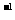 醋酸溶液中的c(H+)
醋酸溶液中的c(H+)
D.在Na2S溶液中,c(Na+)与c(S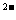 )
)
9.在pH=1的无色透明溶液中,能大量共存的离子组是
A.NH4+、Mg2+、SO4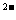 、Cl
、Cl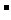 B.K+、OH
B.K+、OH 、NO3
、NO3 、Fe3+
、Fe3+
C.Al3+、Cu2+、SO4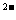 、Cl
、Cl D.Na+、Ca2+、Cl
D.Na+、Ca2+、Cl 、CO3
、CO3
8.将0.1mol下列物质置于1L水中充分搅拌后,溶液中阴离子数最多的是
A.KCl B.Mg(OH)2 C.Na2CO3 D.MgSO4
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com