
5.下列说法不正确的是
A.体系有序性越高,熵值就越低
B.知道了某过程有自发性之后可预测过程完成的快慢
C.吸热反应不一定不能自发进行
D.同种物质气态时熵值最大
4.下列关于实验操作的叙述中正确的是
A.从试剂瓶中取出的任何药品,若有剩余都不应再放回原试剂瓶中
B.用容量瓶配某盐溶液,定容摇匀后发现凹液面最低处低于刻度线,再加水定容
C.配制稀硫酸时可先在量筒中加入一定体积的水,再在搅拌条件下慢慢加入浓硫酸
D.萃取后,分液漏斗中的下层液体从下口流出,上层液体从上口倒出
3.已知下述三个实验均能发生化学反应
|
① |
② |
③ |
|
将铁钉放入硫酸铜溶液中 |
向硫酸亚铁溶液中滴人几滴浓硝酸 |
将铜丝放入氯化铁溶液中 |
下列判断正确的是
A.实验①中Cu2+做还原剂被氧化 B.实验②中Fe2+既显氧化性又显还原性
C.实验③中发生是置换反应 D.上述实验证明氧化性:Fe3+>Cu2+>Fe2+
2.生产和生活离不开各种化学物质,下列说法不正确的是
A.不需要通过化学反应就能从海水中获得食盐和淡水
B.潜水艇在紧急情况下可用过氧化钠供氧
C.氯气与烧碱溶液或石灰乳反应都能得到含氯消毒剂
D.工业上常用硅制造光导纤维
1.瑞典皇家科学院诺贝尔奖委员会将2007年度诺贝尔化学奖授予德国科学家格哈德·埃特尔,以表彰他在“固体表面化学过程”研究中作出的贡献。下列有关说法正确的是

A.臭氧空洞的形成与化石燃料大量使用有关
B.合成氨中N2和H2以物质的量之比3:1在催化剂表面进行
C.氢氧燃料电池的电极均作为反应物参加电极反应
D.汽车尾气中CO可在固体催化剂表面转为参与大气生态环境循环的CO2
31.在化工生产中,硝酸的制备通常采用催化氧化法,原料主要是氨气和氧气。
问题1:由于二氧化碳不能被水完全吸收,因此生成的气体须经过多次氧化、吸收的循环操作,使其充分转化为硝酸(如果不考虑生产过程中的其它损失)。
(1)从理论上分析,要使氨气完全转化为硝酸,则原料氨气和氧气物质的量的投料比至少为 。
(2)如果按理论上的原料将原料放在一个具有反应条件下的密闭容器中进行,所有物质不与外界交换,则最后所得溶液的质量分数为 。
(3)循环操作的次数与二氧化氮在生成硝酸的转化率具有一定的数学关系。计算一定量的二氧化氮气体大约要经过 次循环操作,才能使二氧化氮的转化率约为96%。
问题2:将上述方法制得的硝酸,可以稀释成浓缩得各种不同浓度的硝酸。大量实验证明,同一金属与不同浓度的硝酸反应可生成不同的还原产物。某研究小组实验研究了镁与不同浓度硝酸反应,测得气体产物主要有H2、N2、NO、NO2,溶液中的产物主要有Mg(NO3)2、NH4NO3、H2O。
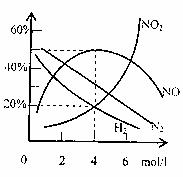
(4)现有0.96Mg与足量浓度为4mol/l的HNO3完全反应,收集到224ml(S.T.P)气体,各气体产物成分和所有硝酸浓度曲线如下图所示。通过计算确定还原产物的组成及各成分的物质的量之比是多少?
30.有55.29g碳酸钾和氯化钙的混合物,在40℃将其加入一定量的水中,碳酸钾和氯化钙刚好完全反应并得到氯化钾的饱和溶液。在该温度下过滤(假定过滤时无损耗),得到104.3g滤液,将滤渣干燥后称量为22.9g。求:
(1)原混合物中碳酸钾的含量分数;
(2)40℃氯化钾的溶解度。
29.下面是有名的Diels-Alder反应的一个实例:
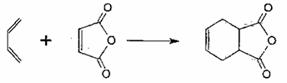
请利用已知反应方程式,回答下列问题:
(1)写出下列反应产物的结构简式:
H2C=CH-CH=CH-CH3+H2C=CH-CHO→ 。
(2)以某链烃A为起始原料合成化合物G的路径如下(图中Mr表示相对分子质量)
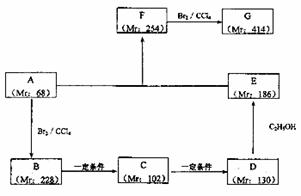
①指出反应类型B→C: ,F→G 。
②写出下列物质的结构简式:
A: ,
F: 。
③写出下列反应式的化学方程式:
B→C: ;
D→E: 。
④写出G与氢氧化钠溶液反应的方程式
。
28.图中A、B、C、D、E、F、G均为有机化合物。
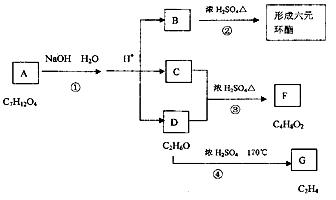
根据上图回答问题:
(1)D的化学名称 ;
(2)反应③的化学方程式是 ;
(3)B的结构简式是 ,A的结构简式是 ,反应③的反应类型是 ;
(4)G是重要的工业原料,用化学方程式表示G的一种重要的工业用途 。
27.某校化学研究性学习小组,在学习金属的冶炼以后,对一氧化碳还原金属氧化物的实验非常感兴趣,他们查阅有关资料后分析:
(1)学生对相关装置进行分析和比较发现这些装置既有各自的优点,同时也发现各个 中均存在一些不足,具体看下表:

(2)根据高三拓展教材中一氧化碳还原氧化铁的实验要求,在上述实验的基础上学生设计了相对更为合理的实验,重点避免了上述三个不足。其中一氧化碳的制备是利用甲酸和浓硫酸共热到60-80℃可发生脱水反应:
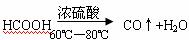 HCOOH
CO↑+H2O
HCOOH
CO↑+H2O
请根据以下各图进行选择形成一套相对较为合理的实验装置图(某些装置可重复使用)
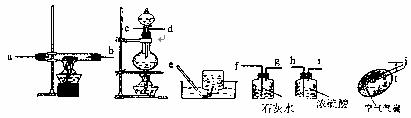
(3)回答以下问题:
①合理实验装置的连接顺序是(写小写字母) 。
②在反应时强调先产生一氧化碳气体,一会再点燃加热氧化铁的酒精灯,原因是 ( )
A.因为一般反应从左到右进行
B.排除体系内的空气,使反应过程更安全
C.甲酸与浓硫酸反应可以产生大量的CO气体
D.此反应加热时间长有利于产生CO
③请说出你所选择的第一个石灰水洗气瓶的作用是 。
④在观察到硬质玻璃管中由 色完全变为 时停止加热,然后继续 ,原因是防止铁被氧化。
⑤硬质玻璃管中发生反应的化学方程式是 。
⑥该实验的一个优点是把实验过程中的尾气利用排水法收集到起来,收集的气体前后有几瓶,若分别先后编号,点燃各个瓶中的气体,中间编号的集气瓶中气体 ,前后编号的集体瓶中气体 ,原因是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com