
12. 下列叙述正确的是
A. 0.01 mol /L CH3COOH与pH = 12的NaOH溶液混合,若c(CH3COO-) >c(Na+)混合液一定呈碱性
B. 常温下,将等体积0.0lmo/L HCl和pH = 12的氨水混合,则混合液的pH <7
C. 0.0lmol/L的某二元弱酸盐Na2A溶液中,c( Na+)= c(H2A) + c( HA-)+ (A2- )
D. 将5mL0.02mol/L的H2SO4与5 mL 0.02mol/L NaOH溶液充分混合,若混合后溶液的体积为10mL, 则混合液的pH =2
11. 如图是198K 时N2与H2反应过程中能量变化的曲线图。下列叙述正确的是
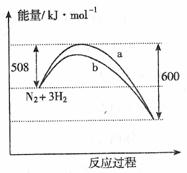
A. 该反应的热化学方程式为:N2 +
3H2  2NH3,
△H = -92kJ·mol-1
2NH3,
△H = -92kJ·mol-1
B. a曲线是加入催化剂时的能量变化曲线
C. 加入催化剂, 该化学反应的反应热改变
D. 在温度体积一定的条件下, 通入lmol N2和3molH2 反应后放出的热量为Q1kJ, 若通入2mol N2和6mol H2 反应后放出的热量为Q2kJ 则184>Q2 >2Q1
10. 室温下,甲溶液中水电离出的H+浓度为10-12 mol /L, 乙溶液中水电离出的H+浓度为10-2 mol /L,下列说法正确的是
A. 甲乙两溶液的pH不可能相同
B. 甲乙两种溶液中加入Al粉都一定会产生H2
C. HCO3-不可能在甲、乙两溶液中大量共存
D. 甲不可能是盐溶液 , 乙不可能是酸或碱溶液
9. 一定温度下,在体积为 VL 的密闭容器中加入1molX和1molY进行如下反应:X(g) + Y(g )  2Z(g )+
W(s) △H >0达到平衡,下列判断正确的是
2Z(g )+
W(s) △H >0达到平衡,下列判断正确的是
A. 向平衡混合物中加入少量W, 正、逆反应速率均增大
B. 平衡后加入X,上述反应的△H增大
C. 温度不变,将容器的体积变为2VL,Z的平衡浓度变为原来的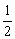
D. 当容器中混合气体的压强不变时,可以证明此反应已达到平衡状态
8. 下列三种有机物是某些药物中的有效成分
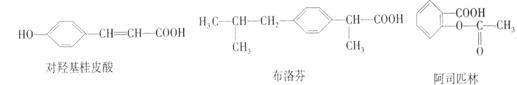
下列说法正确的是
A. 三种有机物都是芳香烃
B. 三种有机物苯环上的氢原子若被氯原子取代,其一氯代物都只有2种
C. 将等物质的量的三种物质加入NaOH溶液中,阿司匹林消耗NaOH最多
D. 1mol 对羟基桂皮酸最多可以和1mol Br2反应
7. 下列叙述中正确的是
A. 第三周期元素的离子半径从左到右依次减小
B. HCl、PCl5、N2、CO2分子中所有原子都满足最外层8电子的结构
C. 晶体内可以不存在化学键,也可以同时存在离子键,极性键和非极性键
D. 若某离子化合物X2Y3中X3+和 Y2-的电子层结构相同, 则X、 Y两元素的原子序数之差可能是5、15或29
6. 下列各项中的两个量,其比值一定为1:2的是
A. 固体Na2O2中阴离子与阳离子的个数
B. 相同温度下0.l mol /L的CH3COOH与 0.2mol /L的CH3COOH溶液中的c(H+)
C. 液面在“0”刻度时,25mL碱式滴定管和50mL碱式滴定管所盛溶液的体积
D. 在反应2H2S + SO2= 3S ↓ + 2H2O中氧化产物与还原产物的质量
5. 化学实验设计和操作中必须十分重视安全问题和环境保护问题,下列实验的设计或操作不合理的是
①实验室用 KClO3热分解法制O2,排水收集O2后先停止加热,再拆除实验装置。
②实验结束后应将固体残渣深埋入土壤中,废液倒入下水道排出。
③给试管中的液体加热时应不时移动试管或加入碎瓷片,以免暴沸伤人。
④为检验CO气体的纯度,用排空法收集一试管气体,然后移近火焰点燃听有无尖锐爆鸣声。
A. ①② B. ①②③④ C. ①②④ D. ②④
4. 下列离子方程式书写正确的是
A. 少量稀 HNO3中加入足量铁粉:Fe + 4H+ + NO3- =NO↑ + Fe3+ +2H2O
B. 以石墨作电极电解MgCl2溶液:2Cl- +
2H2O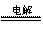 2OH- + H2 ↑+ Cl2↑
2OH- + H2 ↑+ Cl2↑
C. NH4HCO3溶液中加入过最石灰水:HCO3- + Ca2+ +OH-=CaCO3 ↓ +H2O
D. 沸水中滴加FeCl3饱和溶液制备Fe(OH)3(胶体):Fe3++3H2O Fe(OH)3
(胶体) +3H+
Fe(OH)3
(胶体) +3H+
3. 某炼金厂的废水因连降暴雨而溢出,导致河水严重污染。炼金废水中所含CN-有剧毒,其性质与卤素离子相似,还原性介于I-与 Br-之间,HCN为弱酸。下列说法不正确的是
A. CN-可以和稀硫酸反应生成 HCN B. CN-可被Cl2氧化成(CN)2
C. 0.l mol /L HCN溶液pH =1 D. CN-的电子式为[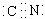 ]-
]-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com