
6£Æœ¬¡–µÁ◊” Ω±Ì æµƒŒÔ÷ ÷–£¨ Ù”⁄º´–‘∑÷◊”µƒ «°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° (°°°° )
A£Æ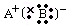 °°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° B£Æ
°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° B£Æ °°°°°°°°°°°°°°°° °°
°°°°°°°°°°°°°°°° °°
C£Æ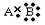 °°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °°°° D£Æ
°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °°°° D£Æ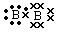 °°°°°°°°°°°°°°°°°°°°°°°°°°°°
°°°°°°°°°°°°°°°°°°°°°°°°°°°°
21. (10 ∑÷)»À¿ý‘⁄ π”√Ω Ùµƒ¿˙ ∑Ω¯≥Ã÷–£¨æ≠¿˙¡ÀÕ≠°¢Ã˙°¢¬¡÷Æ∫Û£¨µ⁄Àƒ÷÷Ω´±ªπ„∑∫”¶”√µƒΩ Ù±ªø∆—ߺ“‘§≤‚ «Ó—(Ti)£¨À¸±ª”˛Œ™°∞Œ¥¿¥ ¿ºÕµƒΩ Ù°±°£ ‘ªÿ¥œ¬¡–Œ £∫
( 1 ) Ti ‘™Àÿ‘⁄‘™Àÿ÷Ð∆⁄±Ì÷–µƒŒª÷√ «µ⁄°°°°°° ÷Ð∆⁄£¨µ⁄°°°°°° ◊£ª∆‰ª˘Ã¨‘≠◊”µƒº€µÁ◊”°° ≤„≈≈≤ºŒ™°°°°°°°°°° £ª
(2) ‘⁄TiµƒªØ∫œŒÔ÷–£¨ø…“‘≥ œ÷+2°¢+3°¢+4 »˝÷÷ªØ∫œº€£¨∆‰÷–“‘+4º€µƒTi◊ÓŒ™Œ»∂®£ª
¢Ÿ∆´«’À·±µµƒ»»Œ»∂®–‘∫√£¨ΩȵÁ≥£ ˝∏þ£¨‘⁄–°–Õ±‰—π∆˜°¢ª∞Õ≤∫Õ¿©“Ù∆˜÷–∂º”–”¶”√°£∆´Ó—À·±µæßÃÂ÷–æß∞˚µƒΩ·ππ æ“‚Õº»ÁÕº£¨À¸µƒªØ—ß Ω «°°°°°°°°°°°°°° £ª
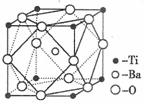
¢⁄“—÷™Ti3+ø…–Œ≥…≈‰Œª ˝Œ™6µƒ≈‰∫œŒÔ°£œ÷”–∫¨Ó—µƒ¡Ω÷÷—’…´µƒæß㨓ª÷÷Œ™◊œ…´£¨¡Ì“ªŒ™¬Ã…´£¨µ´œýπÿ µ—È÷§√˜£¨¡Ω÷÷æßõƒ◊È≥…Ω‘Œ™TiCl3°§6H2O°£Œ™≤‚∂®’‚¡Ω÷÷æßõƒªØ—ß Ω£¨…˺∆¡À»Áœ¬ µ—È£∫
a. ∑÷±»°µ»÷ ¡øµƒ¡Ω÷÷≈‰∫œŒÔæßõƒ—˘∆∑≈‰≥…¥˝≤‚»Ð“∫£ª
b. ∑÷±Õ˘¥˝≤‚»Ð“∫÷–µŒ»ÎAgNO3»Ð“∫£¨æ˘≤˙…˙∞◊…´≥¡µÌ£ª
c. ≥¡µÌÕÍ»´∫Û∑÷±π˝¬Àµ√¡Ω∑ð≥¡µÌ£¨æ≠œ¥µ”∏…‘Ô∫Û≥∆¡ø£¨∑¢œ÷‘≠¬Ã…´æßõƒÀƻГ∫”ÎAgNO3»Ð“∫∑¥”¶µ√µΩµƒ∞◊…´≥¡µÌ÷ ¡øŒ™◊œ…´æßõƒÀƻГ∫∑¥”¶µ√µΩ≥¡µÌ÷ ¡øµƒ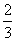 °£
°£
‘ڬÅ´æßÃÂ≈‰∫œŒÔµƒªØ—ß ΩŒ™°°°°°°°°°°°°°°°°°°°°°°°°°°°° £¨¬Ã…´æßÃÂ÷–∫¨”–ªØ—ߺ¸¿ý–Õ «°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
20. (10∑÷)°°°°°°°°°°°°°°°°°° Œ™”–ª˙ŒÔAµƒΩ·ππºÚ Ω£¨ø…“‘Õ®π˝≤ªÕ¨µƒ∑¥”¶÷∆µ√œ¬¡–ŒÔ÷ °£
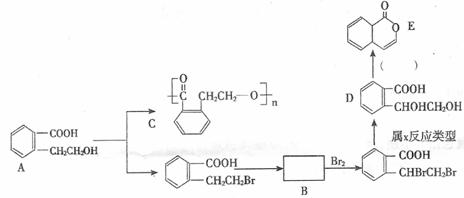
(1) –¥≥ˆA °˙ CµƒªØ—ß∑Ω≥Ã Ω£∫°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
(2) Õ∆∂œBŒÔ÷ µƒΩ·ππºÚ Ω°°°°°°°°°°°°°°°°°°°°°° £ªX∑¥”¶¿ý–Õ «°°°°°°°°°°°°°°°° £ª”… D °˙ E À˘–˵ƒ ‘º¡ «°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
(3) RŒÔ÷ Ù”⁄A µƒÕ¨∑÷“Ïππã¨∆‰–‘÷ »Áœ¬£∫
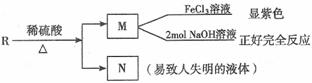
‘–¥≥ˆ∑˚∫œÃıº˛µƒRµƒÕ¨∑÷“ÏππõƒΩ·ππºÚ Ω(»Œ–¥¡Ω÷÷) £∫°°°°°°°°°° £ª°°°°°° °°°£
19. (7∑÷)œ¬Õº±Ì æ∏˜ŒÔ÷ ÷ƺ‰µƒ◊™ªØπÿœµ°£“—÷™£∫A°¢D°¢F°¢H æ˘Œ™µ•÷ £¨X≥£Œ¬œ¬Œ™ŒÞ…´“∫ã¨BŒ™µ≠ª∆…´πÃã¨J»Ð”⁄À·µ√µΩª∆…´»Ð“∫°£«Î∞¥“™«ÛÃÓø’£∫
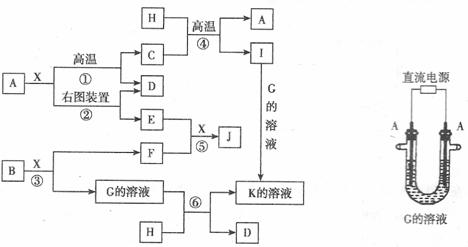
(1)–¥≥ˆ…˙≥…EµƒµÁº´∑¥”¶ Ω£∫°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° £¨∑¥”¶¢ðµƒœ÷œÛ «°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
(2)∑¥”¶¢ŸµƒªØ—ß∑Ω≥Ã Ω «°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° £¨‘⁄ µ—È “÷–“˝∑¢∑¥”¶¢Ðµƒ≤Ÿ◊˜ «°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
(3)∑¥”¶¢Þµƒ¿Î◊”∑Ω≥Ã Ω «°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
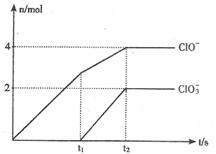
18. (8∑÷) ‘⁄“ª∂®¡øµƒ ت“»È÷–Õ®»Î“ª∂®¡øµƒ¬»∆¯£¨∂˛’þ«°∫√ÕÍ»´∑¥”¶ (∑¢…˙µƒ∑¥”¶æ˘Œ™∑≈»»∑¥”¶) °£…˙≥…ŒÔ÷–”–»˝÷÷∫¨¬»‘™Àÿµƒ¿Î◊”£¨∆‰÷–¡Ω÷÷¿Î◊”µƒŒÔ÷ µƒ¡ø(n)”Î∑¥”¶ ±º‰ (t) µƒ«˙œþ»ÁÕºÀ˘ æ°£“—÷™£¨…˙≥…C1O3-µƒ∑¥”¶Œ™£∫6Ca (OH)2 + 6C12 = 5CaC12 + Ca (C1O3 ) 2 +6H2O°£
‘ªÿ¥£∫
(1) t2 ±£¨Ca(ClO)2”ÎCa (ClO3) 2µƒŒÔ÷ µƒ¡ø÷Æ∫ÕŒ™°°°°°°°° mol£¨∏√ ت“»È÷–∫¨”–µƒCa(OH)2µƒ÷ ¡ø «°°°°°°°°°° g°£
°° (2)æð∑÷Œˆ£¨…˙≥…Ca (ClO3) 2µƒ∑¥”¶ «”…Œ¬∂»…˝∏þ“˝∆µƒ£¨Õ®»À¬»∆¯µƒÀŸ∂»≤ªÕ¨£¨n(ClO -)∫Õn(ClO3-) µƒ±»¿˝“≤≤ªÕ¨°£»Ù‘⁄‘≠ ت“»È÷–Õ®»Î¬»∆¯µƒÀŸ∂»º”øÏ£¨‘Ú∑¥”¶∫Û
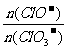 °°°°°° 2(ÃÓ°∞>°±°¢°∞<°±ªÚ°∞=°±)
°°°°°° 2(ÃÓ°∞>°±°¢°∞<°±ªÚ°∞=°±)
(3) = a£¨‘Ún(Cl -)=
°°°°°°°°°°°°°°mol
(”√∫¨aµƒ¥˙ ˝ Ω±Ì æ) °£
= a£¨‘Ún(Cl -)=
°°°°°°°°°°°°°°mol
(”√∫¨aµƒ¥˙ ˝ Ω±Ì æ) °£
17. (10 ∑÷) Ω´≤ªÕ¨¡øµƒH2O(∆¯) ∫ÕCO ∆¯ÃÂ∑÷±Õ®»ÎµΩ“ªÃª˝Œ™l Lµƒ∫„»ð√б’»ð∆˜÷–Ω¯––∑¥”¶£∫H2O (g) + CO( g)  CO2 (g) +H2(g)£ªµ√µΩ“‘œ¬»˝◊È ˝æð£¨æð¥Àªÿ¥œ¬¡–Œ £∫
CO2 (g) +H2(g)£ªµ√µΩ“‘œ¬»˝◊È ˝æð£¨æð¥Àªÿ¥œ¬¡–Œ £∫
|
µ—È◊È |
Œ¬∂» |
∆ º¡ø |
∆Ω∫‚¡ø |
¥ÔµΩ∆Ω∫‚À˘–Ë ±º‰ |
||
|
H2O |
CO |
H2 |
CO |
|||
|
1 |
650°Ê |
1 mol |
2 mol |
0.8 mol |
1.2 mol |
5 min |
|
2 |
900°Ê |
0.5 mol |
1 mol |
0.2 mol |
0.8 mol |
3 min |
|
3 |
900°Ê |
a |
b |
c |
d |
t |
( 1 ) ¢Ÿ”…“‘…œ ˝æ𣨠µ—È1÷–“‘v( CO2) ±Ì 浃∑¥”¶ÀŸ¬ Œ™°°°°°°°°°°°°°° °£
°°°°°° ¢⁄∏√∑¥”¶‘⁄650°Ê ±∆Ω∫‚≥£ ˝ ˝÷µŒ™°°°°°°°°°° £¨∏√∑¥”¶µƒƒÊ∑¥”¶Œ™°°°°°° °°(ÃÓ°∞Œ¸°± ªÚ°∞∑≈°±)»»∑¥”¶°£
¢€»Ù µ—È3“™¥ÔµΩ”Î µ—È2œýÕ¨µƒ∆Ω∫‚◊¥Ã¨(º¥∏˜ŒÔ÷ µƒ÷ ¡ø∑÷ ˝∑÷±œýµ»)£¨«“t < 3min£¨
‘Úa°¢b ”¶¬˙◊„µƒπÿœµ «°°°°°°°°°°°° °£
(2)œ¬Õº1°¢2 ±Ì æ…œ ˆ∑¥”¶‘⁄ ±øÃt1¥ÔµΩ∆Ω∫‚£¨‘⁄ ±øÃt2“Ú∏ƒ±‰ƒ≥∏ˆÃıº˛∂¯∑¢…˙±‰ªØµƒ°° «Èøˆ£∫
°°°°°° ¢ŸÕº1÷– ±øÃt2∑¢…˙∏ƒ±‰µƒÃıº˛ø…ƒÐ «°°°°°°°°°°°°°°°°°°°° °° (–¥“ªÃıº¥ø…£¨œ¬Õ¨)°£
°°°°°° ¢⁄Õº2÷– ±øÃt2∑¢…˙∏ƒ±‰µƒÃıº˛ø…ƒÐ «°°°°°°°°°°°°°°°°°°°°°° °£

(3) ‘⁄850°Ê ±£¨∆‰∆Ω∫‚≥£ ˝K = 1£¨850°Ê ±‘⁄∏√»ð∆˜÷–Õ¨ ±≥‰»À1.0moICO£¨3.0 molH2O£¨1.0molCO2£¨5.0molH2£¨¥À ±∑¥”¶œÚ°°°°°°°° (ÃÓ°∞’˝∑¥”¶°± ªÚ°∞ƒÊ∑¥”¶°±)∑ΩœÚΩ¯––£¨∆Ω∫‚ ±CO2µƒŒÔ÷ µƒ¡øŒ™°°°°°°°°°° °£
16. (10∑÷)œ¬Õº÷–√ø“ª∑ΩøÚ¥˙±Ì“ª÷÷∑¥”¶ŒÔªÚ…˙≥…ŒÔ

(1)»ÙX”… M°¢N¡Ω÷÷∂Ã÷Ð∆⁄«“Õ¨÷Ð∆⁄‘™Àÿ◊È≥…£¨M‘≠◊”µƒ◊ÓÕ‚≤„µÁ◊” ˝ «◊Óƒ⁄≤„µÁ◊” ˝µƒ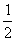 £¨N‘™Àÿ◊Ó∏þ’˝º€”ÎÀ¸µƒ∏∫º€¥˙ ˝∫ÕŒ™6°£∑¥”¶¢Ðµƒ ˝æð»Á”“…œ±Ì∏ÒÀ˘ æ°£
£¨N‘™Àÿ◊Ó∏þ’˝º€”ÎÀ¸µƒ∏∫º€¥˙ ˝∫ÕŒ™6°£∑¥”¶¢Ðµƒ ˝æð»Á”“…œ±Ì∏ÒÀ˘ æ°£
¢Ÿ–¥≥ˆ∑¥”¶¢⁄µƒ¿Î◊”∑Ω≥Ã Ω°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °°°£
¢⁄ŒÔ÷ G µƒÀƻГ∫÷–¿Î◊”≈®∂»”…¥ÛµΩ–°µƒÀ≥–ÚŒ™°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
(2)»ÙX «“ª÷÷∫¨—ıÀ·—Œ£¨«“B «“ª÷÷π˝∂…‘™ÀÿµƒΩ Ù£¨∑¥”¶¢ŸÀ˘µ√B°¢CµƒŒÔ÷ µƒ¡ø÷Ʊ»Œ™4£∫1£¨∑¥”¶¢⁄≤ª–ËÃÿ∂®µƒ∑¥”¶Ãıº˛æÕƒÐΩ¯––£¨«“Aµƒ≈®∂»≤ªÕ¨£¨≤˙ŒÔE≤ªÕ¨£¨‘ÚXŒÔ÷ µƒªØ—ß Ωø…ƒÐ «°°°°°°°°°°°°°°°° °£
(3) »ÙX «“ª÷÷∫¨—ıÀ·—Œ£¨B «Ω Ùµ•÷ £¨C°¢D «∑«Ω Ùµ•÷ £¨∑¥”¶¢⁄–Ë“™B”ÎAµƒ≈®»Ð“∫π≤»»≤≈ƒÐΩ¯––£¨«“…˙≥…µƒE”ÎG «Õ¨“ª÷÷ŒÔ÷ °£
°°°°°° –¥≥ˆ∑¥”¶¢ŸµƒªØ—ß∑Ω≥Ã Ω°°°°°°°°°° °°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°£
°°°°°° 1g πÃè D ‘⁄ C ÷–ÕÍ»´∑¥”¶∑≈≥ˆ 9.3kJ µƒ»»¡ø , –¥≥ˆ∏√∑¥”¶µƒ»»ªØ—ß∑Ω≥à Ω
°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
15. (13∑÷) »˝—ıªØ∂˛Ã˙∫Õ—ıªØ—«Õ≠∂º «∫Ï…´∑€ƒ©£¨≥£”√◊˜—’¡œ°£ƒ≥–£“ªªØ—ß µ—È–°◊ÈÕ®π˝ µ—È¿¥ÃΩæø“ª∫Ï…´∑€ƒ© «Fe2O3°¢Cu2OªÚ∂˛’þªÏ∫œŒÔ°£ÃΩæøπ˝≥ûÁœ¬£∫
≤È‘ƒ◊ ¡œ£∫Cu2O «“ª÷÷ºÓ–‘—ıªØŒÔ, »Ð”⁄œ°¡ÚÀ·…˙≥…Cu∫ÕCuSO4, ‘⁄ø’∆¯÷–º”»»…˙≥…CuO
÷≥ˆºŸ…Ë
ºŸ…Ë1£∫∫Ï…´∑€ƒ© «Fe2O3
ºŸ…Ë2£∫∫Ï…´∑€ƒ© «Cu2O
ºŸ…Ë3£∫∫Ï…´∑€ƒ© «Fe2O3∫ÕCu2OµƒªÏ∫œŒÔ
…˺∆ÃΩæø µ—È
»°…Ÿ¡ø∑€ƒ©∑≈»Î◊„¡øœ°¡ÚÀ·÷–£¨‘⁄À˘µ√»Ð“∫÷–‘ŸµŒº” KSCN ‘º¡°£
(1)»ÙºŸ…Ë1≥…¡¢£¨‘Ú µ—Èœ÷œÛ «°°°°°°°°°°°° °°°°°°°°°°°°°£
(2)»ÙµŒº” KSCN ‘º¡∫ۻГ∫≤ª±‰∫Ï…´£¨‘Ú÷§√˜‘≠πÃÃÂ∑€ƒ©÷–“ª∂®≤ª∫¨»˝—ıªØ∂˛Ã˙°£ƒ„»œŒ™’‚÷÷Àµ∑®∫œ¿Ì¬£ø°°°°°°°°°° ºÚ ˆƒ„µƒ¿Ì”…(≤ª–Ë–¥≥ˆ∑¥”¶µƒ∑Ω≥Ã Ω )°°°°°°°°°°
°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
(3)»ÙπÃÃÂ∑€ƒ©ÕÍ»´»ÐΩ‚‘™πÃÃ¥ʑ⁄ , µŒº” KSCN ‘º¡ ±»Ð“∫≤ª±‰∫Ï…´ , ‘Ú÷§√˜‘≠πÃÃÂ∑€ƒ© «°°°°°°°°°° £¨–¥≥ˆ∑¢…˙∑¥”¶µƒ¿Î◊”∑Ω≥Ã Ω°°°°°°°°°°°°°°°°°°°° °°°°°°°°°°°°°°
°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
ÃΩæø—”…Ï
æ≠ µ—È∑÷Œˆ£¨»∑∂®∫Ï…´∑€ƒ©Œ™Fe2O3∫ÕCu2OµƒªÏ∫œŒÔ°£
(4) µ—È–°◊È”˚”√º”»»∑®≤‚∂®Cu2Oµƒ÷ ¡ø∑÷ ˝°£»°a gπÃÃÂ∑€ƒ©‘⁄ø’∆¯÷–≥‰∑÷º”»»£¨¥˝÷ ¡ø≤ª‘Ÿ±‰ªØ ±£¨≥∆∆‰÷ ¡øŒ™bg( b > a)£¨‘ÚªÏ∫œŒÔ÷–Cu2Oµƒ÷ ¡ø∑÷ ˝Œ™°°°°°°°° °£
(5) µ—È–°◊È”˚¿˚”√∏√∫Ï…´∑€ƒ©÷∆»°Ωœ¥ø檵ƒµ®Ì∂ (CuS04 . 5H20) °„æ≠≤È‘ƒ◊ ¡œµ√÷™ ,
‘⁄»Ð“∫÷–Õ®π˝µ˜Ω⁄»Ð“∫µƒÀ·ºÓ–‘∂¯ πCu2 +°¢Fe2+°¢Fe3+∑÷±…˙≥…≥¡µÌµƒpH »Áœ¬£∫
|
ŒÔ÷ |
Cu(OH)2 |
Fe(OH)2 |
Fe(OH)3 |
|
ø™ º≥¡µÌpH |
6.0 |
7.5 |
1.4 |
|
≥¡µÌÕÍ»´pH |
13 |
14 |
3.7 |
µ—È “”–œ¬¡– ‘º¡ø…π©—°‘Ò£∫A. ¬»ÀÆ°° B. H2O2 °°°°C. NaOH°° D. Cu2(OH)2CO3
µ—È–°◊ȅ˺∆»Áœ¬ µ—È∑Ω∞∏£∫

‘ªÿ¥£∫
¢Ÿ ‘º¡IŒ™°°°°°° £¨ ‘º¡IIŒ™°°°°°° (ÃÓ◊÷ƒ∏)°£
¢⁄ πÃÃÂXµƒªØ—ß ΩŒ™°°°°°°°°°° °£
¢€ ≤Ÿ◊˜IŒ™°°°°°°°°°°°°°°°°°° °£
14. µÁ∆ø≥µÀ˘”√µÁ≥ÿ“ª∞„Œ™«¶–ÓµÁ≥ÿ£¨’‚ «“ª÷÷µ‰–Õµƒø…≥‰µÁµÁ≥ÿ£¨µÁ≥ÿ ◊Ð∑¥”¶ ΩŒ™£∫
Pb+PbO2+4H++
2SO4+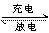 2PbSO4
+2H2O
2PbSO4
+2H2O
‘Úœ¬¡–Àµ∑®’˝»∑µƒ «£∫
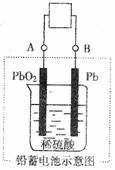
A. ∑≈µÁ ±£∫µÁ¡˜∑ΩœÚ”…BµΩA
B. ≥‰µÁ ±£∫—Ùº´∑¥”¶ «PbSO4 - 2 e- + 2H2O = PbO2 + SO42- +4H+
C. ≥‰µÁ ±£∫«¶–ÓµÁ≥ÿµƒ∏∫º´”¶”Î≥‰µÁ∆˜µÁ‘¥µƒ’˝º´œý¡¨
D. ∑≈µÁ ±£∫’˝º´∑¥”¶ « Pb - 2e- +SO42- = PbSO4
µ⁄IIæÌ (∑«—°‘Ò π≤58∑÷)
13. ∂Ã÷Ð∆⁄‘™ÀÿA°¢B°¢C°¢D°¢Eµƒ‘≠◊”–Ú ˝“¿¥Œ‘ˆ¥Û£¨À¸√«µƒ‘≠◊”∫ÀÕ‚µÁ◊”≤„ ˝÷Æ∫ÕŒ™10£ªBµƒªØ∫œŒÔ÷÷¿ý∑±∂ý£¨ ˝ƒø≈”¥Û£¨A°¢E Õ¨÷˜◊£¨B°¢C°¢DÕ¨÷Ð∆⁄œý¡⁄°£œ¬¡–Àµ∑®≤ª’˝»∑µƒ «
A. ≥£º˚ªØ∫œŒÔE2D2”ÎÀÆ∑¥”¶…˙≥…Dµƒµ•÷ £¨Õ¨ ±…˙≥…µƒ»Ð“∫ƒÐ π∑”Ù ‘“∫±‰∫Ï
B. Cµƒ«‚ªØŒÔ”ÎCµƒ◊Ó∏þº€—ıªØŒÔµƒÀƪ،Ô∑¥”¶µ√µΩµƒ≤˙ŒÔ÷–º»”–¿Î◊”º¸”÷”–π≤º€º¸
C. D”ÎA°¢B°¢C°¢E∑÷±Ω·∫œæ˘ƒÐ–Œ≥…¡Ω÷÷ªÚ¡Ω÷÷“‘…œµƒªØ∫œŒÔ
D. ŒÂ÷÷‘™Àÿµƒ‘≠◊”∞Îæ∂∞¥A-EµƒÀ≥–Ú“¿¥Œ‘ˆ¥Û
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com