
17.(13分)硫酸铵是一种常用的铵态氮肥。下表是硫酸铵化肥品质的主要指标。
|
指标 项目 |
优等品 |
一等品 |
合格品 |
|
外观 |
白色结晶,无可见机械杂质 |
无可见机械杂质 |
|
|
氮(N)含量 |
≥21.0% |
≥21.0% |
≥20. 5% |
新华中学化学研究性学习小组为本地农业生产服务,对某农用品商店出售的一等品硫酸铵化肥的品质进行探究。
[观察外观] 该硫酸铵化肥无可见机械杂质。
[实验探究]按下图所示装置进行实验。
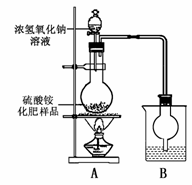
(1)烧瓶内发生反应的离子方程式为: 烧杯中最适宜盛放的试剂是 (填“浓硫酸”、“稀硫酸”或“水”)。
(2)实验过程中,需往烧瓶中加入足量浓氢氧化钠溶液并充分加热的原因是
。
[交流讨论]
甲同学:根据此实验测得的数据,计算硫酸铵化肥的含氮量可能偏高,因为实验装置中存在一个明显缺陷是:
乙同学:实验装置中还存在另一个明显缺陷是:
经过大家充分讨论一致认为:针对甲、乙两位同学指出的实验装置中存在的明显缺陷,需改进实验装置,重新进行实验。
[探究结论]
称取13.5 g硫酸铵化肥样品,用改进后的实验装置重新进行实验,测得实验前后B装置增重3.40 g。该化肥 (填“是”或“不是”)一等品。
16.(5分)用下图所示装置进行实验。

实验步骤:检查气密性;装入少许白磷、红磷;打开夹子K,通入氧气;点燃酒精灯(加热位置如图所示)。
(1)该实验主要用于比较白磷和红磷的 ,还能证明“磷能在氧气中燃烧”。在硬质玻璃管中可以观察到有 (填“白烟”或“白雾”)生成。
(2)该实验符合化学实验设计“环保策略”,主要体现在:
15.下列溶液一定呈中性的是 ( )
A.将pH=5的盐酸稀释100倍所得到的溶液
B.等物质的量的强酸和强碱反应后所得到的混合溶液
C.c (H+) = c (OH-) = 1×10-6 mol·L-1的溶液
D.非电解质溶于水得到的溶液
第Ⅱ卷(非选择题 共55分)
|
14.如下图所示,试管①中盛有96℃的水,试管②中充满气体B,将液体A滴入试管②中,充分反应后打开夹子K,发现试管①中的水立刻沸腾。则A与B可能是 ( )
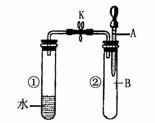
A.水与氮气
B.稀硫酸与一氧化碳
C.饱和食盐水与氯气
D.浓氢氧化钠溶液与二氧化碳
13.黄磷(P4)与浓氢氧化钾溶液反应的化学方程式为:
P4 + 3KOH + 3H2O  PH3↑+
3KH2PO2
PH3↑+
3KH2PO2
被氧化的P与被还原的P的质量之比为 ( )
A.1∶2 B.2∶1 C.3∶1 D.1∶3
12.下列各组物质发生反应时,生成物不因反应条件(浓度、温度或催化剂)的不同而不同的是 ( )
A.Cu与HNO3 B.C2H5OH与O2 C.Na与O2 D.SO2与O2
11.下列实验方案不合理的是 ( )
A.用分液法分离苯和四氯化碳的混合液
B.用焰色反应鉴别NaCl和KCl
C.用饱和Na2CO3溶液除去乙酸乙酯中混有的乙酸和乙醇
D.用KSCN溶液检验FeCl2是否已被氧化而变质
10.酸性高锰酸钾溶液与草酸溶液反应的化学方程式为:
2KMnO4 + 3H2SO4 + 5H2C2O4 == K2SO4 + 2MnSO4 + 10CO2↑ + 8H2O
|
A.增大酸性高锰酸钾溶液的浓度 B.增大草酸溶液的浓度
C.增大压强 D.升高温度
9.下列有关比较中,错误的是 ( )
A.热稳定性:NH3>PH3>H2S
B.熔点:石英>食盐>冰
C.酸性:醋酸>碳酸>苯酚
D.分散质粒子的直径: Fe(OH) 3悬浊液>Fe(OH) 3胶体>FeCl3溶液
8.下列离子方程式正确的是 ( )
A.电解饱和食盐水:Cl- + H2O == OH- + H2↑+ Cl2↑
B.用食醋除去热水瓶胆水垢:2H+ + Mg(OH)2 == Mg2+ + 2H2O
C.用氯化铁溶液腐蚀印刷电路板:Fe3++ Cu == Fe2++ Cu2+
D.用胃舒平Al (OH)3治疗胃酸(含盐酸)过多症Al (OH)3 + 3H+ ==Al3++ 3H2O
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com