
18.4mol·L-1)。设计实验方案来研究影响反应速率的因素。
甲同学研究的实验报告如下表:
|
实验步骤 |
现 象 |
结 论 |
|
①分别取等体积的2 mol·L-1的硫酸于试管中 ② |
反应速率Mg>Fe,Cu不反应 |
金属的性质越活泼,反应速率越快 |
(1)甲同学表中实验步骤②为
。
(2)甲同学的实验目的是 ;要得出正确的实验结论,还需控制的实验条件是 。
乙同学为了更精确的研究浓度对反应速率的影响,利用下图所示装置进行定量实验。

(3)乙同学在实验中应该测定的数据是 。
(4)乙同学完成该实验应选用的实验药品是 。
实验中不选用某浓度的硫酸,理由是 。
实验二:已知2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+8H2O+10CO2↑,在高锰酸甲酸性溶液和草酸溶液反应时,发现开始一段时间,反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快。
(5)针对上述实验现象,丙同学认为KMnO4与H2C2O4反应放热,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你猜想还可能是 的影响。
(6)若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液外,还需要选择的试剂最合理的是 (填字母)
A.硫酸钾 B.硫酸锰 C.二氯化锰 D.水
[选做部分]
共8题,考生必须从中选择2个物理、1个化学题和1个生物题在答题纸规定的区域作答。
30.(16分)影响化学反应速率的因素很多,某校化学小组用实验的方法进行探究。
实验一:他们只利用Cu、Fe、Mg和不同浓度的硫酸(0.5mol·L-1、2mol·L-1、
29.(12分)下图所涉及的物质均为中学化学中的常见物质,其中C、D、E为单质,其余为化合物。它们存在如下图所示的转化关系,反应中生成的水及次要产物均已略去。
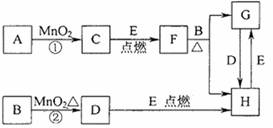
(1)写出化学式:B ,E 。
(2)指出MnO2在相关反应中的作用:反应①中是 剂,反应②中是 剂。
(3)完成F与B反应的化学方程式 。
(4)若反应①是在加热条件下进行,A是 ;若在上述加热或不加热两种条件下得到等量的C单质,反应中转移的电子数之比为 。
28.(14分)瑞典皇家科学院2007年10月10日宣布,将本年度诺贝尔化学奖授予德国马普学会弗里茨一哈勃研究所的格哈德·埃特尔教授,以表彰他在固体表面化学过程研究领域做出开拓性成就。格哈德·埃特尔的重要贡献之一是对哈伯一博施法合氨反应催化机理的研究。格哈德·埃特尔建立的某温度下合成氨反应机理的各步反应的能量变化如图所示,图中的能量单位为kJ·mol-1。(注:图中“吸表示在催化剂表面的吸附)
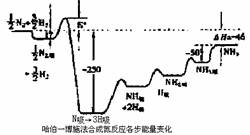
请回答下列问题:
(1)在合成氨反应中,决定反应速率的最主要的步骤是 (填字母)
A.氮分子解离为氢原子
B.氮原子的解离吸附
C.氢分子解离为氢原子
D.氨的解离吸附
(2)合成氨反应的机理为(用化学方程式表示)
① ;
②N2  N2吸
N2吸  2N吸;
2N吸;
③ ;
④NH吸+H吸  NH3吸
NH3吸
⑤NH2吸+H吸 NH3吸
NH3吸  NH3
NH3
(3)某温度下合成氨反应的热化学方程式为 ;
(4)某温度下,合成氨反应Ke=3.0×103(mol·L-1)-2,该温度下,在体积恒定为10L的四个密闭容器中分别充入;(A)10mol、30mol H2和20molNH3(B)10molN2和30molH2(C)20molN2和60molH2(D)10molN2和28molH2(E)0.1molN2、0.3molH2和20MolNH3,则反应达到平衡后,N2的转化率最大的是 (填字母)。
(5)合成氨工业生产中所用的α-Fe催化剂的主要成分是FeO、Fe2O3,当催化剂中Fe3+与Fe3+的物质的量之比为1:2时,其催化剂活性最高,以Fe2O3为原料制备上述催化剂,可向其中加入适量炭粉。发生如下反应:2Fe2O3+C=4FeO+CO2,为制得该种活性最高的催化剂,应向480gFe2O3粉末加入炭粉的质量为 g.
15.含有ag硝酸的稀溶液跟b g铁恰好反应,铁全部溶解,生成NO,已知有a/4g硝酸被还原,则a:b可能是 ( )
①3:1 ②3:2 ③4:1 ④9:2
A.① B.④ C.①③④ D.①④
|
[必做部分]
14.在一定条件下,一固定容积的密闭容器中发生如下反应:2NO2(g) O2(g)+2NO(g);△H>0达到平衡。当改变其中一个条件X,Y随X的变化符合图中曲线的是 ( )
O2(g)+2NO(g);△H>0达到平衡。当改变其中一个条件X,Y随X的变化符合图中曲线的是 ( )
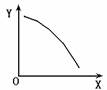
A.当X表示温度时,Y表示NO2的物质的量
B.当X表示催化剂时,Y表示NO2的转化率
C.当X表示反应时间时,Y表示混合气体的密度
D.当X表示NO2的物质的量时,Y表示O2的物质的量
13.在25℃时,将pH=11的NaOH溶液与pH=3的CH3COOH溶液等体积混合后,下列关系式中正确的是 ( )
A.c(Na+)=c(CH3COOH)+c(CH3COO-)
B.c(H+)=c(CH3COO-)+c(OH-)
C.c(Na+)> c(CH3COO-)> c(OH-)> c(H+)
D.c(CH3COO-)> c(Na+)> c(H+)> c(OH-)
12.下列叙述正确的是 ( )
A.78gNa2O2与水蒸气充分反应,转移的电子数为2NA(NA为阿伏加德罗常数的值)
B.常温下,将pH=1的HAc溶液稀释100倍,则稀释后溶液的pH>3
C.14C和14N的质量数相等,化学性质几乎完全相同
D.用试管夹从试管底部由下往上夹住距试管口约1/3处,手持试管夹长柄末端,进行加热
11.下列叙述正确的是 ( )
A.非金属元素之间不能形成离子化合物
B.两种元素组成的分子中一定只含有极性键
C.不同元素的核素质子数不一定相等,但中子数可能相等
D.质子数相等、中子数不等的微粒一定是同一元素的不同核素
9.2008年北京奥运会主体育场“鸟巢”和游泳馆“水立方”是在国内首次采用的膜结构建筑,以钢材为支架,覆盖ETFE薄膜。ETFE是乙烯和四氟乙烯的共聚物,是一种轻质透明的新材料。下列说法不正确的是 ( )
A.ETFE是一种可焊接的材料 B.ETFE极易分解符合环保要求
C.ETFE韧性好、拉伸强度高 D.ETFE比玻璃轻、发全系数高
|
A.相同条件下等质量的正丁烷燃烧放出的热量大于异丁烷,则可推知正丁烷的稳定性大于异丁烷
B.纯碱溶液能去油污与纯碱的水解无关
C.甲烷、乙酸、乙醇都能发生取代反应
D.蛋白质溶液加盐后都发生变性
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com