
8.下列物质性质的变化规律与分子间作用力有关的是 ( )
A.HF、HCI、HBr、HI的热稳定性依次减弱
B.碳化硅、晶体硅的熔、沸点很高
C.NaF、NaCI、NaBr、NaI的熔点依次降低
D.F2、CI2、Br2、I2的熔、沸点逐渐升高
7.下列过程中,共价键被破坏的是 ( )
A.碘升华 B.溴蒸汽被木炭吸附 C.HaCI溶于水 D.HCI气体溶于水
6.下列各组中,元素的电负性递增的是
A.Na K Rb B.N B Be C.O S Se D.Na P CI
5.下列叙述中正确的是 ( )
A.在离子晶体中不可能存在非极性键
B.在共价化合物的分子晶体中不可能存在离子键
C.全由非金属元素组成的化合物一定是共价化合物
D.直接由原子构成的晶体一定是原子晶体
4.下列化学式能真实表示物质分子组成的是 ( )
A.NaOH B.SO3 C.CsCI D.SiO2
3.Rm+与Xn-具有相同的电子层结构,则微粒半径 ( )
A.前者大于后者 B.前者小于后者
C.前者等于后者 D.大小比较不能确定
2.以下能级符号不正确的是 ( )
A.3s B.3p C.3d D.3f
1.在物质结构研究的历史上,首先提出原子结构有核模型的科学家是 ( )A.汤姆生 B.玻尔 C.卢瑟福 D.普朗克
29.(16分)根据反应框图填空,已知反应1~5均为工业生产及应用中常见反应,其中B、G、I、J、L均为常见单质,其中B、J、L为气体,C为红棕色粉末状固体。
A是工业生产中重要的矿石原料的主要成分,其相对分子质量为120.
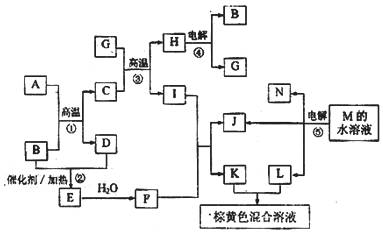
(1)写出A、B的化学方程式A ______________;B______________。
(2)写出下列化学反应方程式
反应③的化学方程式___________________________________。
反应⑤的离子方程式___________________________________。
(3)工业生产中,由E转化F的反应是在(设备)中进行的,并常用________________
来吸收E,优点是__________________________
(4)写出K与L反应的离子方程式___________________________
28.(14分)乙烯和乙烷混合气体共a mol,与b mol,的氧气共存于一密闭的容器中,点燃后充分反应,乙烯和乙烷全部消耗完,得到CO和CO2的混合气体和45水。试求:
(1)CO和CO2混合气体的物质的量=________,生成的水的物质的量=_________。
(2)当=1时,乙烯和乙烷的物质的量之比n(乙烯)n(乙烷)=_______________。
(3)当=1时,且反应后CO和CO2混合气体的物质的量为反应前氧的2/3时,则b=
;得到的CO和CO2的物质的量之比n(CO) : n(CO2)=_________________.
(4)的取值范围是_________________;的取值范围是________________
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com