
3.《科学》杂志评出某年10大科技突破,其中“火星上‘找’到水的影子”名列第一。下列关于水的说法中正确的是
A.水的电离过程是放热的过程
B.盐的水解一定能促进水的电离
C.催化剂能提高水分解的转化率
D.金属的电化腐蚀与水无关
1.根据热化学方程式(在101kPa时):S(s)+O2(g)=SO2(g);△H=-297.23kJ/mol分析下列说法中不正确的是
A.S的燃烧热为△H=-297.23kJ/mol
B.S(s)+O2(g)=SO2(g)放出的热量大于297.23kJ
C.S(s)+O2(g)=SO2(g)放出的热量小于297.23kJ
D.形成1mo1 SO2的化学键释放的总能量大于断裂1mo1 S(s)和1mo1 O2(g)的化学键所吸收的总能量
33.(8分)[化学--有机化学基础]
根据图示回答下列问题:
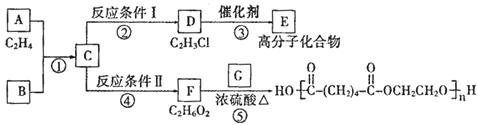
(1)写出结构简式:E____________________,G______________________;
(2)写出反应类型:①___________________,⑤______________________;
(3)写出化学方程式:②_________________,④______________________。
32.(8分)[化学--物质结构与性质]
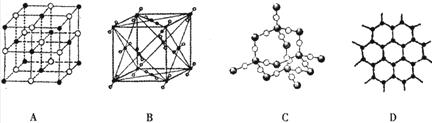
化合物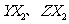 中X、Y、Z都是前三周期元素,X与Y同周期,Y与Z同主族,Y元素的最外层中P轨道上的电子数等于前一电子层电子总数,X原子最外层的P轨道中有一个轨道填充了2个电子。则
中X、Y、Z都是前三周期元素,X与Y同周期,Y与Z同主族,Y元素的最外层中P轨道上的电子数等于前一电子层电子总数,X原子最外层的P轨道中有一个轨道填充了2个电子。则
(1)X原子的电子排布式是______________________,Y源自的价层电子轨道表达式是_____________________;
(2)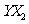 的分子构型是_____________,一个
的分子构型是_____________,一个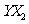 的熔沸点比
的熔沸点比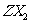 _________,(选填“高”或“低”),理由是_________________________________________________________;
_________,(选填“高”或“低”),理由是_________________________________________________________;
(3) 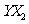 分子中,Y原子的杂化类型是_________________,一个
分子中,Y原子的杂化类型是_________________,一个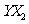 键分子中含____个
键分子中含____个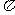 键。
键。
(4)下图表示一些晶体的结构(晶胞),其中代表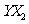 的是____________(填序号)。
的是____________(填序号)。
31.(8分)[化学--化学与技术]
亚氯酸钠(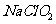 )是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂的漂白与杀菌。以下是过氧化氢法生产亚氯酸钠的工艺流程图:
)是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂的漂白与杀菌。以下是过氧化氢法生产亚氯酸钠的工艺流程图:
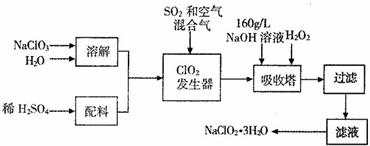
已知:
①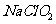 的溶解度随温度升高而增大,适当条件下可结晶析出
的溶解度随温度升高而增大,适当条件下可结晶析出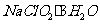 ;
;
②纯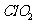 易分解爆炸,一般用稀有气体或空气稀释到10%以下。
易分解爆炸,一般用稀有气体或空气稀释到10%以下。
(1)发生器中鼓入空气的作用可能是________________________________;
(2)吸收塔内发生反应的化学方程式为______________________________;吸收塔内的温度不能超过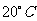 ,其目的是防止
,其目的是防止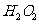 分解,写出
分解,写出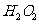 分解的化学方程式____________________________________;
分解的化学方程式____________________________________;
(3)在碱性溶液中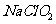 比较稳定,所以吸收塔中应维持
比较稳定,所以吸收塔中应维持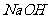 稍过量,判断
稍过量,判断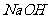 是否过量的简单实验方法是_________________________________;
是否过量的简单实验方法是_________________________________;
(4)从滤液中得到NaClO2·3H2O粗晶体的实验操作依次是_____________________。
30.(16分)
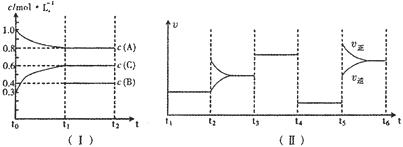
向一定体积的密闭容器中加入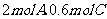 和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如图I所示,其中
和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如图I所示,其中 阶段
阶段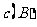 未画出。图Ⅱ为
未画出。图Ⅱ为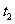 时刻后改变反应条件,化学反应速率随时间变化的情况,四个阶段改变的条件均不相同,每个阶段只改变浓度、温度、压强、催化剂中的一个条件,其中
时刻后改变反应条件,化学反应速率随时间变化的情况,四个阶段改变的条件均不相同,每个阶段只改变浓度、温度、压强、催化剂中的一个条件,其中 阶段为使用催化剂。
阶段为使用催化剂。
请回答下列问题:
(1)若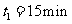 ,则
,则 阶段以C物质的浓度变化表示的反应速率为_________;
阶段以C物质的浓度变化表示的反应速率为_________;
(2) 阶段改变的条件为___________,B的起始物质的量浓度为______________。各阶段平衡时对应的平衡常数如下表所示:
阶段改变的条件为___________,B的起始物质的量浓度为______________。各阶段平衡时对应的平衡常数如下表所示:
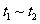
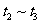
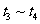

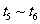
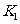
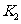
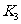
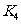
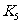
则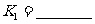 (保留两位小数),
(保留两位小数),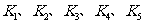 之间的关系为____________(用“>”、“<”或“=”连接);
之间的关系为____________(用“>”、“<”或“=”连接);
(3) 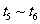 阶段保持容器内温度不变,若A的物质的量共变化了
阶段保持容器内温度不变,若A的物质的量共变化了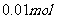 ,而此过程中容器与外界的热交换总量为
,而此过程中容器与外界的热交换总量为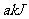 ,写出此温度下该反应的热化学方程式__________;
,写出此温度下该反应的热化学方程式__________;
(4)在相同条件下,若起始时容器中加入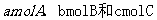 ,要达到
,要达到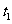 时刻同样的平衡,
时刻同样的平衡,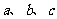 要满足的条件为________________。
要满足的条件为________________。
[选做部分]
共8个小题,考生从中选择2个物理题、1个化学题和1个生物题作答。
29.(13分)
短周期常见元素形成的单质或化合物A、B、C、D、E转化关系如下图所示(反应条件已略去):
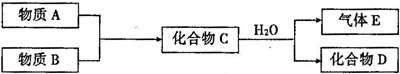
物质A与物质B之间的反应不在溶液中进行,E可能与A、B两种物质中的某种相同请回答下列有关问题:
(1)若C是离子化合物,D是一种强碱,则C物质的电子式为___________________;
(2)若C与水发生复分解反应,E的水溶液呈弱酸性,D既能与强酸反应又能与强碱反应。
①D与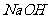 溶液反应的离子方程式为___________________________________;
溶液反应的离子方程式为___________________________________;
②E与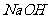 (物质的量之比为l:2)反应后的溶液中,所有离子浓度之间的关系为_______________________________________(列等式)。
(物质的量之比为l:2)反应后的溶液中,所有离子浓度之间的关系为_______________________________________(列等式)。
(3)若C是一种气体,D是一种强酸。
①A与B反应的化学方程式为_____________________________________________
②组成D的各元素的原子半径由大到小的顺序为____________________________。
28.(13分)
菠菜营养丰富,素有“蔬菜之王”之称,在营养价值上是一种高效的补铁剂。长期以来民间流传着“菠菜不能与豆腐同食”、“菠菜根比菠菜茎叶更有营养”等说法。某学校兴趣小组的同学拟通过实验探究以下问题:
①菠菜是否含有丰富的铁?
②菠菜是否含有草酸类物质?
③菠菜根中铁的含量是否比菠菜茎和叶的高?
该同学通过上网查询,获得以下资料:草酸又名乙二酸,其酸性比乙酸稍强,草酸及其盐具有较强的还原性,其中草酸钙不溶于水。
他们设计的实验步骤如下:
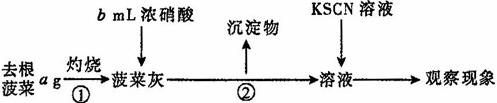
Ⅰ.
Ⅱ.取菠菜根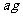 使用相同仪器、试剂,重复I中实验,观察实验现象。
使用相同仪器、试剂,重复I中实验,观察实验现象。
Ⅲ.将菠菜在少量开水中煮沸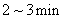 ,冷却后滤去菠菜,得滤液。向滤液中加入足量
,冷却后滤去菠菜,得滤液。向滤液中加入足量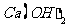 溶液,然后再加入足量试剂X,观察现象。
溶液,然后再加入足量试剂X,观察现象。
请回答以下问题:
(1)操作①中使用的仪器除三角架、酒精灯、玻璃棒外还需要____________操作②的名称是________________;
(2)可以说明菠菜根中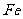 元素含量要比菠菜茎叶中多的现象是__________________;
元素含量要比菠菜茎叶中多的现象是__________________;
(3)菠菜中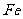 的是+2价还是+3价?_______________________;
的是+2价还是+3价?_______________________;
(4)通过步骤Ⅲ可以确定菠菜中含有草酸类物质。由于滤液中含有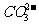 ,故需加入试剂X排除
,故需加入试剂X排除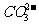 的干扰。则X是_____________(写化学式),加入试剂X后观察到的现象是_________________。
的干扰。则X是_____________(写化学式),加入试剂X后观察到的现象是_________________。
15.由短周期元素构成的某离子化合物X中,一个阳离子和一个阴离子核外电子数之和为20。则有关X的下列说法正确的是 ( )
A.X中阳离子和阴离子个数不一定相等
B.X中一定有离子键,一定不含共价键
C.若X只含两种元素,则两种元素可在同一周期也可在同一主族
D.X中阳离子半径一定大于阴离子半径
第Ⅱ卷(必做120分+选做32分,共152分)
|
第Ⅱ卷共16个题。其中23-30题为必做部分,考生可用黑色签字笔、钢笔或圆珠笔直接将答案写在答题纸上;31-38题为选做部分,考生必须从中选择2个物理、1个化学和1个生物题作答,多选、多做不计分。选做的题目,考生须用黑色签字笔、钢笔或圆珠笔写在答题纸上规定的位置,在试题卷上答题无效。
[必做部分]
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com