
12.实验室有一瓶久置的白色K2SO3粉末,为确定其是否被氧化及其成分,元素分析表明粉末中K和S元素的质量比为39 :16,下列结论正确的是
A.根据元素分析结果推测该粉末为纯净物
B.将粉末溶于水,加入氯化钡,有白色沉淀生成,证明原粉末是K2SO4
C.将粉末加入盐酸中,产生气泡,证明原粉末是K2SO3
D.将粉末溶于水,加入氯化钡和过量的盐酸,有白色沉淀和气泡生成 ,证明原粉末是K2SO4和K2SO3的混合物
11.X、Y是元素周期表ⅦA族中的两种元素,下列叙述中能说明X的非金属性比Y强的是
A.X原子的电子层数比Y原子的电子层数多
B.X的气态氢化物比Y的气态氢化物稳定
C.X的氢化物的沸点比Y的氢化物的沸点低
D.用石墨做电极电解等物质的量浓度的NaX和NaY的混合溶液,Y -先被氧化
10.新鲜水果、蔬菜、乳制品中富含的维生素C具有明显的抗衰老作用,但很容易被空气氧化。某课外小组利用碘滴定法测某橙汁中维生素C的含量,其化学方程式为:
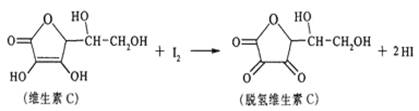
下列说法不正确的是
A.上述反应为取代反应 B.滴定时可用淀粉溶液作指示剂
C.滴定时应缓慢并轻轻的振荡锥形瓶 D.脱氢维生素C的分子式为C6H6O6
9.下列除去杂质的实验方法不正确的是
A.除去CO2中少量HCl气体:通过饱和NaHCO3溶液后再干燥气体
B.除去Na2CO3固体中少量NaHCO3:置于坩埚中加热
C.除去苯中溶有的少量苯酚: 加入适量浓溴水反应后过滤
D.除去FeCl3酸性溶液中少量的FeCl2:通入稍过量的Cl2
8.把NaHCO3和NaOH的混合物放在密闭容器中加热。关于混合物加热前后消耗盐酸的物质的量.下列判断正确的是
A.加热前消耗的多 B.加热后消耗的多
C.加热前后一样多 D.当NaOH适量时才会一样多
7.同温同压下,等体积的两容器内分别充满14N18O、和13C18O气体,下列说法正确的是
A.所含分子数和质量均不相同 B.含有相同的分子数和电子数
C.含有相同的质子数和中子数 D.含有相同的分子数和中子数
6.将等体积的硫酸铝、硫酸锌、硫酸钠溶液分别与足量的氯化钡溶液反应,若生成的硫酸钡沉淀的质量相等,则三种硫酸盐溶液中SO42-的物质的量浓度比为
A.1︰2︰3 B.1︰1︰1 C.3︰3︰1 D.1︰3︰3
5.现有四组物质的溶液,仅用酚酞试液及同组物质之间相互反应就能鉴别出来的是
A.NaOH Ba(OH)2 HCl B.NaOH HCl NaCl
C.NaOH HC1 HNO3 D.H2SO4 NaCl Na2SO4
4.在短周期元素中,若某元素原子的最外层电子数与其电子层数相等,则符合条件的元素种数为
A.1种 B.2种 C.3种 D.4种
3.2006年,科学家发明了一种能够给电子设备提供动力的生物燃料电池。该电池的两个涂覆着催化剂酶的电极处于充满空气和少量氢气的玻璃槽中,总反应为:2H2 +O2=2H2O ,由于气体可以混合从而省去了昂贵的燃料隔离膜,其工作原理如图。下列说法不正确的是
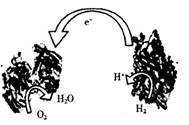
A.右边电极为该电池的负极
B.该电池可以在高温环境下使用
C.该装置为化学能转变为电能的装置
D.该电池正极发生的是还原反应
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com