
4.碱金属与卤素所形成的化合物大都具有的性质是( )
①低熔点 ②水溶液不能导电 ③熔融状态能导电 ④晶体能导电
⑤能溶于水 ⑥易溶于苯
A.①②③ B.③⑤ C.④⑤ D.③④⑤⑥
3.电子工业制造光电管时,需要一种经强光照射就失去电子从而接通电路的材料。制造这种材料的物质属于( )
A.ⅦA族元素 B.聚乙烯 C.ⅠA族元素 D.二氧化硅
2.“摇摇冰”是一种即用即冷的饮料,吸食时将饮料罐隔离层中的化学物质和水混合摇动即会制冷。其化学原理是( )
A.生石灰与水反应放出大量的热 B.硝酸铵溶于水能吸热
C.硝酸铵溶于水呈酸性 D.生石灰溶于水呈碱性
1.查阅资料发现,金属钠不仅能跟氧气和水反应,还能跟多种其它物质发生反应,其中包括与酒精在常温下反应。要研究金属钠跟酒精反应的性质以及它与水反应的异同点,下列的研究方法中没有用到的是
A.实验法 B.观察法 C.分类法 D.比较法
29、(10分)Al和Si、Ge和As在元素周期表金属和非金属过渡位置上,在其单质和化合物在建筑业、电子工业和石油化工等方面应用广泛。请回答下列问题:
(1)As的价层电子构型为
(2)AlCl3 是化工生产中的常用催化剂,熔点为192.6℃,熔融状态以二聚体Al2Cl6形式存在,其中铝原子与氯原子的成键类型是
(3)超高导热绝缘耐高温纳米氮化铝(AlN)在绝缘材料中的应用广泛,AlN晶体与金刚石类似,每个Al原子与 个N原子相连,与同一个Al原子相连的N原子构成的空间构型为 。在四大晶体类型中,AlN属于 晶体。
(4)Si和C同主族,Si、C和O成键情况如下:
|
|
C-O |
C=O |
Si-O |
Si=O |
|
键能/kJ·mol-1 |
360 |
803 |
464 |
640 |
在C和O之间可以形成双键形成CO2分子,而Si和O则不能和碳那样形成有限分子原因是
。
(5)SiCl4(l)常用作烟雾剂,原因Si存在3d轨道,能同H2O(l)配位而剧烈水解,再潮湿的空气中发烟,试用化学方程式表示其原理
28.(10分)奥美拉唑(Omeprazole)是基于2005年诺贝尔医学奖成果研制的药物,该药物对幽门螺旋杆菌引起的胃及十二指肠溃疡根治率最高。奥美拉唑的合成路线如下(Me表示甲基):
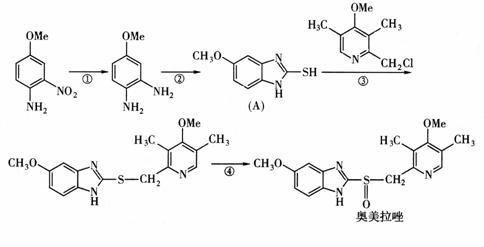
试回答下列问题:
(1)奥美拉唑的分子式是: 。
(2)指出下列反应的类型:① ;③ 。
(3)反应②是与一种无机小分子在氢氧化锂催化下发生的反应,二者各一分子反应在得到A的同时还得到一分子的硫化氢,则该无机小分子的化学式为: 。
(4)反应④是用液态氧化剂氧化而发生的反应,除生成奥美拉唑外还生成水,请写出④的化学反应方程式: 。
(5)根据结构判断奥美拉唑可能发生的化学反应是: 。
A.与氢氧化钠发生水解反应 B.能与氯气发生加成反应
C.与乙酸发生酯化反应 D.能使酸性高锰酸钾溶液褪色
27.(9分)萨罗(Salol)是一种消毒剂,它的分子模型如图所示(图中球与球之间的连线代表化学键,如单键、双键):
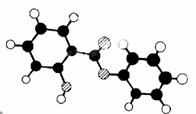
(1)根据上图模型写出萨罗的结构简式:_________________ ______。
(2)写出萨罗分子结构中含有官能团的名称: 。
(3)萨罗经水解、分离、提纯可得到纯净的苯酚和水杨酸。请写出其水解方程式:
。
(4)写出同时符合下列四种条件的水杨酸的同分异构体共有_ ______种。
①含有苯环;②能发生银镜反应,不能发生水解反应;③在稀NaOH溶液中,1mol该同分异构体能与2mol NaOH发生反应;④只能生成两种一氯代产物。
(5)从(4)确定的同分异构体中任选一种,指定为下列框图中的A。
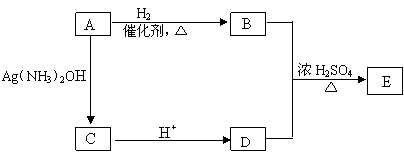

写出下列反应的化学方程式:
B+D→E: ;
该反应属于 反应。
26.(12分)辉钼矿(MoS2)是钼最重要的矿物。图26-1是辉钼矿多层焙烧炉的示意图,其中1,2,3,…是炉层编号。580,600,610,…是各炉层的温度(℃)。下图2给出了各炉层的固体物料的摩尔百分组成。
已知:MoS2焙烧生成1molMoO3的反应热为△H1=-1011KJ/mol,MoO2氧化生成1molMoO3的反应热为△H2=-154KJ/mol。试回答:
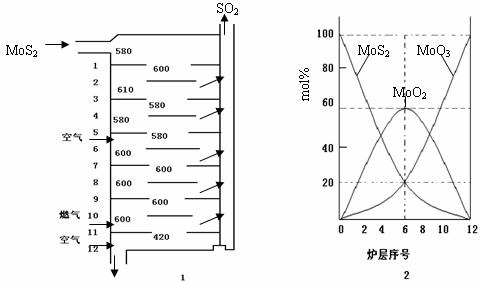
(1)辉钼矿焙烧生成MoO3的反应中被氧化的元素是: ;指出辉钼矿焙烧生成的尾气对环境的一种危害: 。
(2)第6炉层存在的固体物质分别是: ;它们的物质的量之比是: 。
(3)辉钼矿焙烧生成MoO3的热化学反应方程式是: 。
(4)图2表明,中间炉层(4-6)可能存在一种“固体+固体→固体+…”的反应,请写出该反应的化学方程式: 。
(5)通过(3)和(4)你能解释为什么中间炉层(4-6)的炉温比上下炉层的炉温低吗? 。
25.(8分)与化学平衡类似,电离平衡的平衡常数,叫做电离常数(用K表示,K只与温度有关)。下表是几种常见弱酸的电离平衡常数(25℃)。
|
酸 |
电离方程式
|
电离平衡常数K |
|
CH3COOH |
CH3COOH CH3COO-+H+ CH3COO-+H+ |
1.76×10-5 |
|
H2CO3 |
H2CO3 H++HCO3- H++HCO3-HCO3-  H++CO32- H++CO32- |
K1==4.31×10-7 K2==5.61×10-11 |
|
H3PO4 |
H3PO4 H++H2PO4― - H++H2PO4― -H2PO4―  H++HPO42― H++HPO42― HPO42―  H++PO43- H++PO43- |
K1==7.1×10-3 K2==6.3×10-8 K3==4.2×10-13 |
回答下列各题:
(1)温度升高时, (填“促进”或“抑制”)弱酸的电离,K值 (填“增大”、“减小”或“不变”)。
(2)在温度相同时,各弱酸的K值不同,那么K值的大小与酸性的相对强弱关系是
。
(3)若把CH3COOH、H2CO3、HCO3-、H3PO4、H2PO4―、HPO42-都看作是酸,则它们酸性强弱顺序是_________________________________________。
(4)若醋酸的起始浓度为0.010mol/L,则平衡时溶液的pH是多少?(写出计算过程,结果以对数形式表示)
24.(10分)制取纯净CuCl2·2H2O的生产过程是:
(1)用粗CuO(含少量铁)溶解在足量的稀盐酸里加热、过滤,得到CuCl2(含FeCl2)的溶液,经测定,溶液的PH值为3。
(2)对(1)的溶液按下列步骤进行提纯:

 已知:①可做氧化剂的物质有(A)KMnO4
(B)K2Cr2O7
(C)H2O2
(D)NaClO
已知:①可做氧化剂的物质有(A)KMnO4
(B)K2Cr2O7
(C)H2O2
(D)NaClO
②Cu2+ 、Fe2+在PH值为4~5时不水解,而Fe3+却几乎全部水解。
试回答:
(1)加入的氧化剂X是(答编号): ;
加入X的作用是: ;
反应的离子方程式是: 。
(2)物质Y是 ;沉淀Z是 。加入Y能形成沉淀Z的原因是: 。
(3)分离出沉淀Z,并将溶液III蒸发欲获得晶体CuCl2·2H2O。采取什么措施才能顺利得到晶体CuCl2·2H2O?______________________ 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com