
6.在F、P、S三种元素中,每种元素都有某些方面区别于其它两种元素;若从中选出氟元素,选择的理由是 ( )
A.单质固态时属于分子晶体
B.一定条件下,能与氢气发生化合反应
C.最高价氧化物对应的水化物是强酸
D.单质与冷水反应非常剧烈
29.(15分)有机物A是一种镇痛解热药品,其结构简式为:
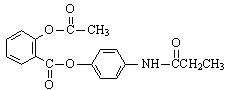
由它可衍生出一系列物质,有关变化如图:
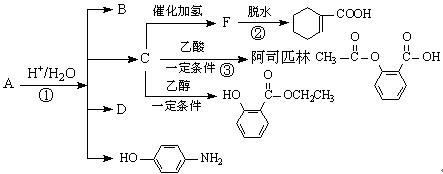
(1)①、③反应类型分别是_______、__________;B和D的关系是_____________(填同种物质或同系物或同分异构体)。
(2)写出反应②的化学方程式:___________________________________________;
(3)写出C与NaHCO3溶液反应的化学方程式____________________________;
(4)1molA在氢氧化钠溶液中水解,最多消耗氢氧化钠_____________mol;
(5)能与FeCl3溶液发生显色反应,且属于酯类的C的同分异构体有多种,写出其中一种的结构简式______________________。
28.(15分)现有一定量含有Na2O杂质的Na2O2试样,用下图的实验装置测定Na2O2试样的纯度。(可供选用的反应物只有CaCO3固体、6mol/L盐酸、6mol/L硫酸和蒸馏水)
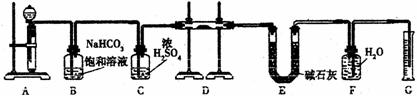
回答下列问题:
(1)实验前必须检查装置的气密性。仪器连接好后,在__________中加适量的水,关闭A中分液漏斗阀门后微热试管,若看到_________________说明装置气密性好。
(2)装置A中液体试剂选用盐酸而不用硫酸.理由是_______________________。
(3)装置B的作用是________________ ______ _______________;
装置C的作用是____________________________________ _________ _;
装置E中碱石灰的作用是____________________________ ______________。
(4)装置D中发生反应的化学方程式是:________________________________________
(5)若开始时测得样品的质量为2.0g,反应结束后测得气体体积为224mL(标准状况),则Na2O2试样的纯度为______________。
27.(15分)某待测液中可能含有Fe2+、Fe3+、Ag+、Al3+、Ba2+、Ca2+、NH4+等离子,进行如下实验(所加酸、碱、氨水、溴水均过量)。
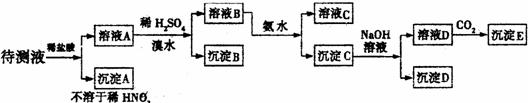
根据实验结果可以肯定上述___________离子一定存在。请填写下列物质的化学式:
(1)沉淀A: 。
(2)沉淀C: 。
(3)沉淀D: 。
(4)沉淀E: 。
26.(15分)A、B、C、D、E都是元素周期表中前20号元素,其原子序数依次增大。B、C、D同周期,A、D同主族,E和其它元素既不在同周期也不在同主族。B、C、D的最高价氧化物的水化物均能互相发生反应生成盐和水。化合物EA2中A-的原子核外K电子层和L电子层上的电子数之比为1∶4。
(1)A、E元素符号分别为________、________,D元素的原子结构示意图是_______。
(2)A、B、C、D四种元素的原子半径由小到大的顺序为________(用元素符号表示)。
(3)A和D的氢化物中,前者沸点较高,原因是_____________。
(4)C、D形成的化合物水溶液显________性(填“酸”或“碱”),原因是(用离子方程式表示):_________________________________。
13.下图为某化学反应的速率与时间的关系示意图,在t1时刻升高温度或者增大压强,速率的变化都符合示意图的反应是( )

A.2SO2(g)+O2(g)  2SO3(g);△H<0
2SO3(g);△H<0
B.4NH3(g)+5O2(g)  NO(g)+6H2O(g);△H<0
NO(g)+6H2O(g);△H<0
C.H2(g)+I2(g)  2HI(g);△H>0
2HI(g);△H>0
D.C(s)+H2O(g)  CO(g)+H2(g);△H>0
CO(g)+H2(g);△H>0
第Ⅱ卷(非选择题共10题共174分)
12.2008年北京将举办第二十九届奥林匹克夏季运动会,如下图酷似奥林匹克旗中的五环的一种有机物被称之为奥林匹克烃,下列说法正确的是 ( )
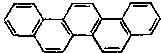
A.该有机物属于芳香族化合物,是苯的同系物
B.该有机物是只含非极性键的非极性分子
C.该有机物的一氯代物只有一种
D.该有机物完全燃烧生成H2O的物质的量小于CO2的物质的量
11.下列离子方程式正确的是 ( )
A.铁片溶于稀硫酸:2Fe+6H+=2Fe3+ +3H2↑
B.在小苏打溶液中加入醋酸:HCO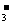 +H+=C02↑+H2O
+H+=C02↑+H2O
C.在氯化铝溶液中加入过量氨水:Al3+ +3NH3·H2O=A1(OH)3↓+3NH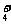
D.钠与水反应:Na+2H2O =Na+ +2OH-+H2↑
9.室温下,下列四种混合溶液中pH最大的是 ( )
A.0.1mol·L-1CH3COOH溶液与0.1mol·L-1NaOH溶液等体积混合
B.0.1mol·L-1H2S04溶液与0.1mol·L-1NaOH溶液等体积混合
C.pH=2的CH3COOH溶液与pH=12的NaOH溶液等体积混合
D.pH=2的H2SO4溶液与pH=12的NaOH溶液等体积混合
|
A.标准状况下,22.4L CHCl3中含有的氯原子数目为3NA
B.0.5mol重水D2O中含有共价键数为NA
C.1mol氦气含有的原子数为2NA
D.足量的铜片与含4mol HNO3的浓硝酸充分反应生成的二氧化氮的分子数为2 NA
8.对于反应KMnO4+HCl→KCl+MnCl2+Cl2+H2O(未配平),若有0.1 molKMnO4参加反应,下列说法正确的是 ( )
A.转移电子0.5mol B.生成Cl2 0.5 mol
C.被氧化的HCl为1.6mol D.Cl2是还原产物
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com