
28.(18分)据报道,自2003年以来,一种名为苹果醋(ACV)浓缩饮料风靡美国。苹果醋是由苹果发酵而成的酸性饮品,具有解毒、降脂、减肥和止泻等功效。苹果醋X的分子式为C4H6O5。为确定该有机物的结构式特进行如下实验(见下表)
|
实验步骤 |
实验内容 |
|
① |
X与足量的金属钠反应产生氢气。 |
|
② |
X与醇或羧酸在浓硫酸加热条件下均能生成有水果香味的有机物。 |
|
③ |
一定条件下X的分子内脱水产物(直链状化合物)可与溴水发生加成反应 |
|
④ |
33.5 g X与100 mL的5 mol·L-1氢氧化钠溶液恰好完全中和。 |
请根据题目要求填写下列空格:
(1)X的结构简式为:_____________________,其同类同分异构体的结构简式有: _______________________,____________________________。
(2)写出X发生反应的化学方程式:①______________________________,
③ 。
(3)在一定条件下有机物X可发生化学反应的类型有(填序号)_____________。
A.水解反应 B.取代反应 C.加成反应 D.消去反应
E.加聚反应 F.中和反应
(4)写出X在浓硫酸加热条件下发生反应所得六元环状化合物的结构简式为:_____________________________________。
27. (12分)t℃时,将2molSO2和1molO2通入体积为2L的恒温恒容密闭容器中,发生如下反应:2SO2(g)+O2(g) 2SO3(g),△H=-196.6kJ/mol.
2min时反应达到化学平衡,此时测得反应物O2还剩余0.8mol,请填写下列空白:
(12分)t℃时,将2molSO2和1molO2通入体积为2L的恒温恒容密闭容器中,发生如下反应:2SO2(g)+O2(g) 2SO3(g),△H=-196.6kJ/mol.
2min时反应达到化学平衡,此时测得反应物O2还剩余0.8mol,请填写下列空白:
(1)从反应开始到达化学平衡,生成SO3的平均反应速率为 ;平衡时SO2转化率为 。
(2)下列叙述能证明该反应已达到化学平衡状态的是(填标号,下同) 。
A.容器内压强不再发生变化
B.SO2的体积分数不再发生变化
C.容器内气体原子总数不再发生变化
D.相同时间内消耗2nmolSO2的同时消耗nmolO2
E.相同时间内消耗2nmolSO2的同时生成nmolO2
F.混合气体密度不再变化
(3)反应达到化学平衡后,以下操作将引起平衡向正反方向移动并能提高SO2转化率的是 。
A.向容器中通入少量O2
B.向容器中通入少量SO2
C.使用催化剂
D.降低温度
E.向容器中通入少量氦气(已知:氦气和SO2、O2、SO3都不发生反应)
(4)t2℃时,若将物质的量之比n(SO2):n(O2)=1:1的混合气体通入一个恒温恒压的密闭容器中,反应达到平衡时,混合气体体积减少了20%。SO2的转化率为 。
26.(16分)A、B、C、D、E五种短周期元素,核电荷数依次增加,其中A与D同族,C与E同族。A的一种原子内无中子,B原子最外层电子数是内层电子数的2倍,一个C2-离子含10个电子。
(1)工业制取D单质的反应方程式是 。
(2)甲是由A、B、C三种元素组成的相对分子质量最小的物质,且可以发生银镜反应。甲的一种用途是 。由甲中的两种元素组成,且与甲等电子的物质的分子式是 ,该物质与C的单质在KOH溶液中形成电源的负极反应式为 。
(3)由A、B两种元素组成的非极性分子有多种,其中一个分子含4个原子的为乙,乙的电子式是 。已知乙的燃烧热为1300 kJ∕mol,乙燃烧热的热化学反应方程式是 。
(4)均由A、C、D、E四种元素组成的两种物质丙和丁在溶液中反应方程式是
。
(5)A与C形成一种物质戊,在酸性条件下,将少量戊加入淀粉KI溶液后,溶液显蓝色,反应的离子方程式是 。
13.
|

A.1L1mol/L的醋酸溶液中离子总数为2NA
B.0.5mol熔融的KHSO4中含有阳离子的数目为NA
C.0.4molNaCl晶体中含有右图所示的结构单元的数目为0.1NA
D.标准状况下,22.4LCH2Cl2和CHCl3 的混合物所含有分子数目为NA
第Ⅱ卷
12.某芳香族酯类化合物甲的分子式为C14H10O5,1mol甲水解后只生成一种产物乙,其物质的量为2mol,下列说法正确的是 ( )
A.符合上述条件的甲共有3种
B.1mol甲最多可以和3molNaOH反应
C.乙不能和溴水发生反应
D.2mol乙最多消耗1molNa2CO3
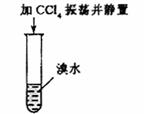
11.下列实验报告记录的实验现象正确的是


10.糖类、油脂和蛋白质都是人类必需的基本营养物质,下列关于它们的说法中不正确的是
|
A.淀粉、油脂和蛋白质都能发生水解反应
B.糖类、油脂和蛋白质都属于高分子化合物
C.人们可以利用电泳来分离某些氨基酸和蛋白质
D.可以利用丁达尔效应来鉴别葡萄糖和淀粉溶液
9.下列各组离子在指定溶液中一定能大量共存的是 ( )
①加入Al能放出H2的溶液中:Fe2+、Al3+、NO3-、Cl-、S2-
②使pH=11的溶液中:Na+、AlO2-、NO3-、S2-、SO
③由水电离的c(H+)=10-12mol·L-1的溶液中:Cl-、HCO3-、NO3-、NH4+、F-
④加入Mg能放出H2的溶液中:Mg2+、NH4+、Cl-、K+、SO
⑤使甲基橙变红的溶液中:Fe3+、NH4+、Cl-、K+、SO
A.①③④ B.①②④ C.②④⑤ D.①②⑤
8.下列有关比较中,大小顺序排列错误的是 ( )
A.热稳定性:PH3>H2S>HBr>NH3
B.物质的熔点:石英>食盐>冰>汞
C.结合质子的能力:CO32->CH3COOˉ>SO42-
D.分散系中分散质粒子的直径;Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液
7.现有物质的量浓度为0.1mol·L-1的下列5种物质的水溶液:
①HC1 ②H2SO4 ③CH3COOH ④NH4C1 ⑤NaOH
其水溶液中由水电离出的c(H+)的大小关系是 ( )
A.④>③>①=⑤>② B.①=②>③>④>⑤
C.③>①>②>④>⑤ D.③>④>①>⑤>②
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com