
9.下列说法正确的是
A.第二周期元素的第一电离能随原子序数递增依次增大
B.卤族元素中氟的电负性最大
C.CO2、SO2都是直线型的非极性分子
D.CH2=CH2分子中共有四个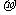 键和一个
键和一个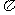 键
键
8.判断下列有关化学基本概念的依据正确的是
A.氧化还原反应:元素化合价是否变化
B.共价化合物:是否含有共价键
C.强弱电解质:溶液的导电能力大小
D.酸性氧化物:氧化物是否为非金属氧化物
7. 已知A、B、C、D、E是核电荷数依次增大的五种短周期元素,原子半径按D、E、B、C、A的顺序依次减小,B和E同主族,下列推断不正确的是
A.A、B、E一定在不同周期 B.D为第二周期
C.A、D可能在同一主族 D.C、D的单质可能化合为离子化合物
6.下列各组比较项目包含的数据关系中,前者比后者大的是
A.氨水与氯水中微粒种数 B.NH4+离子与 P4分子中的键角
C.C2H2与 C6H6分子中碳碳键键长 D.H2O2与 O2分子中氧氧键键能
5.下列分子中属于含有极性键的非极性分子,且分子中各原子最外层都满足8电子稳定结构的是
A.CH4 B.PC13 C.SiC14 D.XeF4
4.化学用语是学习化学的工具和基础。下列有关化这用语的使用正确的是
A.用食醋除去水壶内的水垢:CaCO3+2H+=Ca2++CO2↑+H2O
B.纯碱溶液呈碱性的原因是:CO32-+2H2O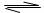 H2CO3+2OH-
H2CO3+2OH-
C.用铁作阳极,电解饱和食盐水的离子方程式:Fe+2H2O Fe(OH)2+H2↑
Fe(OH)2+H2↑
D.表示氢气燃烧灼热的热化学方程式为:2H2(g)+O2(g)=2H2O(1);
△H=-571.6KJ·mol-1
3.下列各组离子能在溶液中大量共存,在足量该溶液中加入少量Mg(OH)2固体,可以使Mg(OH)2固体溶解得到澄清溶液的是
A.Na+、NH4+、C1-、NO3- B.H+、Fe2+、C1-、NO3-
C.Na+、S2-、SO32-、SO42- D.K+、HCO3-、NO3-、A1O2-
2.下列叙述中正确的是
A.58.5克氯化钠晶体中约含6.02×1023个NaC1分子
B.在含6.02×1023个硅原子的二氧化硅晶体中含有4×6.02×1023个Si-O键
C.6.02×1023个甲基正离子(CH3+)所含的电子数为9×6.02×1023个
D.若N等于0.012kg12C所含的碳原子数,那么N也等于44克干冰(12C18O2)所含的二氧化碳分子数
1.2007年9月1日,经国务院批准,国家发改委、中宣部等十七个部委在人民大会堂举行“节能减排全民行动”启动仪式,要求在全国范围内形成全民节能减排氛围。下列有关做法不符合这一要求的是
A.将煤液化、气化,提高燃料的燃烧效率
B.在汽车上安装汽车尾气催化转化装置,使之发生如下反应:2CO+2NO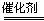 2CO2+N2
2CO2+N2
C.在大力推广乙醇汽油的同时,研究开发太阳能汽车和氢燃料电池汽车
D.在水力发电、火力发电、核能发电和风力发电中,要大力发展火力发电
29.(12分)NO很容易与许多分子迅速发生反应,科学家发现在生命体中会不断地产生NO,用于在细胞和细胞间传递信息;NO还参与心血管系统、免疫系统以及中枢和外围神经系统的调控。
(1)实验室用金属铜和稀硝酸制取NO的离子方程式
(2)NO是有毒气体,某学生为防止污染,用分液漏斗和烧杯装配了一套简易的、能随开随用、随关随停的NO气体发生装置,如图Ⅰ所示。
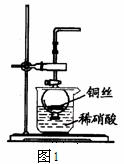
①实验室若没有铜丝,而只有小铜粒,在使用上述装置进行实验时,可用丝状材料包裹铜粒以代替铜丝进行实验,这丝状材料的成分可以是 (填选项编号)
(A)铁 (B)铝 (C)银 (D)玻璃 (E)聚丙烯塑料
②打开分液漏斗的活塞使反应进行,在分液漏斗中实际看到的气体是红棕色的,原因是 (填化学方程式)
(3)为证明铜丝与稀硝酸反应生成的确实是NO,某同学另设计了一套如图Ⅱ所示制取NO的装置。反应开始后,可以在U形管右端观察到无色的NO气体。

①长玻璃管的作用是 。
②让反应停止的操作方法及原因是
(4)以下收集NO气体的装置(见图Ⅲ,图在下页),合理的是 (填选项代号)

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com