
19.(9分)以下是工业上用软锰矿制备高锰酸钾的一种工艺流程。

(1)操作I的实验操作名称是 。
(2)上述流程中可以循环使用的物质有______________、______________(写化学式)。
(3)KMnO4稀溶液是一种常用的消毒剂。其消毒机理与下列物质相同的是______(填代号)。
A.84消毒液(NaClO溶液) B.双氧水 C.甲醛 D.75%酒精
(4)高锰酸钾保存在棕色试剂瓶,下列试剂保存不需要棕色试剂瓶的是_______(填代号)。
A.浓硝酸 B.硝酸银 C.新制氯水 D.烧碱
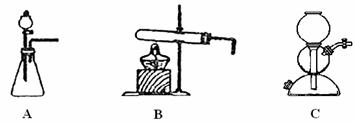
(5)该生产中需要纯净的CO2气体。若实验室要制备少量纯净的CO2所需试剂最好选择___ __(选填代号)。
A.石灰石 B.稀HCl C.稀H2SO4 D.纯碱
所需气体发生装置是_____________(选填代号)。
18.通过对实验现象的观察、分析推理得出正确的结论是化学学习的方法之一。对下列实验事实解释正确的是
|
|
现象 |
解释 |
|
A |
KI淀粉溶液中通入Cl2,溶液变蓝 |
Cl2能与淀粉发生显色反应 |
|
B |
浓HNO3在光照条件下变黄 |
浓HNO3不稳定,生成有色产物能溶于浓硝酸 |
|
C |
某溶液中加入硝酸酸化的氯化钡溶液,有白色沉淀生成 |
说明该溶液中含有SO42- |
|
D |
向盐酸中加入浓硫酸时产生白雾 |
说明浓硫酸具有脱水性 |
17.在一定条件下,可逆反应:N2+3H2  2NH3,DH<0,达到平衡时,当单独改变下列条件后,有关叙述错误的是
2NH3,DH<0,达到平衡时,当单独改变下列条件后,有关叙述错误的是
A.加催化剂V正、V逆都发生变化且变化的倍数相等
B.降温,V正、V逆都减小,且V正减小倍数大于V逆减小倍数
C.加压,V正、V逆都增大,且V正增大倍数大于V逆增大倍数
D.加入氩气,V正、V逆都增大,且V正增大倍数大于V逆增大倍数
16.镁及其化合物一般无毒(或低毒)、无污染,且镁原电池放电时电压高而平稳,使镁原电池越来越成为人们研制绿色原电池的关注焦点。其中一种镁原电池的反应为:
 ;在镁原电池放电时,下列说法错误的是
;在镁原电池放电时,下列说法错误的是
A.Mg2+向正极迁移 B.正极反应为:Mo3S4+2xe- = Mo3S42x-
C.Mo3S4发生氧化反应 D.负极反应为:xMg - 2xe- = xMg2+
15.下列各组离子在溶液中按括号内的物质的量之比混合,得到无色、碱性、澄清溶液的是
A.Na+、Al3+、Cl-、OH- (5:1:4:4) B.NH4+、Ba2+、OH-、Cl- (1:1:1:2)
C.Fe3+、Na+、Cl-、S2- (1:2:3:1) D.K+、H+、I-、HCO3- ( 1:1:1:1)
14.丙烯酸的结构简式为:CH2=CH-COOH,下列对其性质的叙述中不正确的是
A.与钠反应放出氢气 B.能发生酯化反应
C.不能与新制的Cu(OH)2悬浊液反应 D.能与溴水发生加成反应
13.常温下,下列有关叙述正确的是
A.NaB溶液的pH=8,c(Na+)–c(B–)=0.99×10–6mol/L
B.Na2CO3溶液中,2c(Na+)=c(CO32–)+c(HCO3–)+c(H2CO3)
C.pH相等的①NH4Cl、②(NH4)2SO4、③NH4HSO4三种溶液中,c(NH4+)大小顺序为:①=②>③
D.10 mL pH=12的氢氧化钠溶液中加入pH=2的HA至pH刚好等于7,所得溶液体积V(总)≥20mL
12.元素A和B的原子序数都小于18。已知A元素原子最外层电子数为a,次外层电子数为b;B元素原子的M层电子数为(a-b),L层电子数为(a+b),则A、B两元素所形成的化合物的性质可能有
A.能与水反应 B.能与硫酸反应
C.能与碳酸钠反应 D.能与氢氧化钠反应
11.钢铁“发蓝”是将钢铁制品浸到某些氧化性的溶液中,在钢铁的表面形成一层四氧化三铁的技术过程。其中一种办法是将钢铁制品浸到亚硝酸钠和浓氢氧化钠的混合溶液中加热到130℃反应。其过程可以用如下化学方程式表示:
① 3Fe+NaNO2+5NaOH = 3Na2FeO2+H2O+NH3↑;
② 6Na2FeO2+NaNO2+5H2O = 3 Na2Fe2O4+ NH3↑+7NaOH;
③ Na2FeO2+ Na2Fe2O4+2H2O = Fe3O4+4NaOH;
下列说法不正确的是
A.该生产过程会产生污染 B.反应②中的氧化剂是NaNO2
C.整个反应过程中每有16.8gFe参加反应转移0.8mol电子
D.反应①②③均是氧化还原反应
10.下列离子方程式正确的是
A.将少量SO2气体通入NaClO溶液中:SO2+2ClO-+H2O==SO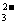 +2HClO
+2HClO
B.在硫酸氢钾溶液中加入Ba(OH)2溶液至pH=7:
2H++SO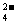 +Ba2++2OH–==
BaSO4↓+2H2O
+Ba2++2OH–==
BaSO4↓+2H2O
C.在碳酸氢镁溶液中加入足量Ca(OH)2溶液:
Mg2++2HCO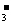 +Ca2++2OH–== MgCO3↓+CaCO3↓+2H2O
+Ca2++2OH–== MgCO3↓+CaCO3↓+2H2O
D.三氯化铝溶液中加入过量氨水:Al3++3OH– == Al(OH)3↓
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com