
26.(15分)A、B、C三种元素的质子数之和为16,它们的单质在一定条件下两两化合可以生成三种常见的化合物D、E、F、F的一个分子中只含有10个电子,E的相对分子质量比D大。
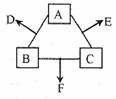
(1)B的元素名称是________,C单质的电子式是__________。
(2)A、B两元素还能形成一种比D相对分质量大16的化合物,请写出该化合物的一种用途________;A、C两元素也还能形成一种比E相对分子大16的化合物,请写出实验室制备该化合物反应的化学方程式_______________。
(3)E、F在一定条件下可以发生反应生成C元素的单质和D,该反应中氧化产物与还原产物的物质的量之比为_____________。
(4)A、B、C三种元素能组成一种原子个数比为3:4:2的常见化合物,0.1mol·L-1的该化合物的水溶液中,离子浓度由大到小的顺序是_____________。
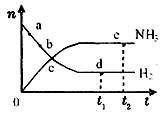
13.对于密闭容器中的反应:N2(g)+3H2(g) 2NH3(g);△H<0,在672K,30MPa下n(NH3)和n(H2)随时间变化的关系如图所示。下列叙述正确的是 ( )
2NH3(g);△H<0,在672K,30MPa下n(NH3)和n(H2)随时间变化的关系如图所示。下列叙述正确的是 ( )
A.点a处的正反应速率比点b点的大
B.点c点的正反应速率等于逆反应速率
C.点d(t1时刻)的n(N2)比点e(t2时刻)处的n(N2)大
D.其他条件不变,773k下反应至t1时刻,此时画出的两根平行间的距离将要变大
第Ⅱ卷(非选择题,共174分)
12.下列有关实验操作说法中,正确的是 ( )
①用pH试纸测得氯水的pH为2
②用量筒、试管胶头滴管、玻璃棒、蒸馏水和pH试纸,可鉴别pH相等的硫酸和醋酸
③分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
④用碱式滴定管量取25.00mL溴水
⑤可用渗析的方法除去淀粉中混有的少量的NaCl杂质
⑥在进行过滤操作时,为了加快速率,可用玻璃棒不断搅拌过滤器中液体
A.①③⑤ B.②③⑤ C.③④⑤ D.①③④⑥
11.现有Na2CO2、H2SO4、Ba(OH)2三种物质的量浓度与体积都相等的溶液,若以不同顺序将它们中的两种混合起来,出现沉淀后过滤,再将滤液与第三种溶液混合起来,最终所得的溶液 ( )
A.一定呈酸性 B.不可能呈碱性 C.可能呈中性 D.一定呈中性
9.下列叙述正确的是 ( )
A.液态氟化氢中存在氢键,所以其分子比氯化氢更稳定
B.阴离子的核外电子排布一定与上一周期稀有气体原子核外排布相同
C.甲烷、二氧化碳都是非极性分子,因此它们分子的空间结构相同
D.若ⅡA某元素的原子序数为m,则同周期IIIA元素的原子序数有可能m+11
|
①原子的最外层电子数大于3;②单质在反应中都只能作氧化剂;
③对应的含氧酸都是强酸; ④氢化物常温下都是气态,所以又叫气态氢化物。
A.只有①② B.全部 C.只有①②③ D.只有①②④
8.2008年北京奥运会“祥云”火炬用的环保型燃料--丙烷(C3H8),悉尼奥运会火炬所用燃料为65%丁烷(C4H10)和35%丙烷,已知丙烷的燃烧热为:2221.5kJ·mol-1,下列有关说法正确的是 ( )
A.丙烷燃烧的热化学方程式C3H8(g)+5O2(g)=3CO2(g)+4H2O(g);△H=-2221.5kJ·mol-1
B.奥运火炬燃烧主要是将化学能转变为热能和光能
C.丙烷、空气及铂片可组成燃料电池,在丙烷附近的铂极为电池的正极
D.丙烷的沸点比丁烷高
7.设NA为阿伏加德罗常数,以下叙述正确的是 ( )
A.5.6g铁与硝酸反应失去的电子数一定为0.3NA
B.标准状况下,22.4L已烷所含碳原子数为6NA
C.20℃、1.01×105Pa时,2.8gC2H4和CO的混合气体,含气体分子数为0.1NA
D.0.1L 3mol·L-1的Al2(SO4)3溶液中含有的Al3+数目为0.6NA
6.食品保鲜膜按材质分为聚乙烯(PE)、聚氯乙烯(PVC)等种类。PE保鲜膜可直接接触食品,PVC保鲜膜则不能直接接触食品,它对人体有潜大危害。下列有关叙述不正确的是 ( )
A.PE、PVC都属于链状高分子化合物,受热易熔化
B.PE、PVC的单体都是不饱和烃,能使溴水褪色
C.焚烧PVC保鲜膜会放出有毒气体HCl
D.废弃的PE和PVC均可回收利用以减少白色污染
28.(12分)据报道,北京奥运会“祥云”火炬燃料为丙烷,悉尼奥运会火炬燃料为丁烷和丙烷混合气。
(1)常温、同压下,等体积的丙烷和丁烷完全燃烧恢复到原状态,生成二氧化碳的体积比为 。
(2)已知丁烷的燃烧热(生成液态水)为2880kJ/mol,1mol丙烷和丁烷(物质的量之比1:1)的混合气完全燃烧放出的热量为2550kJ。写出丙烷燃烧的热化学方程式
(3)标准状况下,1.0mol丙烷和丁烷的混合气和足量氧气混合完全燃烧后,恢复至原状态,混合气体的体积减小了70.0L,混合气体中丙烷和丁烷的体积比为 。
(4)标准状况下,aL的某丙烷和丁烷的混合气体,在bL足量氧气中完全燃烧后,恢复到原状态体积为VL,所得气体体积V为(用a和b表示) 。
27.(15分)A、B、D、E和F为中学化学常见的化合物,A、B、D、E的焰色反应均呈黄色,F为无色无味气体。相互转化关系如下:A+F→B+O2 B+F+H2O→D D+E→B+H2O请根据题目要求回答下列问题。
(1)①写出E的电子式 ;
②写出反应A+F→B+O2的化学方程式 ;
③写出D溶液与E溶液反应的离子方程式 。
(2)如图16装置(I)为以E为电解质的氢氧燃料电池的示意图。
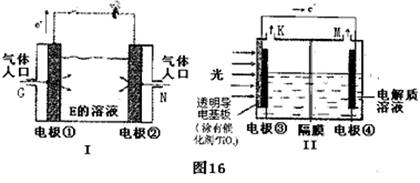
装置(I)中G和N为气体进口,其中G口进入的气体名称是 ,写出电极②的电极反应式 。
(3)装置(II)是新近研制装有涂二氧化钛的光电析的光电电解水装置的示意图,在电极附近的K出口产生气体化学式是 。
(4)在A中加入稀硫酸可生成一种含有非极性键的共价化合物X,写出向E和X的混合溶液中,通入二氧化氮反应的离子方程式 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com