
1.下列有关钋(Po)的说法正确的是
A. 钋原子的核外电子数是126 B. 钋原子核内中子数与质子数之差是42
C. 钋是金属元素,最外层电子数小于4 D. 钋元素的相对原子质量是210
29.(16分)
(1)苯氯乙酮是一具有荷花香味且有强催泪作用的化学试剂,它的结构简式如下图所示:
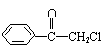
 则苯氯乙酮不可能具有的化学性质是
(填字母序号)
则苯氯乙酮不可能具有的化学性质是
(填字母序号)
A、加成反应 B、取代反应 C、消去反应
D、水解反应 E、银镜反应
(2)今有化合物:
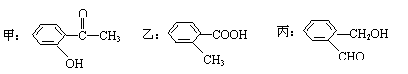

①请写出丙中含氧官能团的名称
②请判别上述哪些化合物互为同分异构体:
③请按酸性由强至弱排列甲、乙、丙的顺序:
(3)由丙烯经下列反应可制得F、G两种高分子化合物,它们都是常用的塑料。
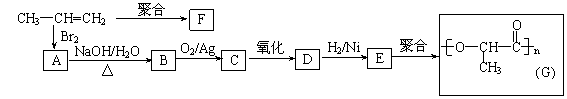

①丙烯分子中,最多有 个原子在同一个平面上;
②聚合物F的结构简式是 ;
③B转化为C的化学方程式是 ;
④在一定条件下,两分子E能脱去两分子水形成一种六元环状化合物,该化合物的结构简式是 。
28.(16分) 我国化工专家侯德榜的“侯氏制碱法”曾为世界制碱工业做出了突出贡献。他以NaCl、NH3 、CO2等为原料先制得NaHCO3,进而生产出纯碱。有关反应的化学方程式为:NH3 + CO2 + H2O = NH4HCO3 ; NH4HCO3 + NaCl = NaHCO3↓+ NH4Cl ;
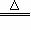 2NaHCO3 Na2CO3 + CO2↑+
H2O
2NaHCO3 Na2CO3 + CO2↑+
H2O
⑴碳酸氢铵与饱和食盐水反应,能析出碳酸氢钠晶体的原因是 (填标号)。
A.碳酸氢钠难溶于水 B.碳酸氢钠受热易分解
C.碳酸氢钠的溶解度相对较小,所以在溶液中首先结晶析出
⑵某探究活动小组根据上述制碱原理,进行碳酸氢钠的制备实验,同学们按各自设计的方案实验。
① 一位同学将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验装置如下图所示(图中夹持、固定用的仪器未画出)。
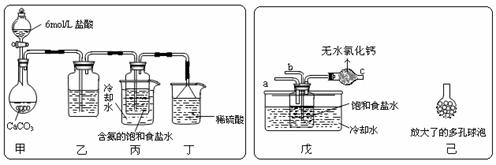
试回答下列有关问题:
 (Ⅰ)乙装置中的试剂是 ;
(Ⅰ)乙装置中的试剂是 ;
(Ⅱ)丁装置中稀硫酸的作用是 。
(Ⅲ)实验结束后,分离出NaHCO3 晶体的操作是 (填分离操作的名称)。
② 另一位同学用图中戊装置(其它装置未画出)进行实验。
(Ⅰ)实验时,须先从 管通入 气体,再从 管中通入 气体。
(Ⅱ)有同学建议在戊装置的b管下端连接己装置,理由是
。
⑶请你再写出一种实验室制取少量碳酸氢钠的方法:
。
27.(14分)t℃时,将3 mol A和1 mol B气体通入体积为2 L的密闭容器中(容积不变),发生如下反应:3A(气)+B(气) xC(气),2 min时反应达到平衡状态(温度不变),剩余了0.8 mol B,并测得C的浓度为0.4
xC(气),2 min时反应达到平衡状态(温度不变),剩余了0.8 mol B,并测得C的浓度为0.4 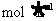 ,请填写下列空白:
,请填写下列空白:
(1)从开始反应至达到平衡状态,生成C的平均反应速率为_____________________,A的转化率是 ;
(2)x=____ ___;
(3)若继续向原平衡混合物的容器中通入少量氦气(假设氦气和A、B、C都不反应)后,化学平衡(填字母)___ _____;
A.向正反应方向移动 B.向逆反应方向移动 C.不移动
(4)若向原平衡混合物的容器中再充入a mol C,在t℃时达到新的平衡,此时B的物质的量为n(B)=____________________mol;
(5)如果上述反应在相同温度和容器中进行,欲使反应达到平衡时C的物质的量分数与原平衡相等,起始加入的三种物质的物质的量n(A)、n(B)、n(C)之间应该满足的关系式为____________________________________________。
26.(14分)A、B、C、D、E均为中学化学常见的纯净物,B为自然界中含量最多的液体,它们之间有如下的反应关系:
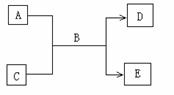
(1)常温下,若A为气态单质,C为非金属氧化物,A、C均能使品红溶液褪色,相对分子质量E﹥D,则:该反应的反应方程式为 ,检验D中阴离子的方法是 。
(2)若A为短周期的金属单质,D为气态单质,C溶液呈强酸性或强碱性时,该反应都能进行。写出反应的离子方程式 ;
。
(3)若A、C均为化合物,E为白色沉淀,C为引起温室效应的主要气体,写出E可能的化学式(写两种) 、 。
写出生成E的一个离子方程式 。
13.以氢氧化钾溶液、氢气、氧气组成的燃料电池,电解饱和硫酸钠溶液一段时间,假设电解时温度不变且用惰性电极,下列说法不正确的是
A.当电池负极消耗mg气体时,电解池阴极有mg气体生成
B.电解池的阳极反应式为:4OH-- 4e-==2H2O + O2↑
C.电解后,c(Na2SO4)不变,且溶液中有晶体析出
D.电池中c(KOH)不变;电解池中溶液pH变大
第Ⅱ卷(非选择题,共174分)
本卷共10题
12.2006年中国防治禽流感药物研究取得重大突破,从中药材提取的金丝桃素对人工感染的H5N1亚型禽流感家禽活体具有良好的治愈率。已知金丝桃素的结构简式为如下,下列有关说法正确的是
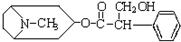
A.金丝桃素的分子式为C17H22O3N
B.金丝桃素能在NaOH溶液中加热反应得到两种芳香族化合物
C.金丝桃素能与浓硫酸和浓硝酸的混合液反应
D.1mol金丝桃素最多能与4molH2发生加成反应
11.在甲、乙两烧杯溶液中,含有大量的Cu2+、K+、H+、NO3-、CO32-、OH-等6种离子。已知甲烧杯的溶液呈蓝色,则乙烧杯中大量存在的离子是
A.Cu2+、H+、NO3- B.K+、CO32-、OH-
C.CO32-、OH-、NO3- D.K+、H+、NO3-
10.做实验时不小心粘了一些高锰酸钾,皮肤上的黑斑很久才能消除,如果用草酸的稀溶液洗涤马上可以复原,其离子方程式为:MnO4-+
C2O42-+H+ → CO2↑+ Mn2++ ,关于此反应的叙述正确的是
,关于此反应的叙述正确的是
A.该反应的氧化剂是C2O42- B.该反应右边方框内的产物是OH-
C.配平该反应,电子转移总数是5e- D.配平该反应后,H+的系数是16
9.根据实验现象所作的的结论一定正确的是
A.无色试液 出现银镜
结论:试液中有醛类物质
出现银镜
结论:试液中有醛类物质
B.无色试液 产生白色沉淀 结论:试液中含有Ca(OH)2
产生白色沉淀 结论:试液中含有Ca(OH)2
C.无色试液 试液变红 结论:试液显碱性
试液变红 结论:试液显碱性
D.无色试液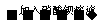 产生白色沉淀
结论:试液中含有SO42-离子
产生白色沉淀
结论:试液中含有SO42-离子
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com