
10.下列有关说法正确的是
A.MgCl2、聚氯乙烯、HD均为化合物
B.干馏、常压分馏、萃取都是物理变化
C.明矾、冰醋酸、硫酸钡和干冰均为电解质
D.质子数相同、电子数也相同的粒子,不可能是一种分子和一种离子
9.2008年北京奥运会“祥云”火炬用的是环保型燃料--丙烷(C3H8),悉尼奥运会火炬所用燃料为65%丁烷(C4H10)和35%丙烷,已知常压下1 mol丙烷完全燃烧生成稳定氧化物时放出的热量为2221.5kJ,下列有关说法正确的是
A.奥运火炬燃烧主要是将化学能转变为热能和光能
B.丙烷的沸点比正丁烷高
C.丙烷、空气及铂片可组成燃料电池,在丙烷附近的铂极为电池的正极
D.丙烷燃烧的热化学方程式为C3H8(g)+5O2(g)=3CO2(g)+4H2O(g);△H=-2221.5kJ.mol-1
30.(7分)用0.4molA金属与足量稀硫酸充分反应。将放出的气体干燥后通过45g灼热的CuO粉末,反应后的固体剩余物的质量为40.2g。实验测得在反应中气体的利用率为50%,在该金属形成的氧化物中氧的质量分数为47.1%。计算:
(1)金属与稀硫酸反应时放出氢气的体积(标准状况)。
(2)该金属的相对原子质量。
29.(20分)水蒸汽通过灼热的焦炭后,流出的气体的主要成分是CO和H2,还有CO2和水蒸汽等。请用上图中提供的仪器,选择必要的试剂,设计一个实验,证明上述混合气中有CO和H2。(加热装置和导管等略去)
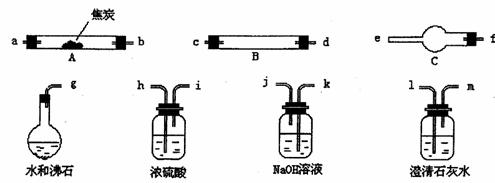
回答下列问题:
(1)盛浓硫酸的装置的用途是
盛NaOH溶液的装置的用途是
(2)仪器B中需加入的试剂的名称(或化学式)是
所发生反应的化学方程式是
(3)仪器C中需加入试剂的名称(或化学式)是
所发生反应的化学方程式是
(4)按气流方向连接各仪器,用字母标示借口的连接顺序:
g– a – b
(5)能证明混合气体中含有CO的实验依据是:
(6)能证明混合气中含有H2的实验依据是:
28.(16分)已知A、B、D、E四种物质中均含有同一种短周期元素,D为气体单质,E为黑色粉末,它们有如图所示转化关系(某些产物已略去)。
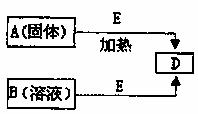
请回答:
(1)A的化学式为 ;B分子的电子式为 。
(2)已知E与含A中某元素的酸在一定条件下反应,产生一种含该元素的气体X。某化学兴趣小组为研究该气体的性质,设计如图所示装置进行试验。装置III中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
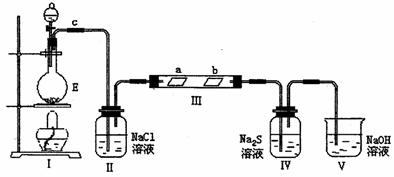
①加入式试剂前,检验气体发生装置I的气密性的操作是:
②写出装置I中发生反应的离子方程式:
③实验过程中,观察到装置IV中出现淡黄色沉淀,其主要反应的离子方程式为:
④实验结束后,该小组同学观察到在装置III中的b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为达到这一预期目的,你认为应对实验装置作如何改进
(3)气体X能与溶液B反应,生成气体D,写出该变化的化学方程式:
27.(10分)下图是无机盐A-M在一定条件下的转化关系(部分产物及反应条件未列出)。其中,I是由第三周期元素组成的单质中熔点最高的金属,K是一种红棕色气体。
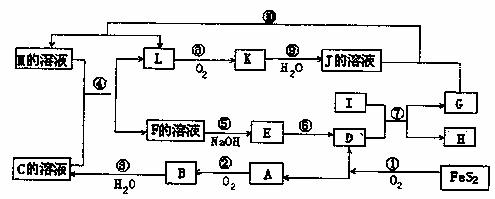
请填写下列空白:
(1)在周期表中,组成单质G的元素位于第 周期,第 族。
(2)在反应⑩中,氧化剂与还原剂的物质的量之比为 。
(3)工业上完成反应①、②的设备名称分别为 。
(4)写出反应④的离子方程式 。
(5)写出C的浓溶液与I在加热时反应的化学方程式:
。
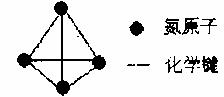
26.(14分)对于氮元素形成的单质,除了已知的氮气,科学家还先后研究出了N4、N60、N70、高聚氮等。其中高聚氮是在高压下通过氮气的聚合形成的,晶体中每个氮原子都通过三个单键与其它氮原子结合并向空间发展构成立体网状结构;N4分子结构如图所示。已知断裂N4分子中1molN-N吸收167kJ热量,断裂其它分子中1molN-N吸收193kJ热量,生成1molN≡N放出942kJ热量。根据以下信息和数据,回答下列问题:
(1)N70的摩尔质量为 。
(2)N4、N60、N70、高聚氮形成晶体时,熔沸点最高的是 。
(3)N4、N60、N70、高聚氮中,最不稳定的可能是 。
(4)1molN4气体转变为N2将 (填“吸收”或“放出”) kJ热量。
(5)原子数相同,电子总数相同的分子互称为等电子体。仅由第二周期元素形成的分子中,互为等电子体的是 和 ;
和 。
25.(11分)(1)为减少城市空气中二氧化硫含量,太原市政府规定在市区内禁止燃烧原煤。“蜂窝煤”是将原煤粉碎后添加黏土、生石灰加工而成的一种常见的燃料,请写出“蜂窝煤”燃烧时有关“固硫”(不使含硫化合物进入大气)反应的化学方程式:
(2)山西祁县是中国驰名的玻璃之都,该县出产的玻璃日用品和工艺品现在已行销世界各国。工业制造普通玻璃的原料是 ,主要反应的化学方程式为:
24.下列各组物质中,只用一种试剂不能区别的是 ( )
A.四种黑色固体:FeO、Fe、CuO、C
B.四种无色溶液:(NH4)2SO4、NH4Cl、Na2SO4、NaCl
C.四种无色气体:H2、HCl、SO2、CO2
D.四种无色液体:苯、四氯化碳、已烯、乙醇
第Ⅱ卷(共78分)
|
23.下列变化能够实验的是 ( )
①酸性氧化物与酸反应 ②两种含氧化合物反应有气体生成
③两种酸溶液反应后呈中性 ④两种弱酸性溶液混合后呈强酸性
A.②③④ B.①②③④ C.②④ D.②③
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com