
11.下列说法正确的是 ( )
A.常温时,NaHCO3 溶液的pH 值比同浓度的Na2CO3 溶液小
B.将纯水加热至较高温度,水的离子积变大、pH变大、呈碱性
C.把Al2(SO4)3 和FeCl2溶液分别在空气中蒸干并灼烧最后分别得到Al2O3和Fe203 固体
D.以酚酞作指示剂,用相同浓度的盐酸滴定等体积等浓度的NaOH溶液和氨水,消耗盐酸的体积相同
9.下列离子方程式书写正确的是 ( )
A.硫酸亚铁溶液与稀硫酸、双氧水混合:Fe2++H2O2+2H+=Fe3++2H2O
B.在标准状况下,17.92LCO2气体通人到1Llmol/L的NaOH溶液中:
4C02 + 50H- = CO32- + 3HC03- + H20
C.等体积、等物质的量浓度的Ba(OH)2溶液与NaHCO3溶液混合:
Ba2++2OH-+2HCO3-=BaCO3↓+CO32-+H2O
D. 碳酸钠水解:CO32-+2H2O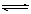 H2CO3+2OH-
H2CO3+2OH-
|
A.6 g NO2和40 g N2O4组成的混合气体中原子总数约为3NA
B.20g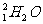 中所含的中子数为9 NA
中所含的中子数为9 NA
C.4.5g SiO2晶体中含有的硅氧键数目为0.3 NA
D.1 mol Fe与足量的Cl2反应时,失去的电子数为3NA
8.有关化学实验的基本操作中,正确的是 ( )
A.配制100 mL 1.0 mol/LNa2C03溶液,称取10.6 g无水碳酸钠,加入100 mL容量瓶中,加水溶解、定容
B.为测定熔融氢氧化钠的导电性,可在瓷坩埚中熔化氢氧化钠固体后进行测量
C.中和热测定实验中以环形铜丝搅拌棒代替环形玻璃搅拌棒会使测定值比理论值偏低
D.检验亚硫酸钠固体是否变质,先将少量样品溶于水中,再加入酸化的硝酸钡溶液
7.下列有关物质分类或归类正确的是 ( )
①混合物:盐酸、漂白粉、水玻璃、水银
②化合物:CaCl2、NaOH、HCl、HD
③电解质:明矾、石膏、冰醋酸、食盐
④同素异形体:C60、C70、金刚石、石墨
⑤同系物:CH2O2、C2H4O2、C3H6O2、C4H8O2
⑥同分异构体:乙二酸二乙酯、乙二酸乙二酯、二乙酸乙二酯
A.①③⑤ B.②③④ C.②④⑥ D.③④
6.胡锦涛同志在十七大报告中指出,应加强能源资源节约和生态环境保护,增强可持续发展能力。下列行为与之不相符的是 ( )
A.将作物秸秆通过化学反应转化为乙醇用作汽车燃料
B.使用资源节约型、环境友好型的生物降解塑料包装
C.大量使用化学肥料,提高农作物的产量和质量
D.推广煤炭脱硫技术、减少直接燃煤,防止酸雨发生
29.(17分)咖啡酸(A)是一种具有止血、镇咳、祛痰的芳香烃的衍生物,其分子模型如下图所示(图中球与球之间的连线代表化学键,如单键、双键等)。它具有如下转化关系
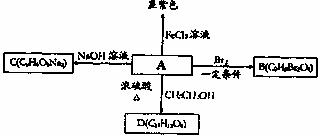
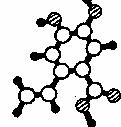
(1)写出A中除酚羟基外的含氧官能团名称 ,A的结构简式 。
(2)写出下列化学方程式或反应类型:
①A→B反应类型: ;
②A→D化学方程式: 。
(3)1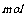 的A和
的A和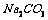 溶液反应,最多消耗
溶液反应,最多消耗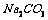
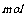 。
。
(4)E是1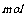 与1
与1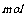 H2加成后的产物,同时符合下列的三个要求的E的同分异构体其中有
种。
H2加成后的产物,同时符合下列的三个要求的E的同分异构体其中有
种。
①苯环上有三个取代基,其中之两个为酚羟基
②属于酯类且能发生银镜反应
③苯环上的一氯化物只有2种
(5)现有咖啡酸和甲苯(C7H8)的混合物,它们的物质的量之和为n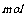 。该混合物在足量的氧气中完全燃烧,并将生成的产物通过足量的盛有无水硫酸铜的装置,则该装置增重
g。
。该混合物在足量的氧气中完全燃烧,并将生成的产物通过足量的盛有无水硫酸铜的装置,则该装置增重
g。
28.(19分)某化学兴趣小组的同学模拟工业制造硫酸的生产过程,设计了如图所示的装置,请按要求回答下列问题:
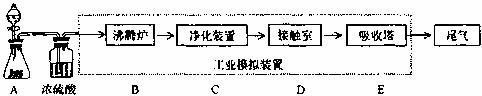
(1)装置A用来制取氧气,相应的化学反应施工为 。
(2)C装置为净化装置,若无该装置,将混合气体直接通入D装置,除对设备有腐蚀个,还会造成的后果是 。
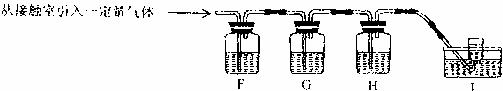
(3)甲同学为检验从接触室中出来的气体的主要成份,甲同学设计如下实验:
①请写出表中空格:
|
仪器 |
加入试剂 |
加入该试剂的目的 |
|
F |
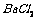 溶液 溶液 |
检验尾气中的SO3 |
|
G |
|
|
|
H |
|
|
②乙同学认为,上述实验中检验尾气中的方法是错误的,其理由是(用必要的文字及化学反应方程式说明)
。
27.(12分)常温下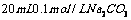 在溶液中逐滴加入
在溶液中逐滴加入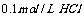 溶液
溶液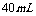 ,溶液pH的逐渐降低,此时溶液中含碳元素的微粒的量浓度的百分含量(纵轴)也发生变化
,溶液pH的逐渐降低,此时溶液中含碳元素的微粒的量浓度的百分含量(纵轴)也发生变化
(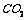 因逸出未画出),如下图所示
因逸出未画出),如下图所示
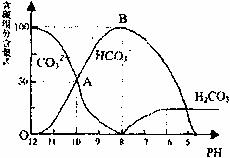
根据图回答下列问题:
(1)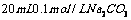 溶液呈碱性的原因是(用离子方程式表示):
;
溶液呈碱性的原因是(用离子方程式表示):
;
(2)当反应到A点时,此时溶液中所有阳离子和阴离子的浓度大小关系? ;
(3)B点表示的含义是 ;
(4)当混合液的PH=
时,开始放出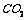 气体。
气体。
26.(12分)A、B、C和D均为短周期元素组成的非金属单质。其中B、C、D在常温下为气态,A为固体,W为含42个电子的离子化合物。它们满足如下图的转化关系。
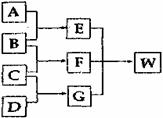
(1)已知E为直线型的非极性分子,则A的元素符号为 。
(2)写出G的电子式 ,W的名称 。
(3)写出D所含元素的最高价氧化物对应水化物的浓溶液与A反应的化学反应方程式
。
(4)将G和E通入饱和食盐水中,有晶体析出,写出该反应的化学反应方程式
。
13.在容积相同且恒定的两密闭容器A和B中,保持温度为150℃,同时向A容器中加入 a mol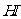 ,向B容器中加入 b mol
,向B容器中加入 b mol 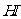 (a>b),当反应
(a>b),当反应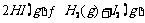 达到平衡后,下列说法正确的是 ( )
达到平衡后,下列说法正确的是 ( )
A.从反应开始达到平衡,所需时间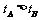
B.平衡时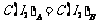
C.平衡时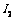 蒸气在混合气体中的体积分数:
蒸气在混合气体中的体积分数:
D.平衡时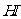 的转化率
的转化率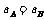
第Ⅱ卷
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com