
13.某同学往体积为1L的干燥容器用排空气法收集NH3气后,测得容器中气体对乙烯的相对密度为0.75,用此容器倒扣于水槽中充分进行喷泉实验,发现进入容器中溶液的体积约是a L,则下列说法正确的是: ( )
A.该同学所收集的氨气中混杂有大量乙烯
B.该同学所收集的气体中氨气与空气的体积比约为1:2
C.所进入容器的溶液中,溶质是NH3.H2O
D.经过计算,a的值约为0.67
非选择题
12.对自然学科的学习,不能局限于被动地接受前人的成果,还应能利用相关知识解释各种变化现象和事实。对于下列事实的解释中,正确的是 ( )
A.蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸有很强的吸水性
B.常温常压下H2S为气态而H2O为液态,说明H2O分子中的共价键比H2S中的强
C.常温下,浓硫酸可以用铁罐贮存,说明此条件下铁与浓硫酸不反应
D.已知溶液中反应CuSO4 + H2S=CuS↓+ H2SO4能进行,说明CuS不溶于水和稀硫酸
11.下列离子组合中,可以大量共存于强酸溶液中的是 ( )
A.Al3+、Na+、NO3-、Cl-
B.Na+、K+、MnO4-、Br-
C.NH4+、Na+、AlO2-、NO3-
D.K+、Na+、SO42-、SO32-
10.溶液中能发生如下反应:2KClO3+I2=2KIO3+Cl2,由此相应的结论中不正确的是( )
|
B.单质的还原性:I2> Cl2
C.元素的非金属性:I>Cl
D.KClO3中的Cl在反应中得电子
9.在下列各组元素中,都属于主族的是 ( )
A.原子序数为11、21、31的元素 B.核电荷数为35、37、38的元素
C.质子数为29、30、31的元素 D.原子核外电子数为18、28、35的元素
8.下列离子方程式书写正确的是 ( )
A.往FeBr2溶液中通入足量的氯气:2Fe2++2Br- +2Cl2 = 2Fe3+ + Br2 + 4Cl-
B.Ca(HCO3)2溶液中加入过量的NaOH溶液:Ca2++2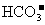 +2OH-=CaCO3↓+2H2O+
+2OH-=CaCO3↓+2H2O+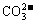
C.用氢氧化钠溶液吸收少量二氧化碳:OH-+CO2=H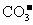
D.钠和冷水反应:Na+2H2O=Na++H2↑+OH-
7.设NA代表阿伏加德罗常数,下列说法正确的是 ( )
A.1.8g重水(D2O)中含NA个中子
B.在铜与足量硫蒸汽的反应中,1 mol铜失去的电子数为2NA
C.在常温常压下,11.2L氧气所含的原子数为NA
D.0.5mol铝与足量烧碱溶液反应,转移的电子数为1.5NA
6.广西从2008年4月起将全面起用车用乙醇汽油。车用乙醇汽油是把乙醇和汽油按一定比例混和配制而成的一种新型汽车燃料。经多项检测结果表明,它不影响汽车的行驶性能,还可以减少有害气体的排放量。下列有关乙醇汽油的说法正确的是 ( )
A.乙醇汽油是一种纯净物
B.乙醇汽油作燃料不会产生污染环境的有害气体
C.乙醇和汽油都可作溶剂,它们也可相互溶解
D.常温常压下,乙醇汽油呈气态
29.(16分)化合物A最早发现于酸牛奶中,它是人体内糖代谢的中间体,可由马铃薯、玉米淀粉等发酵制得,A的钙盐是人们喜爱的补钙剂之一。A在某种催化剂的存在下进行氧化,其产物不能发生银镜反应。在浓硫酸存在下,A可发生如下图所示的反应。
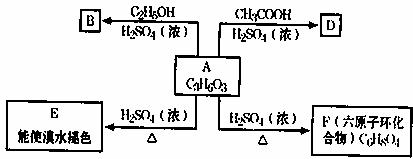
请写出:
⑴化合物的结构简式:A ;B 。
⑵化学方程式:A→E ;
A→F 。
⑶反应类型:A→E ;A→F 。
28.(14分)图示装置可用来制取和观察Fe (OH) 2在空气中被氧化时的颜色变化。实验时必须使用铁屑和6mol·L-1的硫酸,其它试剂任选。请填写下列空白:
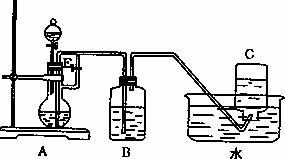
⑴B中盛有一定量的NaOH溶液,A中应预先加入的试剂是 , A中反应的离子方程式是 。
⑵实验开始时应先将活塞E (填“打开”“关闭”或“无关系”),C中收集到气体的主要成分是 。
⑶当C中收集到足量气体后,简述生成Fe(OH)2的操作过程 。
⑷拨去装置B中的橡皮塞,使空气进入,写出有关反应的化学方程式: 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com