
29.(15分)已知具碳碳双键结构的有机物可被酸性高锰酸钾溶液氧化成二元醇,如:
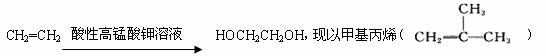
为原料合成环状化合物F和高分子化合物E和G。
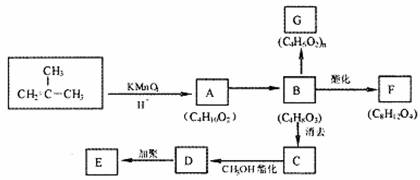
(1)C中所含的官能团是 。
(2)A→B的反应类型是 ;G的结构简式是 。
(3)B→C的化学方程式 。
(4)两分子B之间发生酯化反应除去成酯F外,还可能生成另外一种酯,该酯的结构简式为 。
(5)B物质的同分异构体中,与B所含的官能团种类、数目都相同的(不包括B)还有
种,写出其中一种的结构简式 。
28.(15分)硫酸铜是一种应用极其广泛的化工原料。铜不能与稀硫酸直接反应,本实验中将适量浓硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发、结晶得到硫酸铜晶体(装置如图1、2所示)
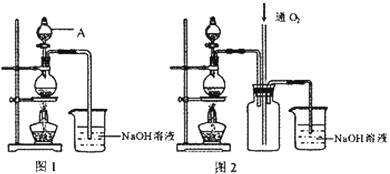
(1)图1烧瓶中发生的离子反应方程式为: 。
(2)图2是图1的改进装置,其优点有: 。
(3)为符合绿色化学的要求,某研究性学习小组进行如下设计:
第一组:以空气为氧化剂法
方案1:以空气为氧化剂。将铜粉在仪器B中反复灼烧,使铜与空气充分反应生成氧化铜,再将氧化铜与稀硫酸反应。
方案2:将空气或氧气直接通入到铜粉与稀硫酸的混合物中,发现在常温下几乎不反应。向反应液中加FeSO4或Fe2(SO4)2,即发生反应。反应完全后向其中加物质甲调节pH到3~4,产生Fe(OH)3沉淀,过滤、蒸发、结晶,滤渣作催化剂循环使用。
(已知Fe(OH)3和Cu(OH)2完全沉淀时的pH分别为3.7、6.4。)
请回答下列问题:①方案中的B仪器名称是 。
②方案2中甲物质是 (填字母序号)。
a.CaO b.CuCO3 c.CaCO3
第二组:过氧化氢为氧化剂法
将3.2g铜丝放到45ml 1.5mol·L-1的稀硫酸中,控温在50℃。加入18mL 10%的H2O2,反应0.5h后,升温到60℃,持续反应1h后,过滤、蒸发结晶、减压抽滤等,用少量95%的酒精淋洗后晾干,得到CuSO4·5H2O的质量为10.6g。
请回答下列问题:
③加热时温度不宜过高的原因是 ,根据有关数据计算出制取CuSO4·5H2O的产率(实际产量与理论产量的百分比)= 。
27.(15分)有一些常见化学反应可用下式表示A+B→C+D+H2O
请你根据下面的提示回答下列问题:
(1)若A、C、D均含有氯元素,B中不含氯元素,则A的分子式为 。
(2)若C、D均为气体且都能使澄清石灰水变浑浊,则A与B的组合属无机物的是
。
(3)若A、C均含有铝元素,且C溶液呈酸性,则A可能是 。写出一个符合该反应的化学方程式: 。
(4)若C为不溶于稀硝酸的白色沉淀,则该反应的离子方程式可能为
。
26.(15分)有A、B、C、D、E五种不同主族元素,其原子序数依次增大,且都不超过20。其中只有E为金属元素,B、C最外层电子数是内层的整数倍,A、B、C三种元素的原子序数之和小于D。请回答下列问题:
(1)E在周期表中位置 。
(2)写出实验室中制备D单质的化学方程式 。并指出该单质的一种用途 。
(3)B、E组成的化合物W是一种重要的化工原料,写出W的电子式 。
(4)X是由上述三种元素组成的一种化合物,已知
5X+2MnO-4+6H+==10CO2↑+2Mn2++8H2O则X为 (填化学式)
(5)由A、B、C三种元素形成的一类有机物完全燃烧时消耗的O2与生成的CO2的物质的量之比为1:2,则此类有机物中相对分子质量最小的化学式为 。
13.将一定质量的锌与10mL 18.5mol·L-1浓硫酸充分反应,锌完全溶解,同时生成标准状况下的气体3.36L。将反应后的溶液稀释至100mL,测得溶液中c(H+)=0.1mol·L-1,则投入的锌的质量是 ( )
A.6.5g B.9.75g C.13g D.16.25g
第Ⅱ卷(非选择题共174分)
12.天文观察台探测到了银河系中心2.6万光年处一巨大气云中的特殊电磁波。这种电磁波表明那里可能有乙醇醛糖分子存在。下列有关乙醇醛糖(HOCH2CHO)的有关说法正确的是 ( )
①乙醇醛糖是一种有机物,易溶于水
②乙醇醛糖能发生取代反应、加成反应、氧化反应以及还原反应
③乙醇醛糖能分别与Na、NaOH溶液发生反应
④1mol乙醇醛糖与足量的银氨溶液作用,可析出2mol Ag
⑤乙醇醛糖与甲酸甲酯互为同分异构体
A.①③ B.①②③④
C.①②④⑤ D.①②③④⑤
11.A、B、C为短周期中原子序数依次增大的三种主族元素,已知C的核内质子数为A、B之和,B的K、L两层电子数之差等于A核外电子数的两倍。下列说法中正确的是( )
A.A、B、C所组成的单质晶体类型不可能相同
B.由A、B、C三种元素所组成的化合物相对分子质量最小为31
C.A与B、A与C所组成的晶体熔化时克服的作用力完全相同
D.A与B、A与C所形成的最简单分子前者是非极性分子,后者为极性分子
9.用NaOH溶液吸收二氧化硫,将所得的混合液进行电解循环再生,这种新工艺叫再生循环脱硫法。其中阴阳膜组合循环再生机理如图,则下列有关说法正确的是 ( )
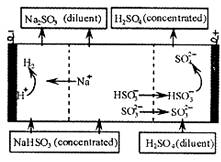
A.阳极区酸性减弱
B.阴极区电极反应式为:2H++2e-=H2↑
C.该过程主要是为了获得H2SO4
D.电解时两个电极都只能用惰性材料
|
A.若混合溶液的pH=7,则V1c1>V2c2
B.若V1=V2,c1=c2,则混合液中c(NH+4)=c(Cl-)
C.若混合液的pH=7,则混合液中c(NH+4)>c(Cl-)
D.若V1=V2,且混合液的pH<7,则一定有c1<c2
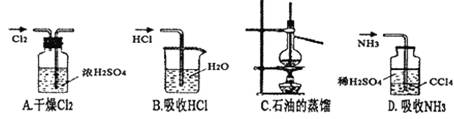
8.用下列实验装置完成对应的实验(部分仪器已省略),能达到实验目的的是 ( )
7.某非金属单质A和氧气发生化合反应生成B。B为气体,其体积是反应消耗的氧气体积的两倍(同温同压)。以下对B分子组成的推测一定正确的是 ( )
A.有一个氧原子 B.有两个氧原子 C.有一个A原子 D.有两个A原子
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com