
11、下列说法正确的是
A.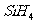 比
比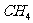 .稳定
.稳定
B.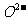 半径比
半径比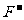 的小
的小
C.Na和Cs属于第ⅠA族元素,Cs失电子能力比Na的强
D.P和As属于第ⅤA族元素,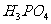 酸性比
酸性比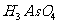 的弱
的弱
10、下列由事实得出的结论错误的是
A.维勒用无机物合成了尿素,突破了无机物与有机物的界限
B、门捷列夫在前人工作的基础上发现了元素周期律,表明科学研究既要继承又要创新
C 、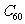 是英国和美国化学家共同发现的,体现了国际科技合作的重要性
是英国和美国化学家共同发现的,体现了国际科技合作的重要性
D、科恩和波普尔因理论化学方面的贡献获诺贝尔化学奖,意味着化学已成为以理论研 究为主的学科
9、下列叙述合理的是
A.金属材料都是导体,非金属材料都是绝缘体
B.棉、麻、丝、毛及合成纤维完全燃烧都只生成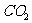 和
和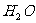
C.水电站把机械能转化成电能,而核电站把化学能转化成电能
D.我国规定自2008年6月1日起,商家不得无偿提供塑料袋,目的是减少“白色污染”
25.(9分)在A、B两份100ml氢氧化钠溶液中分别通入硫化氢气体0.1mol,然后将所得的溶液小心蒸干,分别得固体6.7g和9.8g,则:
(1)据计算推测所得固体的组成可能有哪些?
(2)A、B两份溶液的物质的量浓度为多少?
24.(4分)元素的多属性可以从它的①
② 判断;
元素的非金属性可以从它的③
④ 判断;
23.(8分)用A+、B-、C2-、D、E、F、G和H分别表示含有18个电子的八种微粒(离子或分子),请回答:
(1)A元素是 、B元素是 、C元素是 (用元素符号表示)
(2)D是由两种元素组成的双原子分子,其分子式是 。
(3)E是所有含18个电子的微粒中氧化能力最强的分子,其分子式是 。
(4)F是由两种元素组成的三原子分子,其分子式是 ,电子式是
(5)G分子中含有4个原子,其分子式是 。
22.(5分)根据原子结构理论和元素周期律,回答关于113号元素113X的问题(以X代替其元素符号):
(1)原子核外有 层电子,最外层电子数为
(2)它在元素周期表中的位置 ,属于 元素(“金属”“非金属”)
(3)它的最高价氧化物的水化物的化学式
21.(9分)A、B、C、D为原子序数依次增大的四种短周期元素,其中只有C为金属元素,且A、C同族,B、D同族,B、D的原子序数之和为A、C的原子序数之和的2倍。回答下列问题:
(1)A的元素符号为 B的元素符号为
(2)化合物C2B2的电子式为
(3)由A、B、C、D四种元素形成的两种化合物反应的离子反应方程式为:
(4)化合物CA可以和水反应生成一种气体,写出反应方程式并用双线桥标出电子转移的方向和数目: 。
20.(15分)二氯化二硫(S2Cl2)在工业上用于橡胶的硫化。为在实验室合成S2Cl2,某化学研究性学习小组查阅了有关资料,得到如下信息:
①将干燥的氯气在110℃-140℃与硫反应,即可得S2Cl2粗品
②有关物质的部分性质如下表:
|
物质 |
熔点/℃ |
沸点/℃ |
化学性质 |
|
S |
112.8 |
444.6 |
略 |
|
S2Cl2 |
-77 |
137 |
遇水生成HCl、SO2 S;300℃以上完全分解; S2Cl2+Cl2  2SCl2 2SCl2 |
设计实验装置图如下:
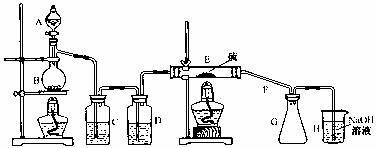
(1)上图尾气处理装置不够完善,请你提出改进意见 。
利用改进后正确装置进行实验,请回答下列问题:
(2)B中反应的离子方程式 。
(3)C、D中的试剂分别是 、 。
(4)如果在加热E时温度过高,对实验结果的影响是 ,在F中可能出现的现象是 。
(5)S2Cl2粗品中可能混有的杂质是(填写两种) 、 ,为了提高S2Cl2的纯度,关键的操作是控制好温度和 。
19.(6分)写出符合下列情况的化学方程式:
(1)H2S作还原剂 ;
(2)氢硫酸作氧化剂 ;
(3)SO2作还原剂 ;
(4)SO2作氧化剂 ;
(5)H2S既作还原剂又作氧化剂 ;
(6)SO2既不作还原剂又不作氧化剂 ;
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com