
6.下列物质中,按只有氧化性,只有还原性,既有氧化性又有还原性的顺序排列的一组是
A.F2、K、HCl B.Cl2、Al、H2 C.NO2、Na、Br2 D.O2、SO2、H2O
5.下列关于化学学习和研究的说法错误的是
A.化学模型有助于解释一些化学现象 B.质量守恒定律是大量试验事实的总结
C.化学家踢出的假设都能被试验证明 D.化学基本原理的应用是有一定条件的
4.下列化学式既能表示物质的组成,又能表示物质的一个分子的是
A.NaOH B.SiO2 C.Fe D.C3H8
3.植物及其废弃物可制成乙醇燃料,下列关于乙醇燃料的说法错误的是
A.它是一种再生能源 B.乙醇易燃烧,污染小
C.乙醇只能在实验室内作燃料 D.粮食作物是制乙醇的重要原料
2.化学科学需要借助化学专用语言描述,下列有关化学用语正确的是
A.CO2的电子式 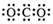 B. Cl-的结构示意图
B. Cl-的结构示意图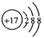
C.乙烯的结构简式 C2H4 D.质量数为37的氯原子17 37Cl
1.食品检验是保证食品安全的重要措施,下列不属于会食品安全检测指标的是
A.淀粉的含量 B.二氧化硫的含量
C.亚硝酸盐的含量 D.甲醛的含量
29.(16分)苯的含氧衍生物A的相对分子质量为180,其中碳元素的质量分数为60%,A完全燃烧消耗O2的物质的量与生成CO2的物质的量相等。请回答下列问题:
(1)A的分子式为__________。
(2)A的苯环上取代基彼此相间,A能发生银镜反应,也能与NaHCO3溶液反应产生CO2,还能与FeCl3溶液发生显色反应,则A含有的官能团名称是__________,
写出A可能的两种结构简式: __________、__________。
(3)A的一种同分异构体B是邻位二取代苯,其中一个取代基是羧基,B能发生右图所示转化:
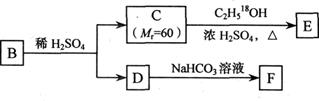
F的结构简式是_________________________;
写出下列反应的化学方程式:
①C→E____________________________________________________________
②D与浓溴水反应__________________________________________________
③B与足量NaOH溶液共热________________________________________
28.(15分)某学生利用以下装置探究纯净干燥的氯气与氨气之间的反应。
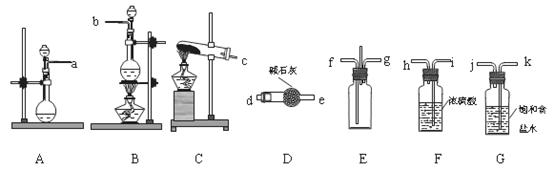
回答下列问题:
(1)根据下列所给试剂,选择制取氨气的装置是(填对应字母) ;写出制备氯气的离子反应方程式 。
二氧化锰、碱石灰、浓盐酸、浓氨水、烧碱、生石灰
(2)已知,E装置是用于使纯净干燥的氯气与氨气发生反应的装置,试说明该装置的设计意图: 。
(3)根据实验目的,所选装置的连接顺序为(填装置的接口字母):
( )接( ) ,( )接( f ),( g )接( ) ,( )接( ) ,( )接( ) ;其中,G装置的作用是 。
(4)氯气和氨气在常温下相混合就会发生反应生成氯化铵和氮气,该反应的化学方程式为: ;其中,氧化剂与还原剂的物质的量之比是 。
(5)请你评价此套装置有何缺点 。
27.(15分)已知A、B、D、E均为中学化学常见单质或化合物,它们之间的关系如图所示(部分产物略去)。
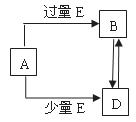
(1)若A和E为单质,组成A单质的元素是自然界中形成化合物种类最多的元素
① B属于分子 (填“极性”或“非极性”),B分子中各原子最外层 (填“是”或“否”)都满足8电子结构;
② 向50 mL4 mol/L的NaOH溶液中通入1.12 L B(标准状况),
反应后溶液中溶质的物质的量之比为 (填化学式和物质的量之比);
③ 4 g A单质完全燃烧放出131.2 kJ的热量,写出表示A单质燃烧热的热化学方程式
(2)若A为第三周期中的元素所形成的氯化物。
① 写出A溶液→B的离子方程式 ;
② 写出A和B的溶液反应的离子方程式 。
(3)若A为常见的金属,在E的冷、浓溶液中,A有钝化现象。已知:X为含有非极键的离子化合物,且1 mol X含有38 mol电子,向D溶液中加入与D等物质的量的X固体,恰好完全反应,写出该反应的离子方程式 。
26.(14分)(1)下列曲线分别表示元素的某种性质与该电荷数的关系(Z为该电荷数,Y为元素的有关性质)。请把与下面元素有关性质相符的曲线标号(a、b、c、d)填入相应的空格中:
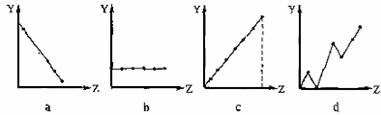
①ⅡA族元素的最外层电子数 。
②第3周期元素的最高化合价 。
③F-、 Na+ 、Mg2+、Al3+的离子半径 。
(2)元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大。已知Y原子最外层电子数与核外电子总数之比为3∶4;M原子的最外层电子数与次外电子数之比为3∶4;N-、Z+、X+离子半径逐渐减小;化合物XN常温下为气体,据此回答:
①N的最高价氧化物的水化物的化学式是 。
②化合物A、B均为由上述五种元素中的任意三种元素组成的强电解质,且两种物质水溶液的酸碱性相同,组成元素的原子数目之比均为1∶1∶1,A溶液中水的电离程度最小,则化合物A中的化学键类型为 ,若B为常见家用消毒剂的主要成分,则B的化学式是 。
③Z与M形成的稳定固体化合物的电子式为 。
④X与Y、X与M均可形成18电子分子,写出这两种分子在水溶液中反应生成一种单质的化学方程式 ,可观察到的实验现象是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com