
13、应2X(g)+Y(g) 2Z(g);△H<0(正反应为放热反应)。在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量[n(Z)]与反应时间(t)的关系如图所示。则下列判断正确的是(
)
2Z(g);△H<0(正反应为放热反应)。在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量[n(Z)]与反应时间(t)的关系如图所示。则下列判断正确的是(
)

A、T1<T2,P1<P2 B、T1<T2,P1>P2 C、T1>T2,P1>P2 D、T1>T2,P1<P2
12、可逆反应: 在密闭容器中反应,达到平衡状态的标志是( )
在密闭容器中反应,达到平衡状态的标志是( )
(1)单位时间内生成n molO2的同时,生成2n molNO2
(2)单位时间内生成n molO2的同时,生成2n molNO
(3)用NO2、 NO、 O2 的物质的量浓度变化表示的反应速率的比为2:2:1的状态
(4)混合气体的颜色不再改变的状态
(5)混合气体的密度不再改变的状态
(6)混合气体的平均相对分子质量不再改变的状态
A、(1)(4)(6) B、(2)(3)(5)
C、(1)(3)(4) D、(1)(2)(3)(4)(5)(6)
11、氢氧燃料电池是一种高性能电池,总反应为2H +O
+O =2H
=2H O,电解质溶液为KOH溶液,下列有关该电池的叙述中错误的是
( )
O,电解质溶液为KOH溶液,下列有关该电池的叙述中错误的是
( )
A、H 为负极,O
为负极,O 为正极
B、工作时电解质溶液的pH不断增大
为正极
B、工作时电解质溶液的pH不断增大
C、负极反应:2H -4e
-4e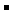 +4OH
+4OH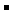 =4H
=4H O
D、正极反应:O
O
D、正极反应:O +4e
+4e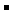 +2H
+2H O=4OH
O=4OH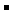
10、pH=1的两种酸溶液A、B各1mL,分别加水稀释到1000mL,其pH与溶液体积(V)的关系如图示,下列说法不正确的是 ( )
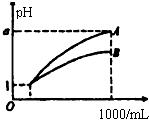
A、A、B两种酸溶液的物质的量浓度一定相等
B、稀释后,A酸溶液的酸性比B酸溶液弱
C、若a=4,则A是强酸,B是弱酸
D、若1<a<4,则A、B都是弱酸
9、25℃时,pH=2的HCl溶液中,由水电离出的H+浓度是 ( ).
A、1×10-7mol·L-1 B、1×10-14mol·L-1.
C、1×10-2mol·L-1 D、1×10-12mol·L-1.
8、元素A和B的原子序数都小于18。已知A元素原子的最外层电子数为a,次外层电子数为b;B元素原子的M层电子数为(a-b),L层电子数为(a+b),则A、B两元素所形成的化合物的晶体类型为 ( )
A、分子晶体 B、金属晶体 C、离子晶体 D、原子晶体
7、原电池的电极名称不仅与电极材料的性质有关,也与电解质溶液有关。下列说法中不正确的是 ( )
A、由Al、Cu、稀H2SO4组成原电池,其负极反应式为:Al-3e-=Al3+
B、由Mg、Al、NaOH溶液组成原电池,其负极反应式为:Al-3e-+4OH-=AlO2-+2H2O
C、由Fe、Cu、FeCl3溶液组成原电池,其负极反应式为:Cu-2e-=Cu2+
D、由Al、Cu、浓硝酸组成原电池,其负极反应式为:Cu-2e-=Cu2+
6、在101kPa和25℃时,有反应的热化学方程式:H2(g) + 1/2O2(g) =H2O(g);
△H=-241.8kJ/mol,H2(g) + 1/2O2(g) =H2O(1);△H=-285.8kJ/mol。下列说法中错误的是: ( )
A、H2燃烧生成1molH2O(g)时,放出241.8kJ的热量
B、H2的燃烧热为285.8kJ
C、O2 前面的1/2表示参加反应的O2的物质的量
D、1mol液态水变成水蒸气时吸收44kJ的热量
5、已知某溶液中滴加酚酞试液显红色,其中能大量存在的离子是 ( )
A、NH
 、Ba
、Ba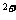 、AlO
、AlO
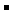 、Cl
、Cl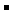 B、SO
B、SO
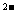 、NO
、NO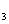
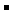 、Fe
、Fe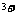 、Al
、Al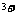
C、 Cl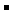 、SO
、SO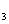
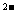 、Na
、Na 、K
、K D、Na
D、Na 、K
、K 、HCO
、HCO
 、Cl
、Cl
4、关于晶体的下列说法正确的是 ( )
A 、在晶体中只要有阴离子就一定有阳离子
B 、在晶体中只要有阳离子就一定有阴离子
C 、原子晶体的熔点一定比金属晶体的高
D 、分子晶体的熔点一定比金属晶体的低
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com