
1.下列所用材料不属于合金的是
A.家用的铝窗 B.建筑用的钢筋 C.铸造用的黄铜 D.温度计用的水银
22、(10分) A、B、C、D、E、F是常见单质,其中A是用量最大,应用最广泛的金属;元素D是地壳中含量最多的金属元素;D元素和E元素在周期表中相邻。G、H、I、J、K、L是常见化合物,其中G在常温下是无色液体,H是黑色固体。以上物质相互间的转化关系如下图所示:
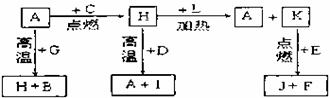
请回答下列问题: (1)元素A在元素周期表中的位置为 周期 族。
(2)写出K的电子式 。 (3)写出H和D反应的化学方程式 。 (4)D能与氢氧化钠溶液反应,请写出该反应的离子方程式 。 23、(8分)电解原理在化学工业中有广泛的应用。如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
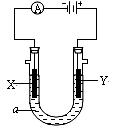
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则:
①电解池中X电极上的电极反应是______ _____,
在X极附近观察到的现象是________ ____。
②Y电极上的电极反应式为_____ ______,
检验该电极反应产物的方法是
。
(2)如果用电解方法精炼粗铜,电解液a选用CuSO4溶液,则:
①X电极的材料是___________,电极反应是_________________________。
②Y电极的材料是____________,电极反应是_________________________。
(说明:杂质发生的电极反应不必写出)
21、(6分)在稀氨水中存在下述电离平衡NH3+H2O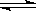 NH3
·H2O
NH3
·H2O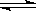 NH4++OH-,分别加入少量下列物质,溶液中c(OH-)如何变化?(填“增大”“减小”或“不变”);平衡移动方向如何?
NH4++OH-,分别加入少量下列物质,溶液中c(OH-)如何变化?(填“增大”“减小”或“不变”);平衡移动方向如何?
|
加入的物质 |
少量(NH4)2SO4固体 |
少量HNO3溶液 |
少量KOH溶液 |
|
c(OH-)的变化 |
①
|
② |
③ |
|
平衡移动方向 |
④ |
⑤ |
⑥ |
20、(共10分)(1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示______________ _,(2分)K值大小与温度的关系是:温度升高,K值_____________ (2分)
(填一定增大、一定减小、或可能增大也可能减小)。
(2)在一体积为10L的容器中,通人一定量的CO和H2O,在850℃时发生如下反应:
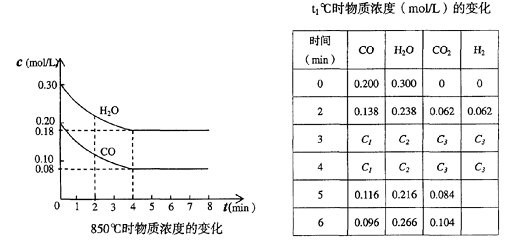
CO(g)十H2O(g)
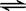 CO2(g)十H2 (g) ;△H<0
CO2(g)十H2 (g) ;△H<0
CO和H2O浓度变化如下图,则 0-4min的平均反应速率v(CO)=______ mol/(L·min) (2分)
(3) (每空1分) t℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如上表。
①表中3min-4min之间反应处于_________状态;
C1数值_________0.08 mol/L (填大于、小于或等于)。
②反应在4min-5min问,平衡向逆方向移动,可能的原因是________(单选),
表中5min-6min之间数值发生变化,可能的原因是__________(单选)。
a.增加水蒸气 b.降低温度
c.使用催化剂 d.增加氢气浓度
19、(4分)液化气中主要成分之一是丁烷( C4H10 )。在25℃ 101 kPa时,10 kg丁烷完全燃烧生成CO2和H2O放出热量5×105 kJ,丁烷的燃烧热为_________ __,丁烷燃烧的热化学方程式为_____________________________ 。
18、(8分)有一学生在实验室测某溶液的pH。实验时,他先用蒸馏水润湿pH试纸,然后用洁净干燥的玻璃棒醮取试样进行检测。
(1)该学生的操作是 (填“正确的”或“错误的”)。
(2)如不正确请说明理由,同时请分析是否一定有误差?答: 。
(3)若按此法分别测定C(H+)相等的盐酸和醋酸溶液的pH,误差较大的是 ,原因是 。
17、(6分)把NH4Cl晶体溶入水中,得到饱和NH4Cl溶液。若在该溶液中加入镁条,则观察到有气泡产生,点燃有爆鸣声,此气体是 ,产生该气体的原因是 ,
(用离子方程式表示)。微热后,能放出有刺激性气味的气体,它能使湿润的红色石蕊试纸变蓝,该气体是 。
16、用铂电极电解500 mL含KNO3和Cu(NO3)2两种溶质的混和溶液,一段时间后在两个电极上均生成11.2 L气体(标准状况下)。则原溶液中铜离子的物质的量浓度为 ( )
A、0.5 mol·L-1 B、1 mol·L-1 C、1.5 mol·L-1 D、2 mol·L-1
第二卷 (非选择题 共52分 )
15、将amLNO、bmLNO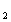 、xmLO
、xmLO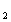 混合于同一集气瓶内,把集气瓶倒立在水中,充分反应后瓶内气体全部溶解,则x对a、b的函数关系式x=f(a,b)是( )
混合于同一集气瓶内,把集气瓶倒立在水中,充分反应后瓶内气体全部溶解,则x对a、b的函数关系式x=f(a,b)是( )
A、(a+b)∕2 B、(2a+b)∕3 C、(4a+b)∕5 D、 (3a+b)∕4
14、用物质的量都是0.1molCH3COOH和CH3COONa配制成1L混合液,已知其中C(CH3COO-)大于C(Na+),对该混合物溶液的下列判断正确的是 ( )
A、C(H+)>C(OH-)
B、C(CH3COO-)+C(CH3COOH)=0.1mol/L
C、C(CH3COOH)>C(CH3COO-)
D、C(CH3COO-)+C(OH-)=0.1mol/L
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com