
4.下列说法正确的是
A.含有金属阳离子的晶体一定是离子晶体
B.只有在原子中,质子数与核外电子数相等
C.非金属元素组成的化合物一定是共价化合物
D.碘与干冰受热变为气体,克服的都是分子间作用力
3.下列关于胶体的说法不正确的是
A.利用渗析的方法可以净和胶体
B.用丁达尔现象可区分溶液的胶体
C.将饱和FeC13溶液长时间加热,一定得到的是Fe(OH)3胶体
D.胶体粒子具有较大的表面积,能吸附离子面带电,故在电场作用下会产生电泳现象
2.下列说法正确的是
A.明矾净水过程中不涉及化学变化
B.由同种元素组成的物质一定是纯净物
C.风化、石油分馏和碘的升华都是物理变化
D.在化学反应中,反应前后原子种类、数目和质量一定不变
1.合理利用燃料减少污染符合“绿色奥运”理念,下列关于燃料的说法正确的是
A.“可燃冰”是将水变为油的新型燃料
B.氢气是具有热值高、无污染等优点的燃料
C.乙醇是比汽油更环保,不可再生的燃料
D.石油和煤是工厂经常使用可再生的化石燃料
24.(6分)标准状况下进行下列实验:甲、乙、丙各取30.0mL同浓度的盐酸,加入同一种镁铝合金,所取合金质量和产生气体的体积如表所列,计算:
|
实验序号 |
甲 |
乙 |
丙 |
|
合金质量(mg) |
510 |
765 |
1530 |
|
气体体积(mL) |
560 |
672 |
672 |
(1)盐酸的物质的量浓度;
(2)合金中Mg和Al的质量之比;
(3)丙实验后,还需向容器中加入上述盐酸溶液多少mL才能使剩余固体恰好完全溶解。
23.(11分)1L某混合溶液,可能含有的离子如下表:
|
可能大量含有的阳离子 |
H+、K+、Mg2+、Al3+、NH4+、Fe2+、Fe3+ |
|
可能大量含有的阴离子 |
Cl-、Br-、I-、ClO-、AlO2- |
(1)往该溶液中逐滴加入NaOH溶液,产生沉淀的物质的量(n)与加入NaOH溶液的体积(V)的关系如图所示。则该溶液中确定含有的离子是 ,一定不含的的阳离子是 ,一定不存在的阴离子是 。
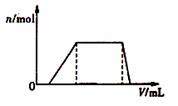
(2)经检测,该溶液中还含有大量的Cl-、Br-、I-,若向1L该混合溶液中通入一定量的Cl2,溶液中Cl-、Br-、I-的物质的量与通Cl2的体积(标准状况)的关系如下表所示,分析后回答下列问题:
|
Cl2的体积(标准状况) |
2.8L |
5.6L |
11.2L |
|
n(Cl-) |
1.25mol |
1.5mol |
2mol |
|
n(Br-) |
1.5mol |
1.4mol |
0.9mol |
|
n(I-) |
a mol |
0 |
0 |
①当通入Cl2的体积为2.8L时,溶液中发生反应的离子方程式为 。
②原溶液中Cl-、Br-、I-的物质的量浓度之比为 。
22.(10分)铁是人体必须的微量元素,治疗缺铁性贫血的常见方法是服用补铁药物。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。好学同学为了检测“速菲”药片中Fe2+的存在,设计并进行了如下实验:
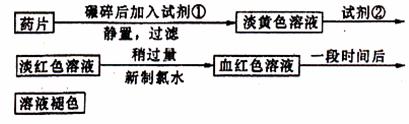
试回答下列问题:
(1)检验Fe3+的离子方程式是 。
(2)试剂①是 ,试剂②是 ,加入新制氯水后,氯水参加的离子反应方程式是 。
(3)加入试剂②后溶液中颜色由淡黄色转变为淡红色是因为 ,写出+2价铁在酸性介质中在空气中转化为+3价铁的离子方程式 。
(4)好学同学猜想血红色溶液变为无色溶液的原因是溶液中的+3价铁被还原为+2价铁,你认为该同学的猜想是否合理? 。若你认为不合理,请你提出你的猜想:(若你认为合理,后面的提问不要作用) ;再根据你的猜想设计一个简单的实验加以验证
。
21.(12分)如图:A为直流电源,B为浸透饱和氯化钠溶液和酚酞试液的滤纸,C为电镀槽,接通电路后,发现B上的c点显红色,请填空:
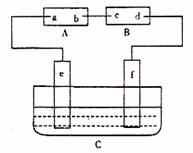
(1)电源A上的a为 极;
(2)滤纸B上发生反应的总化学方程式为: ;
(3)欲在电镀槽中实现铁上镀锌,则电极e上发生的反应为: ;电极f上发生的反应为: ,槽中盛放的电解质溶液(即电镀液)要用含 的溶液。
(4)若A中的总反应为:CH4+2O2+2KOH K2CO3+3H2O,则a电极反应式为:
;
b电极反应式为: 。若电解质溶液中损失了1mol KOH,则参加反应的CH4在标况下的体积为 L。
20.(6分)根据下表中提供的数据回答问题。
|
|
NaCl |
MgCl2 |
AlCl3 |
SiCl4 |
|
熔点 |
810℃ |
710℃ |
180℃ |
-68℃ |
|
沸点 |
1465℃ |
1418℃ |
160℃ |
57℃ |
(1)根据表中数据推测,上述四种氯化物中属于分子晶体的是 。
(2)另设计一个实验,判断氯化铝是离子化合物还是共价化合物
。
(3)NaCl的键的强度比MgCl2的 。(填“强”“弱”或“无法比较”)
19.(6分)在一定温度下,a. 盐酸;b. 硫酸;c. 醋酸三种溶液。
(1)当三种酸的物质的量浓度相同时,c(H+)由大到小的顺序是 。
(2)同体积,同物质的量浓度的三种酸,用相同浓度的NaOH溶液中和,需要NaOH溶液的体积的大小关系是 。
(3)若三者c(H+)相同时,它们的物质的量浓度由大到小的顺序是 。
(4)当三者c(H+)和体积都相同时,分别加入足量的镁,生成的氢气在相同状况下的体积大小关系是 。
(5)当pH相同、体积相同时,分别加入形状完全相同的锌粒,若产生相同状况下相同体积的H2,反应所需时间的长短关系是 。
(6)将pH相同的三种酸均加水稀释至原来的100倍后,pH的大小关系是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com