
22.将等物质的量的X、Y 气体充入一个密闭、体积恒定的容器中,在一定条件下发生如下反应并达到平衡:X(g)+Y(g)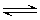 2Z(g);ΔH<0.
当改变某个条件并维持新条件直至新平衡,下表中关于新平衡与原平衡的比较,正确的是 (
)
2Z(g);ΔH<0.
当改变某个条件并维持新条件直至新平衡,下表中关于新平衡与原平衡的比较,正确的是 (
)
|
|
改变的条件
|
新平衡和原平衡的对比 |
|
A |
升高温度 |
X的体积分数变大 |
|
B |
体积不变的前提下,充入不参加反应的稀有气体,增大压强 |
Z的浓度变大 |
|
C |
加入正催化剂 |
Y的体积分数变大 |
|
21.下列各组离子,在强碱性溶液中可以大量共存的是 ( )
|
|
改变的条件 |
新平衡和原平衡的对比 |
|
A |
升高温度 |
X的体积分数变大 |
|
B |
体积不变的前提下,充入不参加反应的稀有气体,增大压强 |
Z的浓度变大 |
|
C |
加入正催化剂 |
Y的体积分数变大 |
|
D |
充入一定量Y气体 |
X的体积分数变大 |
|
|
改变的条件 |
新平衡和原平衡的对比 |
|
A |
升高温度 |
X的体积分数变大 |
|
B |
体积不变的前提下,充入不参加反应的稀有气体,增大压强 |
Z的浓度变大 |
|
C |
加入正催化剂 |
Y的体积分数变大 |
|
D |
充入一定量Y气体 |
X的体积分数变大 |
A.K+、Na+、HSO3-、Cl- B.Na+、Ba2+、AlO2-、NO3-
C.NH4+、K+、Cl-、NO3- D.K+、Na+、ClO-、SO32-
20.X、Y、Z是3种短周期元素,其中X、Y位于同一族,Y、Z处于同一周期。X原子的最外层电子数是其电子层数的3倍。Z原子的核外电子数比Y原子少1。下列说法不正确的是: ( )
A.元素非金属性由弱到强的顺序为Z<Y<X
B.Y元素最高价氧化物对应水化物的化学式可表示为H2YO4
C.3种元素的气态氢化物中,Z的气态氢化物最稳定
D.原子半径由大到小的顺序为Z>Y>X
19.在第三届东北师大附中体育节上使用的发令枪中所用的“火药”成分是氯酸钾和红磷,经撞击发出响声,同时产生白色烟雾。撞击时发生的化学反应方程式为:
5KClO3+6P=3P2O5+5KCl,则下列有关叙述错误的是 ( )
A.上述反应中氧化剂和还原剂的物质的量之比为5:6
B.产生白色烟雾的原因是生成的P2O5白色固体小颗粒(烟)吸水性很强,吸收空气中
的水分,生成酸滴(雾)
C.上述反应中消耗3molP时,转移电子的物质的量为15mol
D.因红磷和白磷互为同分异构体,所以上述火药中的红磷可以用白磷代替
18.由可逆反应测绘出图象如图,纵坐标为生成物在平衡混合物中的百分含量,下列对该反应的判断正确的是( )
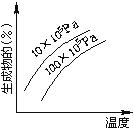
A.反应物中一定有气体B.生成物中一定有气体
C.正反应一定是放热反应
D.无法判断出该正反应是吸热反应还是放热反应
16.下列离子方程式中正确的是 ( )
A.亚硫酸氢钙与稀硝酸反应:HSO3-+H+=H2O+SO2↑
B.澄清石灰水与醋酸溶液混合:Ca(OH)2+2CH3COOH=Ca2++2CH3COO-+2H2O
C.氢氧化镁溶于稀硫酸:Mg(OH)2+2H+=Mg2++2H2O
D.向酸性FeSO4溶液中滴入H2O2:Fe2++H2O2+2H+=Fe3++2H2O
15.同主族元素所形成的同一类型的化合物,其结构和性质往往相似,化合物PH4Cl是一种无色晶体,下列对它的描述中不正确的是 ( )
A.在加热时此化合物可以分解 B.它是一种共价化合物
C.这种化合物能跟碱发生反应
D.该化合物可以由PH3跟HCl化合而成
14.X、Y、Z三种元素,已知X和Y原子核外电子层数相同,Y和Z原子最外层电子数相同,又知三种元素原子最外层电子数总和为14,而质子数总和为28,则三种元素为( )
A.N、P、O B.N、C、Si C.B、Mg、Al D.C、N、P
13.下列说法正确的是 ( )
A.将pH试纸浸在溶液中,观察其颜色变化,跟标准比色卡比较
B.电解饱和食盐水时,阴极室得到氢氧化钠溶液和氢气
C.铁器上镀银,必须把铁器接电源的正极,银接电源负极,用银离子的可溶盐溶液作
电解液
D.用盐酸滴定NaOH溶液的实验中,锥形瓶用水洗后,再用NaOH冲洗2~3次
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com