
8.下列叙述正确的是
A.金属与盐溶液的反应都是置换反应
B.阴离子都只有还原性
C.与强酸、强碱都反应的物质只有两性氧化物或两性氢氧化物
D.分子晶体中都存在范德瓦耳斯力,可能不存在共价键
7. 1 mol过氧化钠与2 mol碳酸钠固体混合后,在密闭容器中加热充分反应,排出气体物质后冷却,残留的固体物质是
A.Na2CO3 B.Na2O2 Na2CO3
C.NaOH Na2CO3 D.Na2O2 NaOH Na3CO3
6.对H2O的电离平衡不产生影响的粒子是
5.据报道,我国拥有完全自主产权的氢氧燃料电池车将在北京奥运会期间为运动员提供服务。某种氢氧燃料电池的电解液为KOH溶液,下列有关该电池的叙述不正确的是
A.正极反应式为: 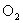 +2H2O+4e-=4OH-
+2H2O+4e-=4OH-
B.工作一段时间后,电解液中KOH的物质的量不变
C.该燃料电池的总反应方程式为:2H2+O2=2H2O
D.用该电池电解CuCl2溶液,产生2.24 L Cl2(标准状况)时,有0.1 mol电子转移
29.(16分)某化学研究性学习小组的同学为了探究氨气具有还原性,设计了氨气与CuO反应的探究实验,请你根据下列装置图完成下列内容:
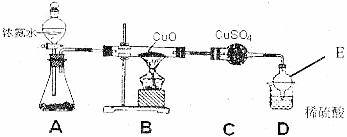
(1)如何检验装置A的气密性,具体操作是: ;
(2)上述装置中,为快速制取少量氨气,A中所盛试剂为 (填一种试剂);
(3装置E的作用是 ;
(4)该装置在设计上有一定的缺陷,为保证实验结果的准确性,你对该装置的改正措施是 ;
(5)利用改正后的装置进行实验,观察到CuO变为红色物质,无水CuSO4变蓝色,同时生成一种无染色的气体。写出上述反应的化学方程式 ;
(6)若氧化铜粉末质量减少了mg,则电子转移为 mol。
28.(16分)咖啡酸(下式中的A)是某种抗氧化剂成分之-,A结构中苯环上有3个取代基,且取代基中不含支链,A遇FeCl3溶液发生显色反应。A有如下转化关系:

(1)咖啡酸A中含氧官能团的名称为 ;
(2)写出A生成D的化学:反应方程式 ,该反应的反应类型为 。
(3)a mol咖啡酸A与足量钠反应生成气体(标准状况) L。
(4)蜂胶的主要成分(分子式为C17H16O4)是由咖啡酸A和-种芳香醇E发生酯化反应生成的,已知E的芳香醇类同分异物体有5种,其中三种为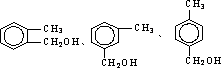 ,请写出另外两种
、 。
,请写出另外两种
、 。
27.(12分)已知:A、B、C均为常见的单质或化合物,它们在一定条件下有如下转化关系

(1)若A可作为呼吸面具和潜水艇中氧气的来源,则化合物B的电子式: ;
(2)若A、B、C均为化合物,且C遇到空气立即变为红棕色,则A与H2O反应的化学方程式为 ;
(3)若C为H2,B为氧化物,则A可能是(写出-种即可) ;
(4)若B、C均为生活中常见的有机物,则B和C反应的化学方程式为 。
26.(16分)A、B、C、D、E均为短周期元素且原子序数依次增大,B原子的最外层电子数是内层电子数的3倍,D元素的最高价氧化物的水化物呈酸性,D和B可形成DB2和DB3型化合物,A和E可形成18电子微粒,C元素是地壳中含量最多的金属元素。
根据以上叙述回答下列问题:
(1)E元素在周期表中的位置是 ;
(2)由1mol气态DB2与B单质反应生成lmol气态DB3,放出98.3KJ的热量,则由DB2转化成DB3的热化学方程式是: ;
(3)写出C的阳离子和含C元素的阴离子在水溶液中反应的离子方程式: ;
(4)A2B和A2D比较,沸点高的是(写分子式) ,其原因是 ;
(5)Na2D溶液呈 性,其溶液中阴离子浓度大小关系是: 。
13.某有机物的结构简式为: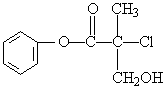 下列说法中不正确的是
下列说法中不正确的是
A.该物质分子式为:C10H11O3Cl
B.该物质既可发生水解反应又可发生消去反应
C.1mol该物质可以与3mol氢气发生加成反应
D.1mol该物质最多可以和2mol的NaOH反应
非选择题
(非选择题 共10小题,共174分)
12.下列各组物质中,X表示某物质,括号内为所含杂质,Y表示要除去杂质所加入的试剂,Z表示除杂质的操作方法,其中正确的一组是
|
|
X |
Y |
Z |
|
A |
苯(苯酚) |
溴水 |
分液 |
|
B |
CO2(HCl) |
饱和Na2CO3溶液 |
洗气 |
|
C |
Fe粉(Al粉) |
NaOH溶液 |
过滤 |
|
D |
SiO2(Fe2O3) |
NaOH溶液 |
过滤 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com