
28.(15分)在实验室中用下图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质。
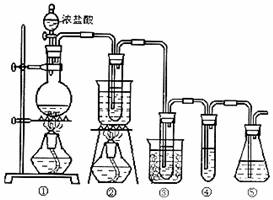
图中:①为氯气发生装置;②的试管里盛有15mL 30% KOH溶液,并置于热水浴中;③的试管里盛有15mL 8% NaOH溶液,并置于冰水浴中;④的试管里加有紫色石蕊试液;⑤为尾气吸收装置。
请填写下列空白:
(1)制取氯气时,在烧瓶里加入一定量的二氧化锰,通过 (填写仪器名称)向烧瓶中加入适量的浓盐酸。实验时为了除去氯气中的氯化氢气体,可在①与②之间安装盛有 (填写下列编号字母)的净化装置。
A.碱石灰 B.饱和食盐水
C.浓硫酸 D.饱和碳酸氢钠溶液
(2)比较制取氯酸钾和次氯酸钠的条件。二者的差异是 。反应完毕后冷却后,②的试管中有大量晶体析出。下图中符合该晶体溶解度曲线的是
(填写编号字母);从②的试管中分离出该晶体的方法是 (填写实验操作名称)。

(3)本实验中制取次氯酸钠的离子方程式是: 。
(4)实验中可观察到④的试管里溶液的颜色发生了如下变化,请填写下表中的空白:
|
实验现象 |
原因 |
|
溶液最初从紫色逐渐变为 色 |
氯气与水反应生成的H+使石蕊变色 |
|
随后溶液逐渐变为无色 |
|
|
然后溶液从无色逐渐变为 色 |
|
27.(15分)固体X是一种常见金属元素M和一种常见非金属元素组成的化合物,其中金属元素M与另一元素的质量比为14:1。在一定条件下,X可发生如下框图的转化关系,有的反应标出全部产物,有的反应标出部分产物,已知A为一种黄色的溶液,B为一种无色无味的液体,P为混合气体,R是无色无味能使澄清石灰水变浑浊的气体,E为红色物质固体,Q为常见非金属单质。

试回答下列问题:
(1)金属元素M的真实元素符号为 ;E物质的化学式为 ;Q物质的化学式为 。
(2)实现G→H,欲不引入新的杂质,N可以选择适量的下列物质是 (填序号)
①KMnO4 ②浓H2SO4 ③H2O2 ④C12
(3)写出下列反应的离子方程式:
D→G ; H→C 。
(4)写出X和浓硝酸反应的化学方程式 。
26.某研究性学习小组成员,利用稀硫酸与某金属的反应来探究影响化学反应速率的因素,下表是研究过程中记录的实验数据:(表中某些数据记录已模糊不清,个别数据已丢失。)
|
实验序号 |
金属质 量/g |
金属 状态 |
c(H2SO4)/mol·L-1 |
V(H2SO4)/mL |
溶液温度/℃ |
金属消失的时间/s |
|
|
反应前 |
反应后 |
||||||
|
1 |
0.10 |
丝 |
0.5 |
50 |
20 |
34 |
500 |
|
2 |
0.10 |
粉末 |
0.5 |
50 |
20 |
35 |
50 |
|
3 |
0.10 |
丝 |
0.7 |
50 |
20 |
36 |
数据模糊 |
|
4 |
0.10 |
丝 |
0.8 |
50 |
20 |
35 |
200 |
|
5 |
0.10 |
粉末 |
0.8 |
50 |
20 |
36 |
数据模糊 |
|
6 |
0.10 |
丝 |
1.0 |
50 |
20 |
35 |
数据模糊 |
|
7 |
0.10 |
丝 |
1.0 |
50 |
35 |
数据模糊 |
50 |
|
8 |
0.10 |
丝 |
1.1 |
50 |
20 |
34 |
100 |
|
9 |
0.10 |
丝 |
1.1 |
50 |
数据丢失 |
44 |
40 |
若实验操作、数据记录均是正确的,请分析上述数据,回答下列问题:
(1)该实验主要是探究 因素对反应速率的影响。
(2)经仔细辨认,模糊的数据疑为25、50、125、250,试将这些疑似数据填入表中,使实验数据较为合理。
(3)试猜测实验9反应前溶液的温度约为 ℃。推测的依据是
。
13.如下图所示,甲、乙之间的隔板K可以左右移动,甲中充入2molA和1molB,乙中充入2molC和1mol He,此时K停在0处。在一定条件下发生可逆反应:2A(g)+(B) 2C(g),反应达到平衡后,恢复到反应发生前的温度。下列有关说法错误的是 ( )
2C(g),反应达到平衡后,恢复到反应发生前的温度。下列有关说法错误的是 ( )
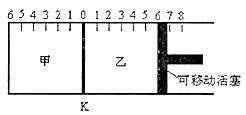
A.根据隔板K滑动与否可判断左右两边的反应是否达到平衡
B.达到平衡后,隔板K最终停留在左侧刻度0-2之间
C.到达平衡时,甲容器的C的物质的量应大于乙容器中C的物质的量
D.若平衡时K停留在左侧1处,则活塞应停留在右侧6处
|
12.在体育比赛中使用兴奋剂是一种不符合奥林匹克精神的行为,某种兴奋剂的结构简式如下图所示,有关该物质的说法中正确的是 ( )
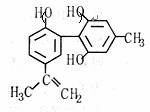
A.分子内所有的原子在同一平面上
B.因为该物质是苯酚的同系物所以遇FeC13溶液可呈现紫色
C.1mol该物质分别与浓溴水和H2反应时,最多消耗Br2和H2分别为4mol和7mol
D.若能使酸性KMnO4溶液的紫色褪去,则可证明该物质分子中是否含有碳碳双键
11.下图所示,止水夹开始时处于关闭状态,将液体A滴入试管2中与气体B充分反应,打开止水夹,可发现试管1内的水立刻沸腾了。则液体A和气体B的组合不可能是下列
( )
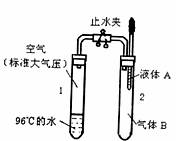
A.氧氧化钠溶液、二氧化碳
B.水、氨气
C.氢氧化钠溶液、一氧化碳
D.水、二氧化碳
9.有X、Y两种元素,原子序数≤20,X的原子半径小于Y,且X、Y原子的最外层电子数相同(选项中m、n均为正整)下列说法正确的是 ( )
A.若X(OH)n为强碱,则Y(OH)n也一定为强碱
B.若HnXOm为强酸,则X的氢化物溶于水一定显酸性
C.若X元素形成的单质是X2,则Y元素形成的单质一定是Y2
D.若Y的最高正价为+m,则X的最高正价一定为+m
|
A.Na2O B.Na2O2 C.Na2和Na2O2 D.Na2O2和NaO2
8.NA代表阿伏加德罗常数,下列说法正确的是 ( )
A.标准状况下,22.4L CC14中含有氯原子数目为4NA
B.7g CnH2n中含有的氢原子数目为NA
C.18g D2O中含有的质子数目为10NA
D.1L 0.5mol·L-1Na2CO3溶液中含有的CO32-数目为0.5NA
7.下列有关化学概念的叙述正确的是 ( )
A.酸性氧化物就是水溶性呈酸性的氧化物
B.碳水化合物就是碳和水组成的化合物
C.弱酸就是溶于水后水溶液中c(H+)很小的酸
D.单糖就是不能水解的糖
6.下列关于日常生活中的化学问题判断正确的是 ( )
A.为了保证食品的卫生和绿色,在食品中不能添加任何化学添加剂
B.在人类必须的三大营养素糖类、油酯、蛋白质中,油酯是热能最高的营养素
C.用硬水洗涤衣物时,肥皂比合成洗涤剂有更好的去污效果
D.用于盛装食品的塑料袋是其主要成分是聚氯乙烯
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com