
10、重金属离子有毒,实验室有甲乙两种废液均有一定毒性,甲废液呈碱性,有毒离子为Ba2+ ,如将甲乙两废液按一定比例混合毒性会明显降低,乙废液中可能含有的离子是( )
A、Cu2+ Cl- B、Mg2+ SO42- C、Cu2+ SO42- D、Ag+ NO3-
9、某溶液中由水电离出来的H+浓度为10-12 mol/L该溶液中一定能大量共存的离子组为( )
A、Fe3+ Na+ SO42- Cl- B、NH4+ K+ Cl- NO3-
C、Ba2+ Na+ Cl- NO3- D、K+ Na+ I- NO3-
8、下列离子方程式正确的是( )
A、少量的亚硫酸氢钠溶液与足量的澄清石灰水混合:
HSO3- + OH- == SO32- + H2O
B、 少量的二氧化碳通入足量的氢氧化钠溶液中
CO2 + OH- == HCO3-
C、 硫酸氢钠溶液与氢氧化钡溶液混合后溶液呈中性
H+ + SO42- + Ba2+ +OH- ==BaSO4 + H2O
D、向溴化亚铁溶液中通入少量氯气
Cl2 + 2Fe2+ == 2Fe3+ + 2Cl-
7、超氧化钾(KO2)与水反应生成氢氧化钾和氧气,其还原剂和氧化剂的质量比为( )
A、1:1 B、2:1 C、3:1 D、4:1
6、重铬酸氨[(NH4)2Cr2O7]受热发生氧化还原反应,下列各组分解产物符合实际的是( )
A、Cr2O3 + NH3 + H2O B、CrO3 + NH3 + H2O
C、Cr2O3 + N2 + H2O D、CrO3 + N2 + H2O
29.(15分)有机物A.B.C互为同分异构体,分子式为C5H8O2,有关的转化关系如图所示。已知:A的碳链无支链,且1 mol A能与4 mol Ag(NH3)2OH完全反应;B为五元环酯。
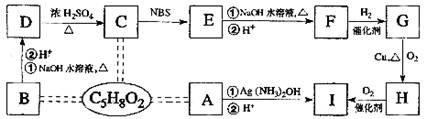
提示:CH3-CH=CH-R Br-CH2-CH=CH-R
(1)A中所含官能团是
。
Br-CH2-CH=CH-R
(1)A中所含官能团是
。
(2)B的结构简式为 .H的结构简式为 。
(3)写出下列反应方程式(有机物用结构简式表示)
C→E ;
E→F(只写①条件下的反应) 。 (4)请指出下列转化的反应类型:
D→C: C→D:
(5)F的加聚产物的结构简式为 。
28.(15分)氨的催化氧化制硝酸的关键步骤是用氧气来氧化氨气制取二氧化氮。请用以下提供的仪器及试剂(所提供的仪器和试剂有多余的),设计组装一套实验装置,以铂为催化剂用氧气氧化氨气制取二氧化氮。
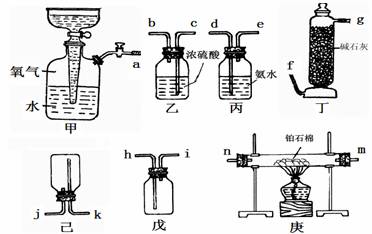
(1)应选用的仪器是: 填仪器下边的甲.乙.丙…等符号)
(2)用玻璃管和胶管(未画出)连接上述仪器,这些仪器的接口的连接顺序是(a.b.c…填写):a接 , 接 , 接 , 接 。
(3)实验前如何检查甲装置的气密性 。
(4)庚装置中发生的化学反应的方程式是: 。
(5)写出获得甲装置中的氧气的任意两种制取方法(用两个反应化学方程式来表示):
, 。
27.(15分)已知A、C、D、F均是溶液,其中A、C是重要的基础化工原料,C可使酚酞试液变红。B、G、I、J、K是固体,其中B是常见的金属单质,G是常见的非金属单质。E、H是气体,且E是单质。H、J、K、L均是由两种元素组成的化合物,L常温下为液态。物质之间的转化关系如下图所示。请回答下列问题:
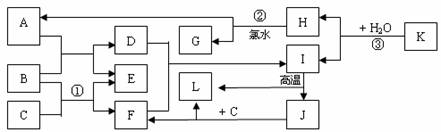
(1)元素B在周期表中的位置是 。J的化学式是 。
(2)反应①所得溶液中各离子浓度由大到小顺序为 。
(3)反应②的化学方程式为 。
反应③的化学方程式为 。
(4)工业上可通过电解熔融的J来制取B的单质,当有6mol电子发生转移时,可得到
g单质B。
26.(15分)A、B、C、D、E、F六种元素分布在三个不同的短周期,它们的原子序数依次增大,其中B与C为同一周期,A与D、C与F分别为同一主族,A、D两元素的原子核内的质子数之和是C、F两元素原子核内质子数之和的一半。又知六种元素所形成的常见单质在常温常压下有三种是气体,三种是固体。请回答下列问题:
(1)由A、C两元素可以组成X、Y两种化合物,X在一定条件下可以分解成Y,X的电子式为 ,其分子属于 (填“极性”、“非极性”)分子。
(2)E是非金属元素,但能表现出一些金属元素的性质,请写出单质E与氢氧化钠溶液反应的离子方程式
(3)一定条件下,A的单质气体与B的单质气体充分反应生成6.8g W气体(已知n(A):n(B)=3:1),可放出18.44 kJ热量,则该反应的热化学方程式
(4)A的单质与C的单质在KOH的浓溶液中可以形成原电池,如果以金属M和金属N为惰性电极,在电池的M极通入A的单质气体,N极通入C的单质气体,则N极的电极反应式为 。
(5)在10升的密闭容器中,通入2mol的FC2气体和3molC的气体单质,一定条件下反应后生成FC3气体,当反应达到平衡时,单质C的浓度为0.21mol/L,则平衡时FC2的转化率为 。
13.agFe2O3和A12O3组成的混合物全部溶于20mL pH=1的硫酸,反应后向所得溶液中加入10mLNaOH溶液,恰好使Fe2+.A13+完全沉淀,则c(NaOH)为 ( )
A.0.1mol·L-1 B.0.2mol·L-1
C.0.4mol·L-1 D.0.8mol·L-1
第Ⅱ卷
|
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com