
13.人们在对烷烃分子空间结构的研究中发现某一系列的烷烃分子只有一种一卤取代物。如:
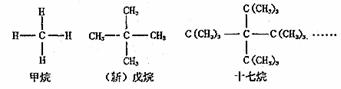
下列说法正确的是 ( )
A.这一系列烷烃中,相邻的烃分子之间碳数之差一定为偶数
B.这一系列的第6种烷烃的碳原子数为2×35
C.这一系列烷烃中,其中含碳量最高的烷烃中碳含量的约为92.3%
D.除这一系列烷烃外,其它烷烃分子不可能只有一种一卤取代物
第II卷(非选择题,共174分)
12.按照图3接通线路,反应一段时间后,下列说法正确的是 ( )
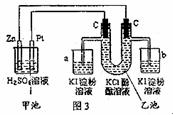 图3
图3
A.甲、乙两池的四个电极上均会产生气泡
B.a、b两烧杯中溶液颜色均有明显变化
C.甲、乙两池中溶液的pH均增大
D.进入a、b两烧杯中气体的质量相等
11.下列实验操作或叙述正确的是 ( )
A.灼烧氢氧化钠或碳酸钠固体选用瓷坩埚
B.用蒸馏水润湿后的pH试纸测溶液的pH一定有误差
C.向沸腾的NaOH稀溶液中滴加FeCl3饱和溶液,可以制得Fe(OH)3胶体
D.实验室配制氯化亚锡(SnCl2)溶液时,可先将氯化亚锡(SnCl2)溶解在较浓的盐酸中,再中入蒸馏水稀释,最后加入少量锡粒
9.反应:①PCl5(g)  PCl3(g)+Cl2(g) ②2HI(g)
PCl3(g)+Cl2(g) ②2HI(g)  H2(g)+I2(g) ③2NO2
H2(g)+I2(g) ③2NO2 N2O4在一定条件下,达到化学平衡时,反应物的转化率是a%。若保持各反应的温度和容器的体积都不变,分别再加入一定量的各自反应物,则转化率 ( )
N2O4在一定条件下,达到化学平衡时,反应物的转化率是a%。若保持各反应的温度和容器的体积都不变,分别再加入一定量的各自反应物,则转化率 ( )
A.均不变 B.①增大②不变③减小
C.均增大 D.①减小②不变③增大
|
A.100mL 0.2mol/L乙酸溶液中,乙酸分子数目为0.02NA
B.1mol O2在反应中作氧化剂时,所得电子数一定为4NA
C.1L 1mol/L的Na2CO3溶液中CO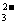 与HCO
与HCO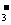 的离子数之和为NA
的离子数之和为NA
D.1mol NaHSO4晶体中离子总数为2NA
8.X、Y、Z、W是原子序数依次增大的四种常见元素。W和Y元素形成的化合物W3Y4具有磁性。X的单质在Y2中燃烧可生成XY和XY2两种气体。Z的单质是一种金属,该金属在XY2中剧烈燃烧生成黑、白两种固体。下列说法错误的是 ( )
A.XY2分子为极性键形成的非极性分子
B.X元素形成的单质的晶体类型可能是分子晶体
C.W元素在周期表中位于过渡元素区,属副族元素
D.Z单质在XY2中燃烧的反应,属于置换反应
7.能正确表示下列化学反应的离子方程式是 ( )
A.氢氧化亚铁固体加入足量的稀硝酸中:Fe(OH)2+2H+=Fe2++2H2O
B.NaHCO3的水解:HCO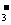 +H2O
+H2O H3O++CO
H3O++CO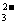
C.用碳酸钠溶液吸收少量二氧化硫:2CO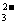 +SO2+H2O=2HCO
+SO2+H2O=2HCO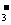 +SO
+SO
D.硫酸铝溶液中加入过量氨水:Al3++3OH-=Al(OH)3↓
6.下列关于环境问题的说法不正确的是 ( )
A.NO2在紫外线照射下,会发生一系列光化学反应,产生有毒的光化学烟雾
B.PH在5.6-7.0之间的降水通常称为酸雨
C.合成材料废弃物造成了严重的环境问题,“白色污染”即是其中最突出的例子
D.废旧电池渗出的重金属离子会造成地下水和土壤的污染
29.(15分)阿司匹林(AsPPrin)是应用最广泛和最成功的合成药物,具有解热、抗炎和镇痛作用。下图是以苯为原料合成阿司匹林反应流程图(已知由CO2可在苯环上引入羧基)。
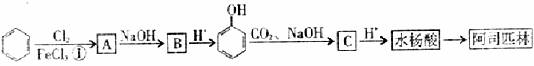
请回答下列问题:
(1)流程中第一步的反应所属的反应类型是 ;
(2)由流程可知,水杨酸是合成阿司匹林的重要原料,已知水杨酸的化学名称为邻羟基苯甲酸,其结构式为,则分子式是 。
(3)水杨酸有多种同分异构体,其中即既属于酚类又属于酯类化合物的同分异构体有
种。
(4)流程中由水杨酸生成阿司匹林反应为酯化反应,又知阿司匹林经酸性水解生成水杨酸和乙酸,则阿司匹林的结构简式是 ;
(5)写出阿司匹林药与足量NaOH溶液反应的化学方程式 ;
(6)写出物质C与二氧化碳水溶液反应的化学方程式
(7)阿司匹林药片需要保存在干燥处,受潮的药片易变质不宜服用;检验受潮药片是否变质的试剂是 (只选一种试剂即可)
28.(15分)实验室有一瓶Na2SO3固体,其中可能含有NaCl、Na2SO4、KNO3、K2CO3、K2SO4中的一种或几种杂质,可通过下列实验确定该样品的成分及Na2SO3质量分数。
称此样品5.0g,加入5.00mL6mol•L-1硫酸溶液(过量),产生无色气体560mL(已换算为标准状况),向逸出气体后的溶液中加入过量的BaCl2溶液,经过滤、干燥得到白色沉淀9.32g。透过蓝色钴玻璃观察,滤液的焰色反应无紫色。
请根据实验记录填写下列空白:
(1)若用下图所示仪器组装进行上述实验,气流从左到右,各仪器导管口连接的顺序是(填字母编号) 接 , 接 , 接 。
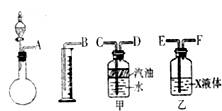
(2)乙中液体X是 ,甲中汽油的作用是 。
(3)实验中,准确测出生成的气体体积的有关操作及注意事项是 。
(4)根据实验记录分析:样品中Na2SO3质量分数是 ;样品中一定含有的杂质是 。
27.(15分)A、B、C、D、E、F是六种中学化学常见的物质,它们之间的转化关系如图所示:
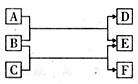
(1)若A、B、C均为氧化物,且E为气体单质,F晶体中所含的阴、阳离子均分别含有10个电子。则B的电子式是 ,B与C反应生成E与F的离子方程式是 。
(2)若A、C、E都是氢化物,三者的分子都是极性分子,其中C的相对分子质量最小;D、E、F都是氧化物,其中D、F为有毒气体。
①A、C、F沸点由高到低的顺序是 ,A、C、E三种氢化物稳定性最强的是 (填化学式)
②B跟C反应生成E和F的化学方程式是 。
③A跟D常温下反应可生成一种单质,其化学方程式是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com